よむ、つかう、まなぶ。
資料2-3 外国での新たな措置の報告状況[1.4MB] (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
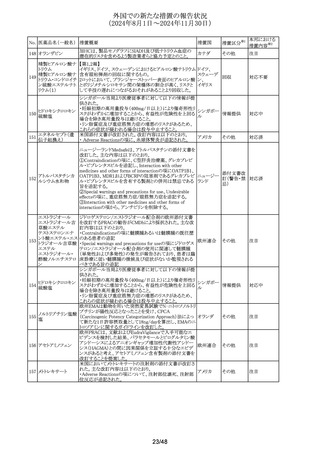
外国での新たな措置の報告状況
(2024年8月1日~2024年11月30日)
No. 医薬品名(一般名) 措置概要
38 フェノフィブラート
措置国
フェノフィブラートの米国添付文書が改訂された。主な内容
は以下のとおり。
Contraindicationsの項
①「透析を受けている患者を含む重度の腎障害」から「末期
腎疾患(ESRD)および透析を受けている患者を含む重度の
腎障害」に変更する。
②「フェノフィブリン酸またはフェノフィブラートに対する過敏
症」から「フェノフィブリン酸、フェノフィブラートあるいは本剤
の賦形剤に対する過敏症。フェノフィブラートでアナフィラキ
シーおよび血管浮腫を含む重篤な過敏反応が報告されて
いる。」に変更する。
Warnings and Precautionsの項
③死亡率および冠動脈性心疾患の罹患率の項に、2型糖
尿病患者を対象とした2件の大規模ランダム化比較試験に
おいて、フェノフィブラートは心血管疾患の罹病率および死
亡率を低下させなかったこと、バックグラウンドでスタチン療
法を受けている2型糖尿病患者を対象とした大規模無作為
化プラセボ対照試験において、ペマフィブラートは心血管疾
患の罹病率および死亡率を低下させなかった旨を追記す
る。
④静脈塞栓性疾患の項に、ペマフィブラートを用いた心血
管系アウトカム試験における肺塞栓症、深部静脈血栓症の
発現率を追記する。
⑤ミオパチーと横紋筋融解症の項のミオパチーのリスク因
子、ミオパチーと横紋筋融解症のリスクを予防または軽減す
アメリカ
るための手順を更新する。
⑥血清クレアチニンの増加の項に、本剤は末期腎疾患
(ESRD)および透析を受けている患者を含む重度の腎障害
患者には禁忌である旨を追記する。
⑦胆石症の項に、胆嚢疾患の既往がある患者には禁忌で
ある旨を追記する。
⑧過敏症反応の項に、本剤はフェノフィブラート、フェノフィ
ブリン酸あるいは本剤の成分に対して過敏症のある患者に
は禁忌である旨を追記する。
Adverse Reactionsの項
⑨ミオパチーと横紋筋融解症、血清クレアチニンの上昇、胆
石症、クマリン系抗凝固薬による出血リスクの上昇、血液学
的変化を追記する。
⑩Clinical Trail Experienceの項に、高トリグリセリド血症また
は原発性高脂血症の成人患者を対象に、他のフェノフィブ
ラート製剤の十分かつ適切にコントロールされた試験に基
づいて、本剤の安全性が確立されている旨を追記する。
⑪Clinical Trail Experienceの項の蕁麻疹、肝酵素の増加に
関する記載を更新する。
⑫Postmarketing Experienceの項に、アナフィラキシー、血
管浮腫を追記する。
Use in Specific Populationsの項
⑬小児、高齢者、腎障害、肝障害の項に関する記載を更新
する。
⑭Pregnancy、Lactationの項をPLLRに従い更新する。
措置区分※1
本邦における
措置内容※2
添付文書改
訂(警告・禁 注目
忌)
エプタコグ アル
チェコにおいて、特定の製造ラインで製造された一部の製
39 ファ(活性型)(遺伝 品における薬剤充填量の不足が生じたため、1mg及び2mg チェコ
子組換え)
製剤の回収が行われた。
回収
対応不要
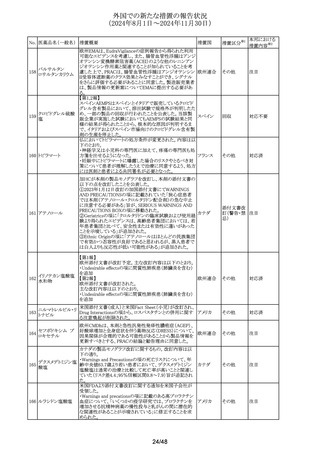
【第1,2報】
欧州添付文書が改訂された。改訂内容は以下のとおり。
・Warnings and Precautions for Useの項について、血中濃
度が高い場合にQT延長があらわれるおそれがある旨を追
記し、中等度以上の肝機能障害患者では投与しないことが
望ましいこと、重度の腎機能障害患者でも投与しないことが
望ましいが、投与する必要がある場合には心電図等をモニ
ベロトラルスタット塩 タリングするよう追記された。
40
アメリカ
酸塩
・Interaction with other medicinal products and other forms
of interactionのP-gpとBCRP阻害剤の項について、 市販後
に得られたデータではP-gp及びBCRP阻害剤であるシクロス
ポリンを併用した際に、血中本薬濃度がCmaxで7%低下、
AUCで27%上昇することが示されたことから、P-gp及びBCRP
阻害剤併用時には特段用量調節は必要ない旨に修正され
た(これまではCmax25%、AUCが55%上昇することから併用
時にはモニタリングが必要と記載されていた)。
その他
注目
7/48
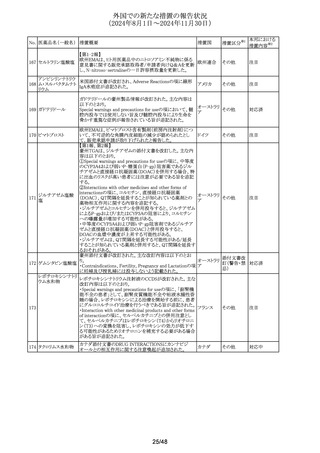
(2024年8月1日~2024年11月30日)
No. 医薬品名(一般名) 措置概要
38 フェノフィブラート
措置国
フェノフィブラートの米国添付文書が改訂された。主な内容
は以下のとおり。
Contraindicationsの項
①「透析を受けている患者を含む重度の腎障害」から「末期
腎疾患(ESRD)および透析を受けている患者を含む重度の
腎障害」に変更する。
②「フェノフィブリン酸またはフェノフィブラートに対する過敏
症」から「フェノフィブリン酸、フェノフィブラートあるいは本剤
の賦形剤に対する過敏症。フェノフィブラートでアナフィラキ
シーおよび血管浮腫を含む重篤な過敏反応が報告されて
いる。」に変更する。
Warnings and Precautionsの項
③死亡率および冠動脈性心疾患の罹患率の項に、2型糖
尿病患者を対象とした2件の大規模ランダム化比較試験に
おいて、フェノフィブラートは心血管疾患の罹病率および死
亡率を低下させなかったこと、バックグラウンドでスタチン療
法を受けている2型糖尿病患者を対象とした大規模無作為
化プラセボ対照試験において、ペマフィブラートは心血管疾
患の罹病率および死亡率を低下させなかった旨を追記す
る。
④静脈塞栓性疾患の項に、ペマフィブラートを用いた心血
管系アウトカム試験における肺塞栓症、深部静脈血栓症の
発現率を追記する。
⑤ミオパチーと横紋筋融解症の項のミオパチーのリスク因
子、ミオパチーと横紋筋融解症のリスクを予防または軽減す
アメリカ
るための手順を更新する。
⑥血清クレアチニンの増加の項に、本剤は末期腎疾患
(ESRD)および透析を受けている患者を含む重度の腎障害
患者には禁忌である旨を追記する。
⑦胆石症の項に、胆嚢疾患の既往がある患者には禁忌で
ある旨を追記する。
⑧過敏症反応の項に、本剤はフェノフィブラート、フェノフィ
ブリン酸あるいは本剤の成分に対して過敏症のある患者に
は禁忌である旨を追記する。
Adverse Reactionsの項
⑨ミオパチーと横紋筋融解症、血清クレアチニンの上昇、胆
石症、クマリン系抗凝固薬による出血リスクの上昇、血液学
的変化を追記する。
⑩Clinical Trail Experienceの項に、高トリグリセリド血症また
は原発性高脂血症の成人患者を対象に、他のフェノフィブ
ラート製剤の十分かつ適切にコントロールされた試験に基
づいて、本剤の安全性が確立されている旨を追記する。
⑪Clinical Trail Experienceの項の蕁麻疹、肝酵素の増加に
関する記載を更新する。
⑫Postmarketing Experienceの項に、アナフィラキシー、血
管浮腫を追記する。
Use in Specific Populationsの項
⑬小児、高齢者、腎障害、肝障害の項に関する記載を更新
する。
⑭Pregnancy、Lactationの項をPLLRに従い更新する。
措置区分※1
本邦における
措置内容※2
添付文書改
訂(警告・禁 注目
忌)
エプタコグ アル
チェコにおいて、特定の製造ラインで製造された一部の製
39 ファ(活性型)(遺伝 品における薬剤充填量の不足が生じたため、1mg及び2mg チェコ
子組換え)
製剤の回収が行われた。
回収
対応不要
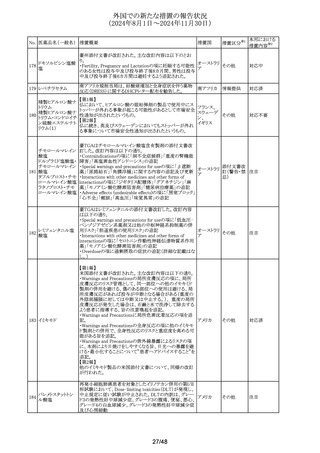
【第1,2報】
欧州添付文書が改訂された。改訂内容は以下のとおり。
・Warnings and Precautions for Useの項について、血中濃
度が高い場合にQT延長があらわれるおそれがある旨を追
記し、中等度以上の肝機能障害患者では投与しないことが
望ましいこと、重度の腎機能障害患者でも投与しないことが
望ましいが、投与する必要がある場合には心電図等をモニ
ベロトラルスタット塩 タリングするよう追記された。
40
アメリカ
酸塩
・Interaction with other medicinal products and other forms
of interactionのP-gpとBCRP阻害剤の項について、 市販後
に得られたデータではP-gp及びBCRP阻害剤であるシクロス
ポリンを併用した際に、血中本薬濃度がCmaxで7%低下、
AUCで27%上昇することが示されたことから、P-gp及びBCRP
阻害剤併用時には特段用量調節は必要ない旨に修正され
た(これまではCmax25%、AUCが55%上昇することから併用
時にはモニタリングが必要と記載されていた)。
その他
注目
7/48