よむ、つかう、まなぶ。
資料2-3 外国での新たな措置の報告状況[1.4MB] (33 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
③Interaction with other drugs and other forms of
interactionの項に以下が追加された。
エストロゲンおよび/またはエストロゲンを含む複合ホルモン
避妊薬と併用すると、血栓形成の可能性が高まる理論的な
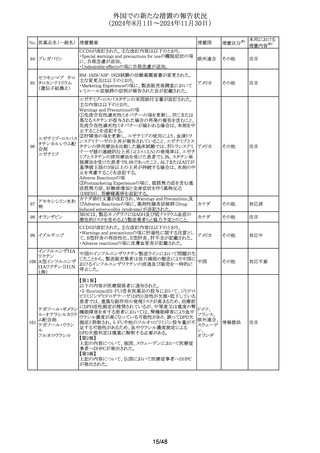
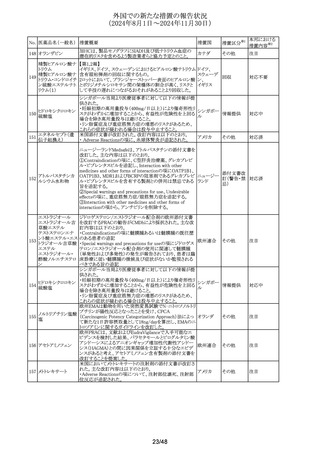
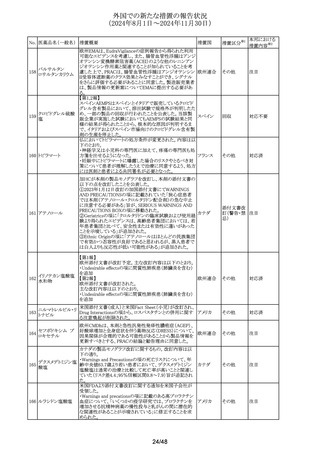
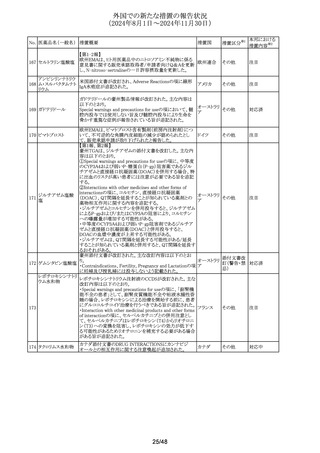
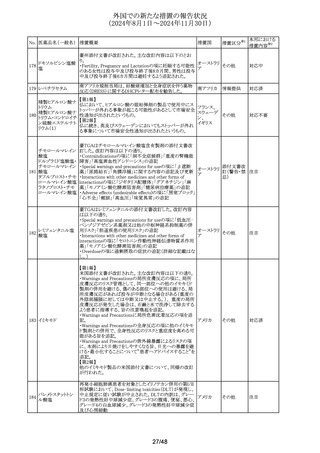
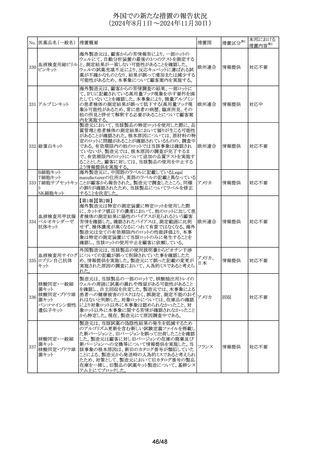
外国での新たな措置の報告状況
リスクがある。一方、本剤の抗線溶作用は血栓溶解薬によっ
(2024年8月1日~2024年11月30日)
て拮抗される可能性がある。
ブラジル、
225 トラネキサム酸
④Fertility, pregnancy, and breastfeeding の項に以下が追
その他
対応済
南アフリカ
加された。
本邦における
No. 医薬品名(一般名) 妊娠
措置概要
措置国
措置区分※1
措置内容※2
妊娠第2期および第3期ならびに分娩時の妊婦におけるトラ
ネキサム酸の使用に関する公表された研究、症例シリーズ
および症例報告から入手可能なデータでは、本薬剤に関連
する流産または母体もしくは胎児の有害転帰のリスクがある
かどうかは明らかにされていない。妊娠中または妊娠第1期
の母体へのトラネキサム酸投与後に、新生児の死亡につな
がる胎児構造異常の症例がある。しかし、他の交絡因子の
ため、妊娠中のトラネキサム酸使用による重大な先天性異
常のリスクは明確に確立されていない。
母乳育児
母乳中にトラネキサム酸が存在することが文献で報告されて
いる。授乳中の児に対するトラネキサム酸の影響または乳汁
分泌への影響に関するデータは限られている。
生殖能
トラネキサム酸の生殖能力への影響に関する臨床データは
ない。動物実験では、トラネキサム酸は臨床的に適切な用
量で雄または雌の生殖能力に影響を与えなかった。
(第2報)
世界保健機関(WHO)のニュースレターにて、南アフリカ規
制当局(SAHPRA)は、トラネキサム酸注射剤の髄腔内への
投与過誤のリスクを最小化することを目的とし、トラネキサム
酸注射剤の製品ラベルについて、「HIGH ALERT」及び
「For IV Use Only」と記載する改訂を行ったことが公表され
た。
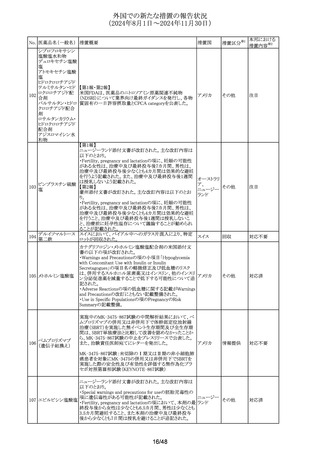
226 アムホテリシンB
ドイツ、ノルウェー及びハンガリーにおいて、容器の閉鎖の
問題により特定ロットの回収を実施する。
アメリカ
欧州PRACは以下についてアミトリプチリンとの因果関係が
否定できないため、アミトリプチリン/ペルフェナジンの製品
情報を改訂する必要があると勧告し、CMDhが合意した。
アミトリプチリン塩酸 ・Special warnings and precautions for useにDRESSを含む
227
欧州連合
塩
重篤な皮膚反応を追記
・Interaction with other medicinal products and other forms
of interactionにセントジョーンズワートとの相互作用
・Undesirable effectsにDRESSを追記
回収
対応不要
その他
注目
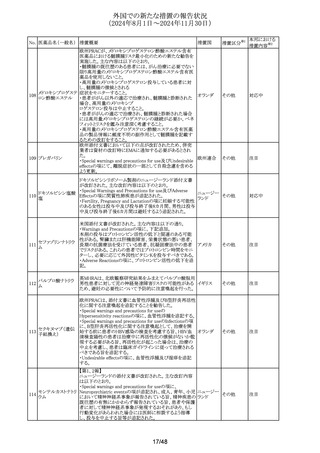
シンガポール HSAは、許容限度値を超えるN-nitrosoアミトリプチリン塩酸 nortriptyline(NNORT)が検出されたため、Pharmaforte
シンガポー
228
回収
塩
Singapore Pte社のアミトリプチリン10mg錠、25mg錠の特定 ル
ロットがリコールされたことを公表した。
米国でプラチナ製剤を含む化学療法及びPD-1又はPD-L1
阻害剤による治療歴を有する局所進行性又は転移性尿路
サシツズマブ ゴビ
上皮がんに対して迅速承認を取得したが、承認条件の検証
229 テカン(遺伝子組換
アメリカ
その他
的第3相試験IMMU132-13(TROPiCS-04試験)において、
え)
主要評価項目である全生存期間が達成されなかったことか
ら、迅速承認を取り下げる予定
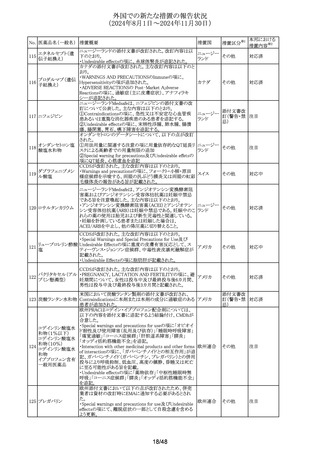
英MHRAは、医療従事者向けのレターを発出した。
・北欧観察研究結果をふまえてバルプロ酸服用男性患者に
バルプロ酸ナトリウ 対して児の神経発達障害リスクの可能性があるため、避妊
230
イギリス
情報提供
ム
の必要性について製品情報が改訂されている
・患者及び医療従事者向け資材については2024年秋を目
途に改訂される
231 炭酸リチウム
豪州TGAにおいて、製品情報に以下の内容が追記された。
・Special warnings and precautions for useの項に、減量手
術を受けた患者では維持量を減らす必要性について追記。
オーストラリ
・Interactions with other medicines and other forms of
その他
ア
interactionsの項に、トピラマート追記。
・Adverse effectsの項に、副甲状腺腺腫、副甲状腺肥大を
追記。
豪州TGAにおいて、製品情報に以下の内容が追記された。
・Special warnings and precautions for useの項に、ガラク
フェノバルビタール トース吸収不良、慢性疼痛、若年患者、既存の肝臓疾患、
オーストラリ
232 フェノバルビタール 薬物乱用又はアルコール依存症の病歴のある患者への注
その他
ア
ナトリウム
意。
・Adverse effectsの項に、逆説的反応(異常な興奮)、幻覚、
落ち着きのなさ、高齢者の混乱、無気力が追記。
33/48
対応不要
対応不要
注目
注目
対応済
interactionの項に以下が追加された。
エストロゲンおよび/またはエストロゲンを含む複合ホルモン
避妊薬と併用すると、血栓形成の可能性が高まる理論的な
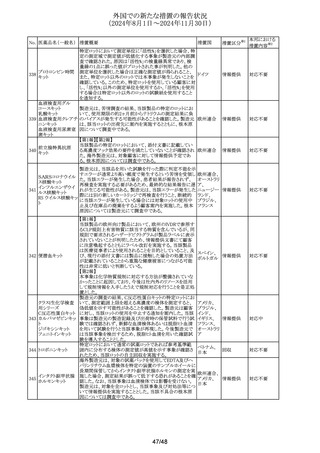
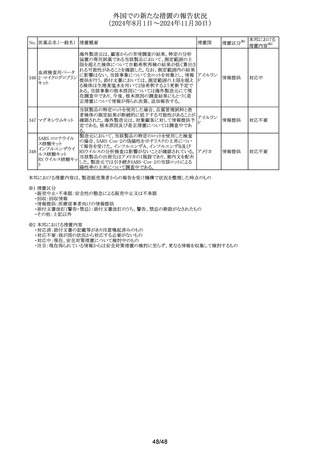
外国での新たな措置の報告状況
リスクがある。一方、本剤の抗線溶作用は血栓溶解薬によっ
(2024年8月1日~2024年11月30日)
て拮抗される可能性がある。
ブラジル、
225 トラネキサム酸
④Fertility, pregnancy, and breastfeeding の項に以下が追
その他
対応済
南アフリカ
加された。
本邦における
No. 医薬品名(一般名) 妊娠
措置概要
措置国
措置区分※1
措置内容※2
妊娠第2期および第3期ならびに分娩時の妊婦におけるトラ
ネキサム酸の使用に関する公表された研究、症例シリーズ
および症例報告から入手可能なデータでは、本薬剤に関連
する流産または母体もしくは胎児の有害転帰のリスクがある
かどうかは明らかにされていない。妊娠中または妊娠第1期
の母体へのトラネキサム酸投与後に、新生児の死亡につな
がる胎児構造異常の症例がある。しかし、他の交絡因子の
ため、妊娠中のトラネキサム酸使用による重大な先天性異
常のリスクは明確に確立されていない。
母乳育児
母乳中にトラネキサム酸が存在することが文献で報告されて
いる。授乳中の児に対するトラネキサム酸の影響または乳汁
分泌への影響に関するデータは限られている。
生殖能
トラネキサム酸の生殖能力への影響に関する臨床データは
ない。動物実験では、トラネキサム酸は臨床的に適切な用
量で雄または雌の生殖能力に影響を与えなかった。
(第2報)
世界保健機関(WHO)のニュースレターにて、南アフリカ規
制当局(SAHPRA)は、トラネキサム酸注射剤の髄腔内への
投与過誤のリスクを最小化することを目的とし、トラネキサム
酸注射剤の製品ラベルについて、「HIGH ALERT」及び
「For IV Use Only」と記載する改訂を行ったことが公表され
た。
226 アムホテリシンB
ドイツ、ノルウェー及びハンガリーにおいて、容器の閉鎖の
問題により特定ロットの回収を実施する。
アメリカ
欧州PRACは以下についてアミトリプチリンとの因果関係が
否定できないため、アミトリプチリン/ペルフェナジンの製品
情報を改訂する必要があると勧告し、CMDhが合意した。
アミトリプチリン塩酸 ・Special warnings and precautions for useにDRESSを含む
227
欧州連合
塩
重篤な皮膚反応を追記
・Interaction with other medicinal products and other forms
of interactionにセントジョーンズワートとの相互作用
・Undesirable effectsにDRESSを追記
回収
対応不要
その他
注目
シンガポール HSAは、許容限度値を超えるN-nitrosoアミトリプチリン塩酸 nortriptyline(NNORT)が検出されたため、Pharmaforte
シンガポー
228
回収
塩
Singapore Pte社のアミトリプチリン10mg錠、25mg錠の特定 ル
ロットがリコールされたことを公表した。
米国でプラチナ製剤を含む化学療法及びPD-1又はPD-L1
阻害剤による治療歴を有する局所進行性又は転移性尿路
サシツズマブ ゴビ
上皮がんに対して迅速承認を取得したが、承認条件の検証
229 テカン(遺伝子組換
アメリカ
その他
的第3相試験IMMU132-13(TROPiCS-04試験)において、
え)
主要評価項目である全生存期間が達成されなかったことか
ら、迅速承認を取り下げる予定
英MHRAは、医療従事者向けのレターを発出した。
・北欧観察研究結果をふまえてバルプロ酸服用男性患者に
バルプロ酸ナトリウ 対して児の神経発達障害リスクの可能性があるため、避妊
230
イギリス
情報提供
ム
の必要性について製品情報が改訂されている
・患者及び医療従事者向け資材については2024年秋を目
途に改訂される
231 炭酸リチウム
豪州TGAにおいて、製品情報に以下の内容が追記された。
・Special warnings and precautions for useの項に、減量手
術を受けた患者では維持量を減らす必要性について追記。
オーストラリ
・Interactions with other medicines and other forms of
その他
ア
interactionsの項に、トピラマート追記。
・Adverse effectsの項に、副甲状腺腺腫、副甲状腺肥大を
追記。
豪州TGAにおいて、製品情報に以下の内容が追記された。
・Special warnings and precautions for useの項に、ガラク
フェノバルビタール トース吸収不良、慢性疼痛、若年患者、既存の肝臓疾患、
オーストラリ
232 フェノバルビタール 薬物乱用又はアルコール依存症の病歴のある患者への注
その他
ア
ナトリウム
意。
・Adverse effectsの項に、逆説的反応(異常な興奮)、幻覚、
落ち着きのなさ、高齢者の混乱、無気力が追記。
33/48
対応不要
対応不要
注目
注目
対応済