よむ、つかう、まなぶ。
資料2-3 外国での新たな措置の報告状況[1.4MB] (36 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
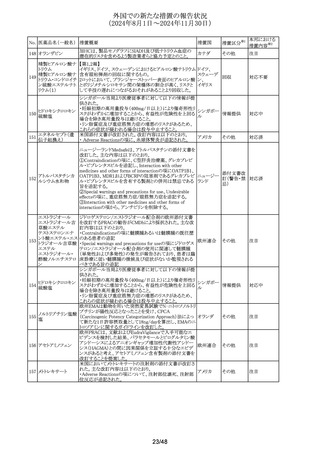
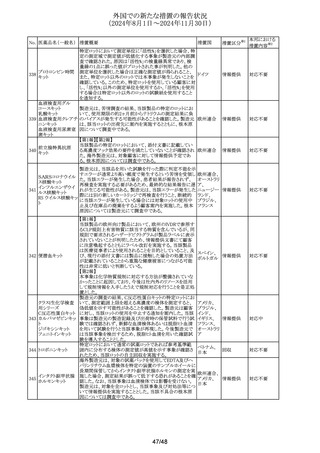
外国での新たな措置の報告状況
(2024年8月1日~2024年11月30日)
No. 医薬品名(一般名) 措置概要
措置国
措置区分※1
豪州添付文書が改訂された。主な改訂内容は以下のとお
り。
・Fertility, pregnancy and lactationの項に妊娠の可能性が
オーストラリ
249 ドセタキセル水和物 ある女性は、治療中及び治療後少なくとも2カ月間は効果的
その他
ア
な避妊を行う必要があり、妊娠の可能性がある女性をパート
ナーに持つ男性患者は、治療中及び治療後少なくとも4カ
月間は効果的な避妊を行う必要がある旨が記載された。
米国FDAが以下のヘパリンナトリウム製品の添付文書の改
訂が行われたことを公表した。
①ヘパリンナトリウム注射液
添付文書のWarnings and Precautionsの項に「高カリウム血
症」が新設され、「ヘパリンは、特に糖尿病、慢性腎不全、既
存の代謝性アシドーシス、血中カリウム高値、またはカリウム
保持薬を服用している患者において、副腎からのアルドステ
ロン分泌を抑制し、高カリウム血症を引き起こす可能性があ
る。高カリウム血症のリスクは治療期間とともに増加するが、
250 ヘパリンナトリウム 通常はヘパリンを中止すると元に戻る」、
アメリカ
その他
「高カリウム血症のリスクがある患者ではヘパリン療法を開始
する前に、ヘパリン療法を受けているすべての患者では、ヘ
パリンを5 日以上投与している、または医師が適切と判断し
た日のいずれか早い時期から血中カリウム濃度の測定を開
始し、定期的測定を行うこと」が追加された。
②ヘパリンナトリウム注射液、ヘパリンロック、ヘパリンフラッ
シュ製剤
Adverse ReactionsのPostmarketing Experienceの項の代謝
栄養障害の項に高カリウム血症が追加された。
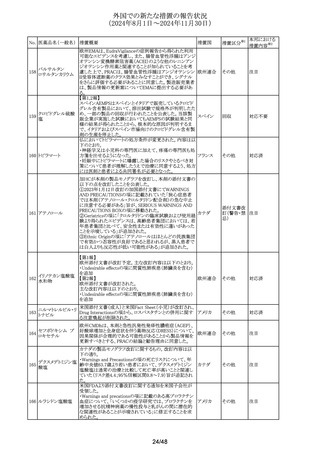
豪州添付文書が改訂され、Special warnings and
オーストラリ
251 メトロニダゾール
precautions for useの項に重症皮膚副作用(SCARs)追記さ
その他
ア
れた。
CCDSが改訂された。主な改訂内容は以下のとおり。
アベルマブ(遺伝子
252
・警告、使用上の注意、 副作用の項に好中球減少症が追 ドイツ
その他
組換え)
記された。
欧州医薬品規制首脳会議(HMA)は、全身用及び吸入用キ
レボフロキサシン水
ノロン含有医薬品及びフルオロキノロン含有医薬品に関す
和物
るPSURのフォローアップの評価報告を掲載し、Undesirable
253 シプロフロキサシン
欧州連合 その他
effectsの項に既存の、機能障害や永続する可能性のある副
オフロキサシン
作用の情報に、不安、自殺念慮、パニック発作、神経痛、注
ノルフロキサシン
意力障害を追記するよう勧告した。
欧州CMDhは、PRACの検討結果に基づき、マクロゴール
3350配合剤のSmPCのSpecial warning for precautionsに「痙
254 マクロゴール
欧州連合 その他
攣発作」および「食道破裂(ブールハーフェ症候群)」に関
する注意喚起を追記するよう勧告している。
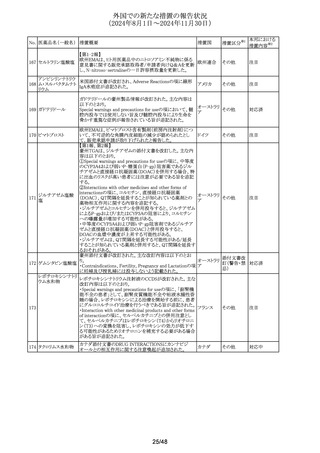
米国FDAがダルテパリンナトリウムの添付文書の
ダルテパリンナトリウ
255
Postmarketing Experienceの代謝・栄養障害の項に高カリウ アメリカ
その他
ム
ム血症を追加したことを公表した。
豪州TGAが、アモキシシリン三水和物/クラリスロマイシン
/エソメプラゾールマグネシウム三水和物の配合剤の製品
エソメプラゾールマ
オーストラリ
256
情報のUndesirable effetsにアモキシシリンの副作用として過
その他
グネシウム水和物
ア
敏症反応の項に対称性薬剤性間擦性および屈側部発疹
(SDRIFE)(バブーン症候群)を追加したことを公表した。
257 アザチオプリン
258 ファモチジン
欧州PRACにより、アロプリノールのSmPCの改訂が勧告さ
れ、Interaction with other medicinal products and other
forms of interactionにアロプリノールと6-メルカプトプリン又
はアザチオプリンとの併用により6-メルカプトプリン又はアザ
チオプリンの血中濃度が上昇し、生命を脅かす汎血球減少
欧州連合 その他
症や骨髄抑制がおこる可能性について注意喚起がなされ
た。また、これに伴い、Special warnings and precautions for
useに「死亡に至った症例があるため、アロプリノールとアザ
チオプリン/6-メルカプトプリンの併用は避けるべきである」
旨が追加された。
豪州の製品情報について、「相互作用」の項に「ポサコナ
オーストラリ
ゾール」「チロシンキナーゼ阻害剤」が、「副作用」の項に「不
その他
ア
整脈」「QT延長」がそれぞれ追加された。
36/48
本邦における
措置内容※2
対応済
注目
注目
注目
対応済
注目
注目
対応不要
対応済
注目
(2024年8月1日~2024年11月30日)
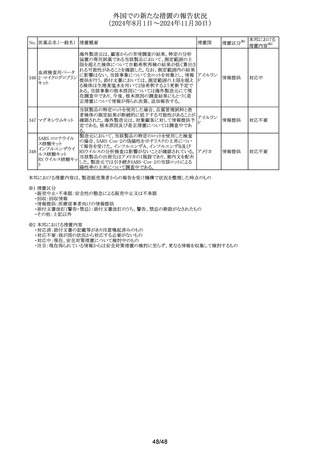
No. 医薬品名(一般名) 措置概要
措置国
措置区分※1
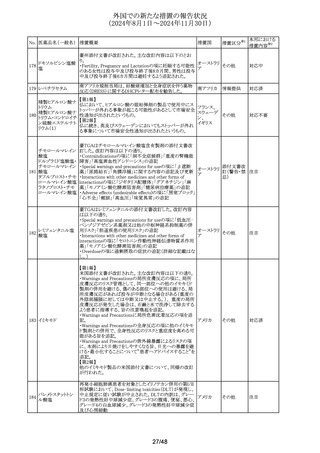
豪州添付文書が改訂された。主な改訂内容は以下のとお
り。
・Fertility, pregnancy and lactationの項に妊娠の可能性が
オーストラリ
249 ドセタキセル水和物 ある女性は、治療中及び治療後少なくとも2カ月間は効果的
その他
ア
な避妊を行う必要があり、妊娠の可能性がある女性をパート
ナーに持つ男性患者は、治療中及び治療後少なくとも4カ
月間は効果的な避妊を行う必要がある旨が記載された。
米国FDAが以下のヘパリンナトリウム製品の添付文書の改
訂が行われたことを公表した。
①ヘパリンナトリウム注射液
添付文書のWarnings and Precautionsの項に「高カリウム血
症」が新設され、「ヘパリンは、特に糖尿病、慢性腎不全、既
存の代謝性アシドーシス、血中カリウム高値、またはカリウム
保持薬を服用している患者において、副腎からのアルドステ
ロン分泌を抑制し、高カリウム血症を引き起こす可能性があ
る。高カリウム血症のリスクは治療期間とともに増加するが、
250 ヘパリンナトリウム 通常はヘパリンを中止すると元に戻る」、
アメリカ
その他
「高カリウム血症のリスクがある患者ではヘパリン療法を開始
する前に、ヘパリン療法を受けているすべての患者では、ヘ
パリンを5 日以上投与している、または医師が適切と判断し
た日のいずれか早い時期から血中カリウム濃度の測定を開
始し、定期的測定を行うこと」が追加された。
②ヘパリンナトリウム注射液、ヘパリンロック、ヘパリンフラッ
シュ製剤
Adverse ReactionsのPostmarketing Experienceの項の代謝
栄養障害の項に高カリウム血症が追加された。
豪州添付文書が改訂され、Special warnings and
オーストラリ
251 メトロニダゾール
precautions for useの項に重症皮膚副作用(SCARs)追記さ
その他
ア
れた。
CCDSが改訂された。主な改訂内容は以下のとおり。
アベルマブ(遺伝子
252
・警告、使用上の注意、 副作用の項に好中球減少症が追 ドイツ
その他
組換え)
記された。
欧州医薬品規制首脳会議(HMA)は、全身用及び吸入用キ
レボフロキサシン水
ノロン含有医薬品及びフルオロキノロン含有医薬品に関す
和物
るPSURのフォローアップの評価報告を掲載し、Undesirable
253 シプロフロキサシン
欧州連合 その他
effectsの項に既存の、機能障害や永続する可能性のある副
オフロキサシン
作用の情報に、不安、自殺念慮、パニック発作、神経痛、注
ノルフロキサシン
意力障害を追記するよう勧告した。
欧州CMDhは、PRACの検討結果に基づき、マクロゴール
3350配合剤のSmPCのSpecial warning for precautionsに「痙
254 マクロゴール
欧州連合 その他
攣発作」および「食道破裂(ブールハーフェ症候群)」に関
する注意喚起を追記するよう勧告している。
米国FDAがダルテパリンナトリウムの添付文書の
ダルテパリンナトリウ
255
Postmarketing Experienceの代謝・栄養障害の項に高カリウ アメリカ
その他
ム
ム血症を追加したことを公表した。
豪州TGAが、アモキシシリン三水和物/クラリスロマイシン
/エソメプラゾールマグネシウム三水和物の配合剤の製品
エソメプラゾールマ
オーストラリ
256
情報のUndesirable effetsにアモキシシリンの副作用として過
その他
グネシウム水和物
ア
敏症反応の項に対称性薬剤性間擦性および屈側部発疹
(SDRIFE)(バブーン症候群)を追加したことを公表した。
257 アザチオプリン
258 ファモチジン
欧州PRACにより、アロプリノールのSmPCの改訂が勧告さ
れ、Interaction with other medicinal products and other
forms of interactionにアロプリノールと6-メルカプトプリン又
はアザチオプリンとの併用により6-メルカプトプリン又はアザ
チオプリンの血中濃度が上昇し、生命を脅かす汎血球減少
欧州連合 その他
症や骨髄抑制がおこる可能性について注意喚起がなされ
た。また、これに伴い、Special warnings and precautions for
useに「死亡に至った症例があるため、アロプリノールとアザ
チオプリン/6-メルカプトプリンの併用は避けるべきである」
旨が追加された。
豪州の製品情報について、「相互作用」の項に「ポサコナ
オーストラリ
ゾール」「チロシンキナーゼ阻害剤」が、「副作用」の項に「不
その他
ア
整脈」「QT延長」がそれぞれ追加された。
36/48
本邦における
措置内容※2
対応済
注目
注目
注目
対応済
注目
注目
対応不要
対応済
注目