よむ、つかう、まなぶ。
資料2-3 外国での新たな措置の報告状況[1.4MB] (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
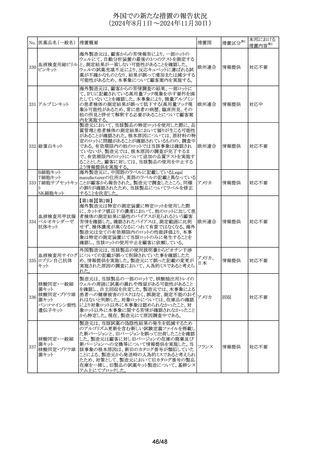
外国での新たな措置の報告状況
(2024年8月1日~2024年11月30日)
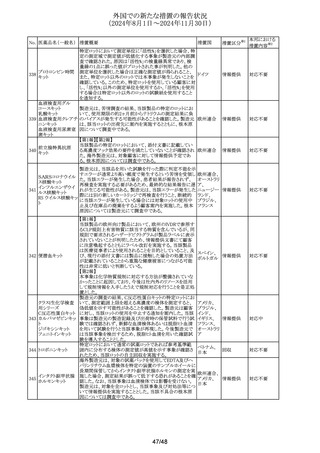
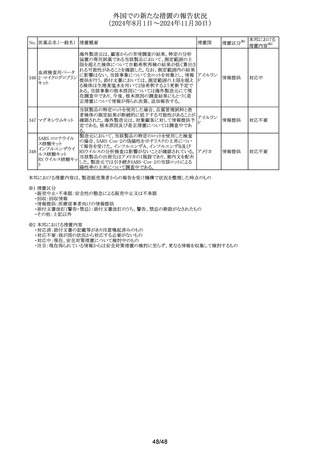
No. 医薬品名(一般名) 措置概要
24 ナロキソン塩酸塩
措置国
【第1報】
欧州PRACはナロキソン含有製剤(ナロキソン/ブプレノル
フィン)について、ガバペンチノイド(ガバペンチン及びプレ
ガバリン)との相互作用、齲歯の発現、小児の中毒及び死に
至る可能性との間に合理的な関連があるとして、添付文書
及びリーフレットの改訂をすべきであると結論付け、SmPCに
以下の点を追記したというもの。
・Interaction with other medicinal products and other forms
of interactionの項に「本剤とガバペンチノイド(ガバペンチン
及びプレガバリン)を併用すると、呼吸抑制、低血圧、重度 ドイツ、
の鎮静、昏睡又は死亡につながる可能性がある」を追記
欧州連合
・Undesirable effectsの項に「思考異常、薬物依存、多幸気
分、敵意、頭痛、片頭痛、浮動性めまい、筋緊張亢進、錯感
覚、傾眠、健忘、運動過多、痙攣発作、会話障害、振戦、肝
性脳症、失神、弱視、涙器障害、結膜炎、縮瞳、齲歯」を追
記
【第2報】
独BfArMは、欧州PRACの見解を受け、ナロキソン含有製剤
(ナロキソン/ブプレノルフィン)のSmPC及びパッケージリー
フレットを改訂するよう要請した。
措置区分※1
本邦における
措置内容※2
その他
注目
【第1報】
欧州CMDhは、製品情報に長期潜伏性アナフィラキシー反
応について以下のとおり追記すべきとするPRACの勧告に
合意した。
・アナフィラキシー反応はグラチラマー酢酸塩の投与直後、
治療開始数ヵ月後~数年後に発現する可能性がある。致死
的転帰に至った症例が報告されている。
【第2報】
CCSIが改訂され、以下の内容が追記された。
・Special warnings and precautions for use、Undesirable
effectsの項に、アナフィラキシー反応はグラチラマー酢酸塩
の投与直後、治療開始数ヵ月後~数年後に発現する可能
ドイツ、
性がある。致死的転帰に至った症例が報告されている旨を
フランス、
追記。
ニュージー
【第3報】
ランド、
ドイツBfArM及びフランスANSMより、医療専門家向けにグラ
25 グラチラマー酢酸塩
オランダ、 その他
チラマー酢酸塩のアナフィラキシー反応が治療開始後数ヵ
イスラエ
月後~数年後に発生する可能性がある旨注意喚起するた
ル、
めにレターがそれぞれ発出された。
スイス、
【第4報】
イギリス
ニュージーランドMedsafeは、欧州での対応を受けて、グラ
チラマー酢酸塩のアナフィラキシー反応が治療開始後数ヵ
月後~数年後に発生する可能性がある旨、レターを発出し
た。
【第5報】
スイスSwissmedicは、グラチラマー酢酸塩のアナフィラキ
シー反応が治療開始後数ヵ月後~数年後に発生する可能
性がある旨、レターを発出した。
【第6報】
英MHRAは、グラチラマー酢酸塩のアナフィラキシー反応が
治療開始後数ヵ月後~数年後に発生する可能性がある旨、
レターを発出した。
【第1報】
加国Health Canadaは、ジゴキシン0.0625mg錠を製造する1
社の特定の1ロットについて、錠剤の大きさが大きい可能性
があり、過量投与の恐れがあるため、該当の1ロットを回収す
ることを通知した。
26 ジゴキシン
カナダ
回収
【第2報】
加国Health Canadaは、ジゴキシンン0.0625mg錠および
0.125mg錠を製造する1社の特定のロットについて、通常サ
イズに見えても(規格よりも)過量もしくは過少量の錠剤が存
在する可能性があるため、回収することを通知した。
4/48
対応済
対応不要
(2024年8月1日~2024年11月30日)
No. 医薬品名(一般名) 措置概要
24 ナロキソン塩酸塩
措置国
【第1報】
欧州PRACはナロキソン含有製剤(ナロキソン/ブプレノル
フィン)について、ガバペンチノイド(ガバペンチン及びプレ
ガバリン)との相互作用、齲歯の発現、小児の中毒及び死に
至る可能性との間に合理的な関連があるとして、添付文書
及びリーフレットの改訂をすべきであると結論付け、SmPCに
以下の点を追記したというもの。
・Interaction with other medicinal products and other forms
of interactionの項に「本剤とガバペンチノイド(ガバペンチン
及びプレガバリン)を併用すると、呼吸抑制、低血圧、重度 ドイツ、
の鎮静、昏睡又は死亡につながる可能性がある」を追記
欧州連合
・Undesirable effectsの項に「思考異常、薬物依存、多幸気
分、敵意、頭痛、片頭痛、浮動性めまい、筋緊張亢進、錯感
覚、傾眠、健忘、運動過多、痙攣発作、会話障害、振戦、肝
性脳症、失神、弱視、涙器障害、結膜炎、縮瞳、齲歯」を追
記
【第2報】
独BfArMは、欧州PRACの見解を受け、ナロキソン含有製剤
(ナロキソン/ブプレノルフィン)のSmPC及びパッケージリー
フレットを改訂するよう要請した。
措置区分※1
本邦における
措置内容※2
その他
注目
【第1報】
欧州CMDhは、製品情報に長期潜伏性アナフィラキシー反
応について以下のとおり追記すべきとするPRACの勧告に
合意した。
・アナフィラキシー反応はグラチラマー酢酸塩の投与直後、
治療開始数ヵ月後~数年後に発現する可能性がある。致死
的転帰に至った症例が報告されている。
【第2報】
CCSIが改訂され、以下の内容が追記された。
・Special warnings and precautions for use、Undesirable
effectsの項に、アナフィラキシー反応はグラチラマー酢酸塩
の投与直後、治療開始数ヵ月後~数年後に発現する可能
ドイツ、
性がある。致死的転帰に至った症例が報告されている旨を
フランス、
追記。
ニュージー
【第3報】
ランド、
ドイツBfArM及びフランスANSMより、医療専門家向けにグラ
25 グラチラマー酢酸塩
オランダ、 その他
チラマー酢酸塩のアナフィラキシー反応が治療開始後数ヵ
イスラエ
月後~数年後に発生する可能性がある旨注意喚起するた
ル、
めにレターがそれぞれ発出された。
スイス、
【第4報】
イギリス
ニュージーランドMedsafeは、欧州での対応を受けて、グラ
チラマー酢酸塩のアナフィラキシー反応が治療開始後数ヵ
月後~数年後に発生する可能性がある旨、レターを発出し
た。
【第5報】
スイスSwissmedicは、グラチラマー酢酸塩のアナフィラキ
シー反応が治療開始後数ヵ月後~数年後に発生する可能
性がある旨、レターを発出した。
【第6報】
英MHRAは、グラチラマー酢酸塩のアナフィラキシー反応が
治療開始後数ヵ月後~数年後に発生する可能性がある旨、
レターを発出した。
【第1報】
加国Health Canadaは、ジゴキシン0.0625mg錠を製造する1
社の特定の1ロットについて、錠剤の大きさが大きい可能性
があり、過量投与の恐れがあるため、該当の1ロットを回収す
ることを通知した。
26 ジゴキシン
カナダ
回収
【第2報】
加国Health Canadaは、ジゴキシンン0.0625mg錠および
0.125mg錠を製造する1社の特定のロットについて、通常サ
イズに見えても(規格よりも)過量もしくは過少量の錠剤が存
在する可能性があるため、回収することを通知した。
4/48
対応済
対応不要