よむ、つかう、まなぶ。
資料2-3 外国での新たな措置の報告状況[1.4MB] (46 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
外国での新たな措置の報告状況
(2024年8月1日~2024年11月30日)
措置区分※1
本邦における
措置内容※2
情報提供
対応不要
情報提供
対応中
情報提供
対応不要
情報提供
対応不要
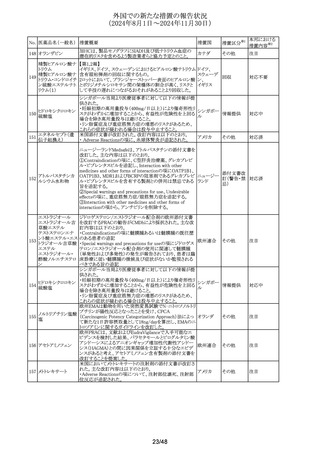
【第1報】【第2報】
海外製造元は特定の測定装置に特定ロットを使用した際
に、カットオフ値以下の濃度において、他のロットに比して患
血液検査用甲状腺 者検体の測定結果に陽性のバイアスが見られるという顧客
334 ペルオキシダーゼ 苦情を確認した。確認されたバイアスは、測定範囲に比例 欧州連合
抗体キット
せず、検体濃度が高くなるにつれて有意ではなくなる。海外
製造元は全ての有効期限内のロットの性能評価より、本事
象は特定の測定装置にて当該ロットのみに発生することを
確認し、当該ロットの使用中止を顧客に依頼している。
情報提供
対応不要
外国製造元は、当該製品の使用説明書からビオチン干渉
血液検査用サイログ についての記載が誤って削除されていた事を確認したた
アメリカ、
335 ロブリン自己抗体
め、情報提供を実施した。製造元にて誤った記載の変更が
日本
キット
実施された原因の調査において、人為的ミスであると考えら
れた。
情報提供
対応不要
製造元は、当該製品の一部のロットで、核酸抽出用トレイの
核酸同定・一般細 ウェルの周囲に試薬の漏れや残留がある可能性があること
菌キット
を確認し、自主回収を決定した。製造元では、本事象による
核酸同定・ブドウ球 患者への健康被害のリスクはなく、誤測定、測定不能のおそ
336
アメリカ
菌キット
れはないと判断した。対象ロットについては、在庫品の確認
バンコマイシン耐性 により対象ロット以外に本事象は認められなかったこと、対
遺伝子キット
象ロット以外に本事象に関する苦情が確認されなかったこと
から特定した。現在、製造元にて原因調査中である。
回収
対応不要
製造元は、当該試薬の偽陰性結果の発生を低減するため
のアルゴリズム更新を含む新しい試験定義ファイルを搭載し
た新バージョンと、旧バージョンを誤って出荷したことを確認
核酸同定・一般細 した。製造元は顧客に対し旧バージョンの在庫の廃棄及び
菌キット
新バージョンへの交換等について情報提供を実施した。当
337
フランス
核酸同定・ブドウ球 該事象の根本原因は、新旧のカタログ番号が類似していた
菌キット
ことによる、製造元から発送時の人為的ミスであると考えられ
たため、対策として、製造元において旧カタログ番号の製品
在庫を一掃し、旧製品の試薬キット製造について、基幹シス
テム上にてブロックした。
情報提供
対応不要
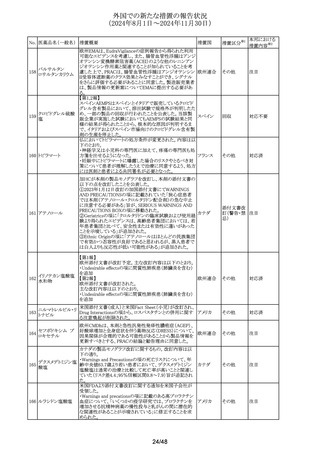
No. 医薬品名(一般名) 措置概要
措置国
海外製造元は、顧客からの苦情報告により、一部ロットの
ウェルにて、自動分析装置の最後の3つのテストを測定する
血液検査用総ビリル と、測定結果が一致しない可能性があることを確認した。
330
欧州連合
ビンキット
ウェルの試薬充填不足により、反応キュベットに運ばれる試
薬が不確かなものとなり、結果が誤って増加または減少する
可能性があるため、本事象について顧客案内を実施する。
海外製造元は、顧客からの苦情調査の結果、一部ロットに
て、IFUに記載されている高用量フック現象を示す要件を満
たしていないことを確認した。本事象により、微量アルブミン
331 アルブミンキット
の患者検体の測定結果が誤って低下する(高用量フック現 欧州連合
象))可能性があるため、常に患者の病歴、臨床所見、その
他の所見と併せて解釈する必要があることについて顧客案
内を実施する。
製造元において、当該製品の特定ロットを使用した際に、品
質管理と患者検体の測定結果において偏りが生じる可能性
があることが確認された。根本原因については、原材料の特
定のロットに問題があることが確認されているものの、調査中
332 総蛋白キット
である。有効期限内の他のロットでは当該事象は確認され 欧州連合
ていないが、製造元では、根本原因の調査が完了するま
で、有効期限内のロットについて追加の品質テストを実施す
ることとした。顧客に対しては、当該製品の使用を中止する
よう情報提供を実施する。
B細胞キット
海外製造元に、中国語のラベルに記載しているLegal
T細胞キット
manufacturerの住所が、英語のラベルの記載と異なっている
333 T細胞サブセットキッ ことが顧客から報告された。製造元で調査したところ、同様 アメリカ
ト
の誤りが確認されたため、当該製品についてラベルを修正
NK細胞キット
することを決定した。
46/48
(2024年8月1日~2024年11月30日)
措置区分※1
本邦における
措置内容※2
情報提供
対応不要
情報提供
対応中
情報提供
対応不要
情報提供
対応不要
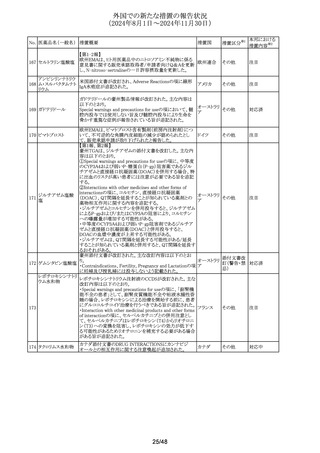
【第1報】【第2報】
海外製造元は特定の測定装置に特定ロットを使用した際
に、カットオフ値以下の濃度において、他のロットに比して患
血液検査用甲状腺 者検体の測定結果に陽性のバイアスが見られるという顧客
334 ペルオキシダーゼ 苦情を確認した。確認されたバイアスは、測定範囲に比例 欧州連合
抗体キット
せず、検体濃度が高くなるにつれて有意ではなくなる。海外
製造元は全ての有効期限内のロットの性能評価より、本事
象は特定の測定装置にて当該ロットのみに発生することを
確認し、当該ロットの使用中止を顧客に依頼している。
情報提供
対応不要
外国製造元は、当該製品の使用説明書からビオチン干渉
血液検査用サイログ についての記載が誤って削除されていた事を確認したた
アメリカ、
335 ロブリン自己抗体
め、情報提供を実施した。製造元にて誤った記載の変更が
日本
キット
実施された原因の調査において、人為的ミスであると考えら
れた。
情報提供
対応不要
製造元は、当該製品の一部のロットで、核酸抽出用トレイの
核酸同定・一般細 ウェルの周囲に試薬の漏れや残留がある可能性があること
菌キット
を確認し、自主回収を決定した。製造元では、本事象による
核酸同定・ブドウ球 患者への健康被害のリスクはなく、誤測定、測定不能のおそ
336
アメリカ
菌キット
れはないと判断した。対象ロットについては、在庫品の確認
バンコマイシン耐性 により対象ロット以外に本事象は認められなかったこと、対
遺伝子キット
象ロット以外に本事象に関する苦情が確認されなかったこと
から特定した。現在、製造元にて原因調査中である。
回収
対応不要
製造元は、当該試薬の偽陰性結果の発生を低減するため
のアルゴリズム更新を含む新しい試験定義ファイルを搭載し
た新バージョンと、旧バージョンを誤って出荷したことを確認
核酸同定・一般細 した。製造元は顧客に対し旧バージョンの在庫の廃棄及び
菌キット
新バージョンへの交換等について情報提供を実施した。当
337
フランス
核酸同定・ブドウ球 該事象の根本原因は、新旧のカタログ番号が類似していた
菌キット
ことによる、製造元から発送時の人為的ミスであると考えられ
たため、対策として、製造元において旧カタログ番号の製品
在庫を一掃し、旧製品の試薬キット製造について、基幹シス
テム上にてブロックした。
情報提供
対応不要
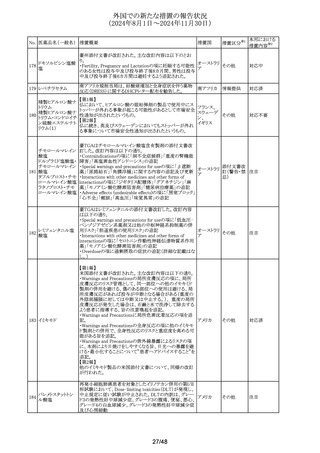
No. 医薬品名(一般名) 措置概要
措置国
海外製造元は、顧客からの苦情報告により、一部ロットの
ウェルにて、自動分析装置の最後の3つのテストを測定する
血液検査用総ビリル と、測定結果が一致しない可能性があることを確認した。
330
欧州連合
ビンキット
ウェルの試薬充填不足により、反応キュベットに運ばれる試
薬が不確かなものとなり、結果が誤って増加または減少する
可能性があるため、本事象について顧客案内を実施する。
海外製造元は、顧客からの苦情調査の結果、一部ロットに
て、IFUに記載されている高用量フック現象を示す要件を満
たしていないことを確認した。本事象により、微量アルブミン
331 アルブミンキット
の患者検体の測定結果が誤って低下する(高用量フック現 欧州連合
象))可能性があるため、常に患者の病歴、臨床所見、その
他の所見と併せて解釈する必要があることについて顧客案
内を実施する。
製造元において、当該製品の特定ロットを使用した際に、品
質管理と患者検体の測定結果において偏りが生じる可能性
があることが確認された。根本原因については、原材料の特
定のロットに問題があることが確認されているものの、調査中
332 総蛋白キット
である。有効期限内の他のロットでは当該事象は確認され 欧州連合
ていないが、製造元では、根本原因の調査が完了するま
で、有効期限内のロットについて追加の品質テストを実施す
ることとした。顧客に対しては、当該製品の使用を中止する
よう情報提供を実施する。
B細胞キット
海外製造元に、中国語のラベルに記載しているLegal
T細胞キット
manufacturerの住所が、英語のラベルの記載と異なっている
333 T細胞サブセットキッ ことが顧客から報告された。製造元で調査したところ、同様 アメリカ
ト
の誤りが確認されたため、当該製品についてラベルを修正
NK細胞キット
することを決定した。
46/48