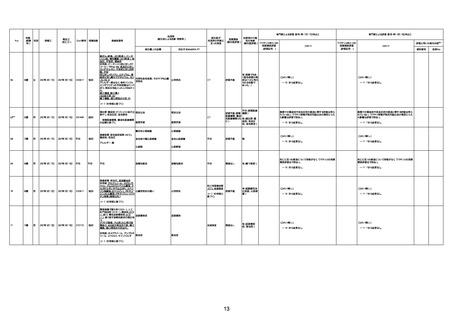
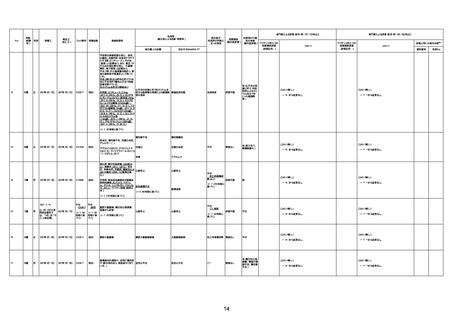
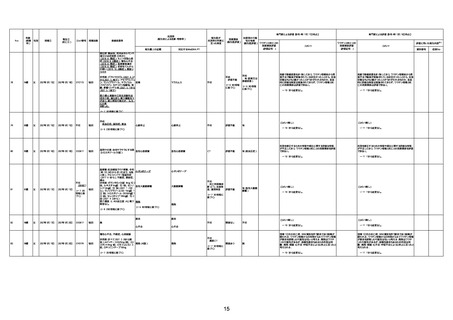
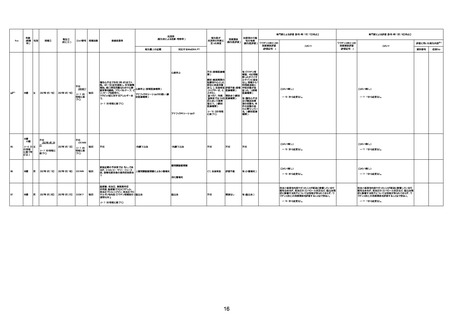
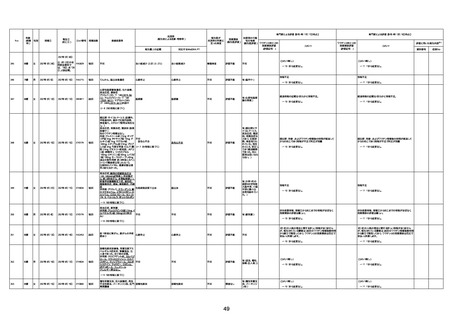
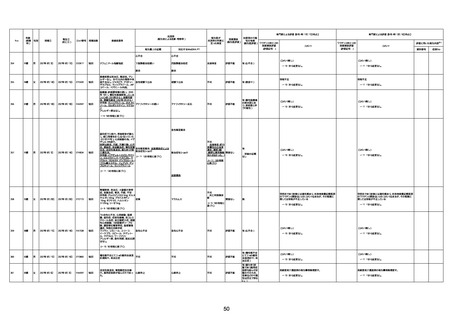
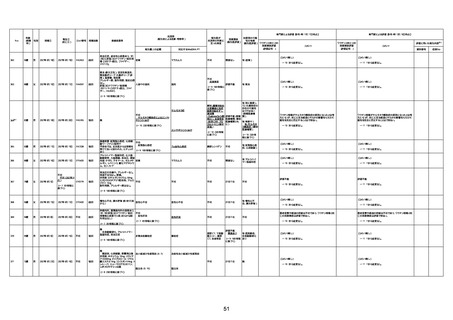
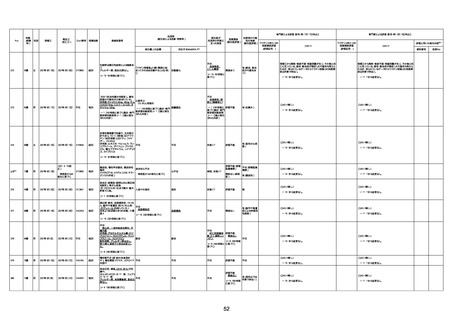
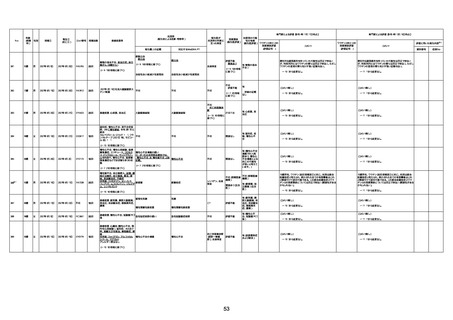
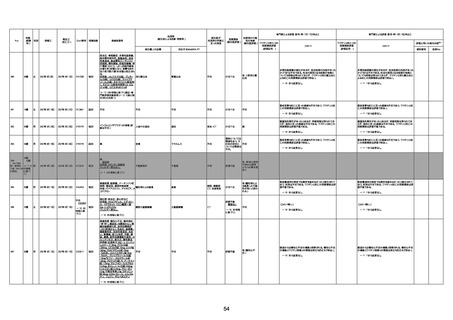
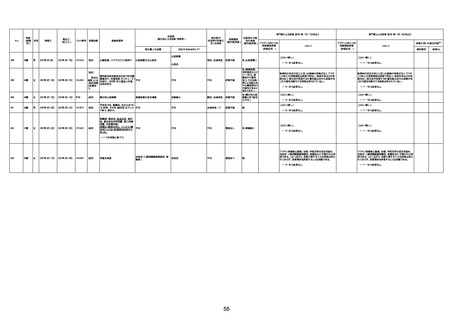
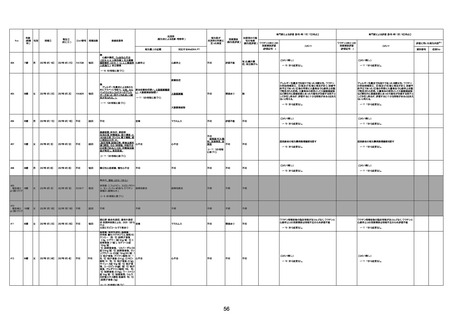
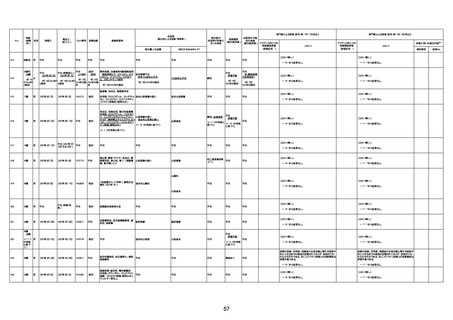
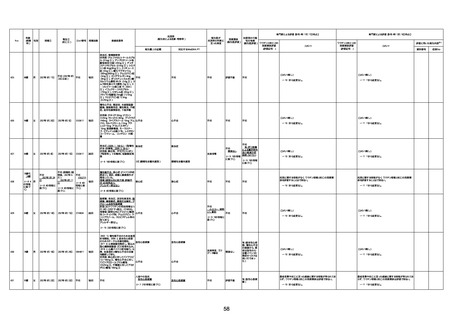
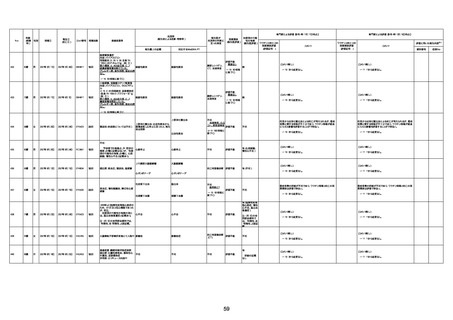
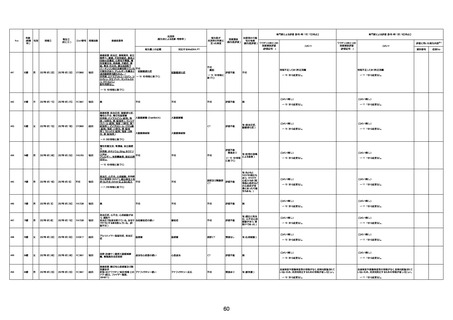
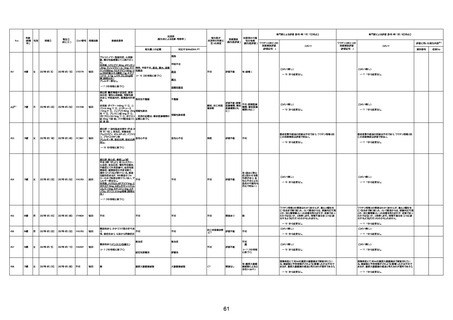
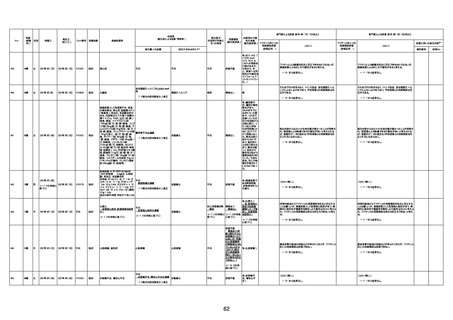
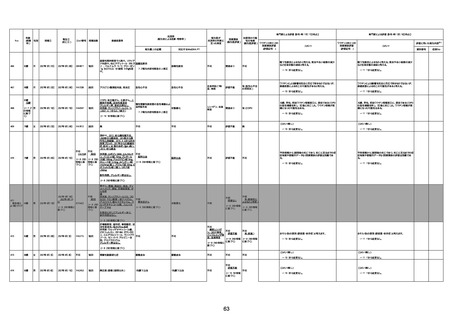
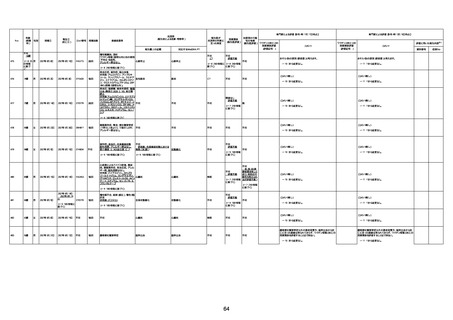
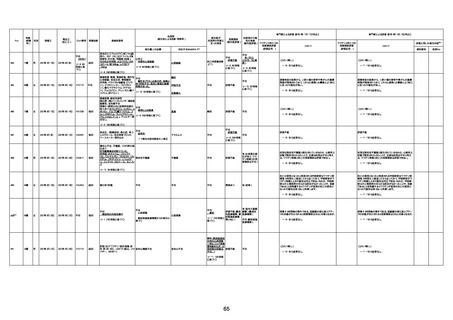
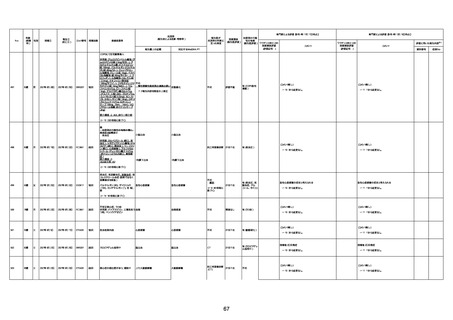
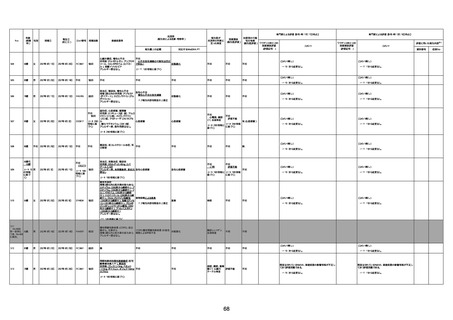
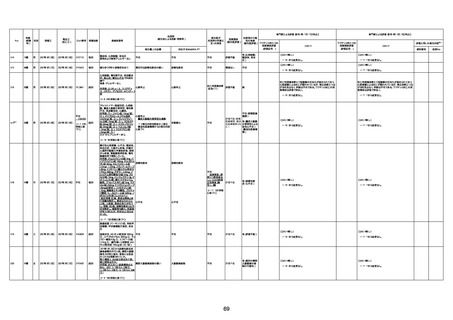
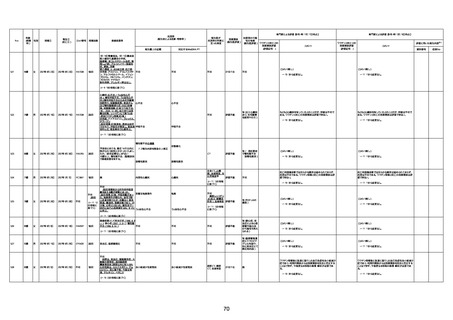
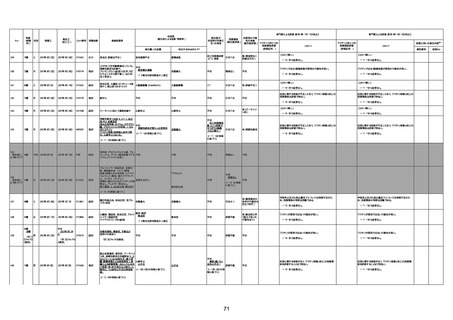
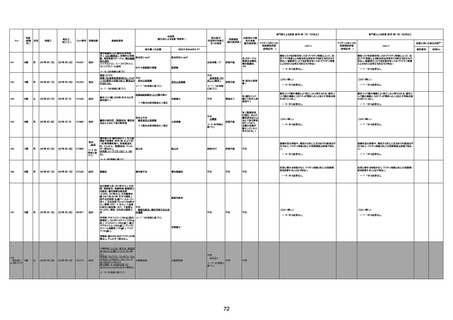
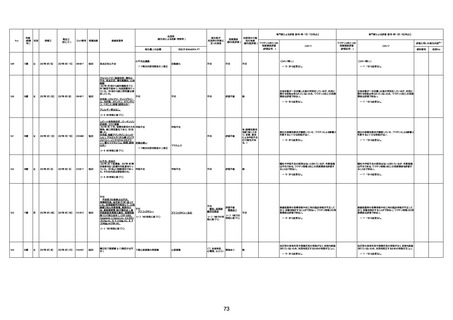
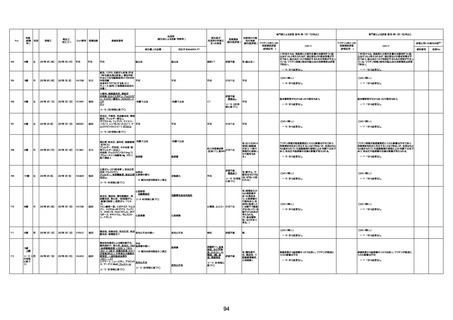
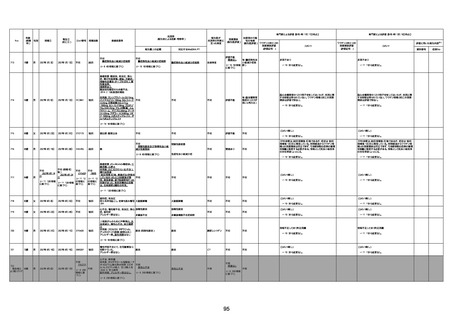
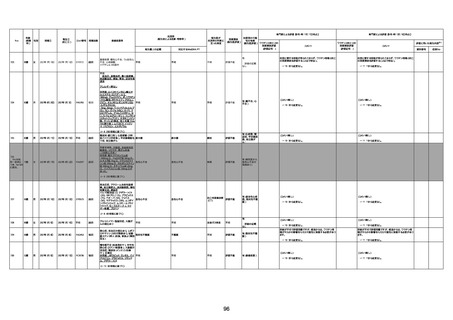
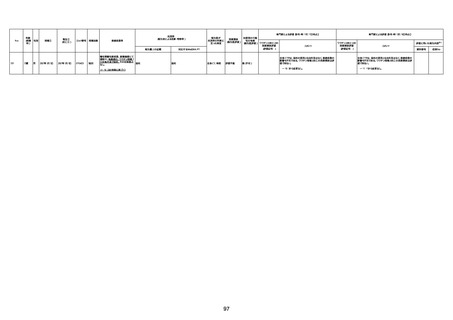
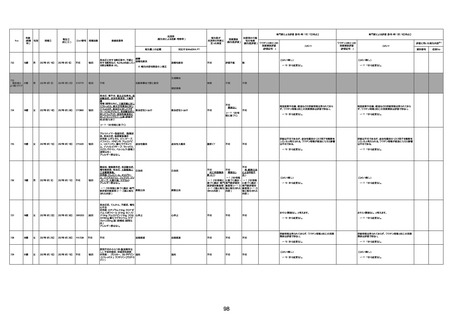
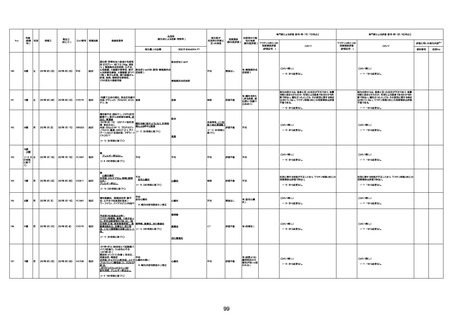
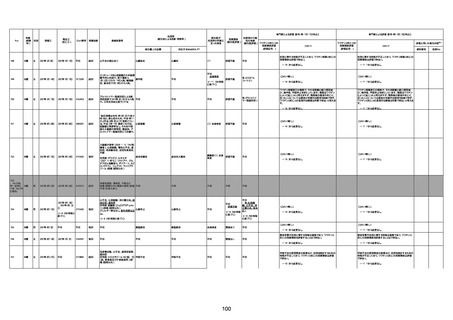
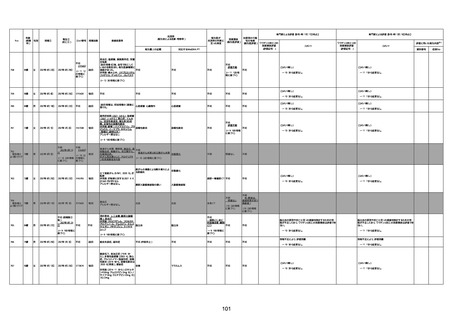
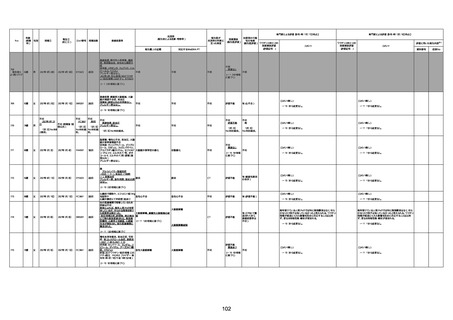
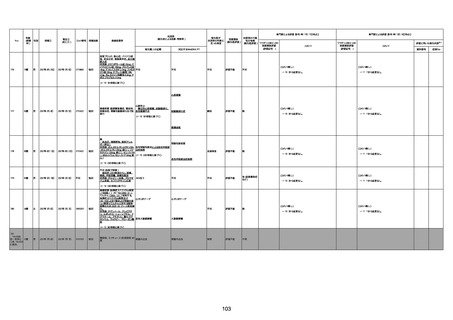
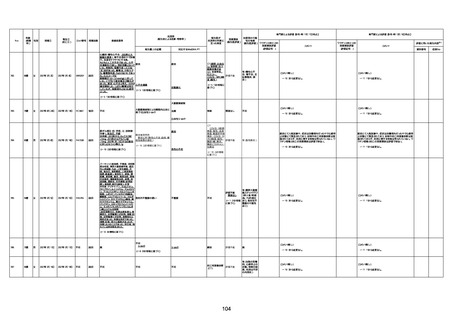
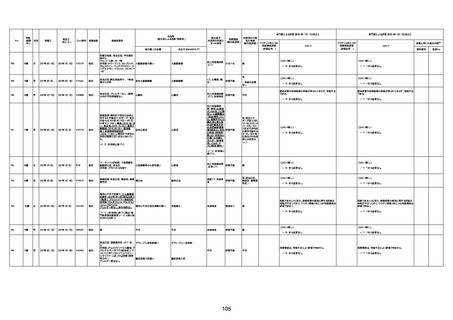
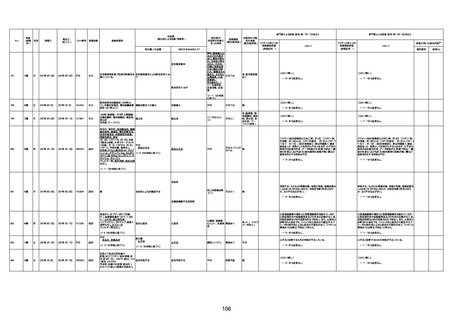
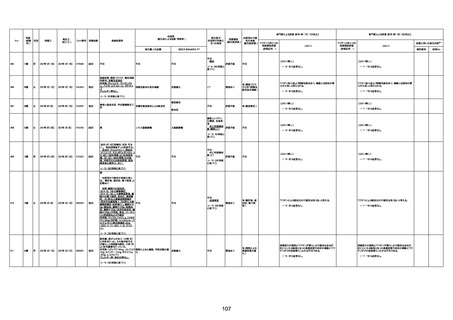
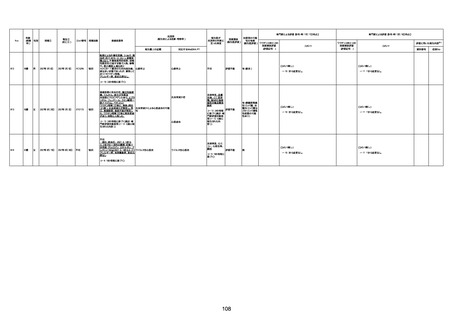
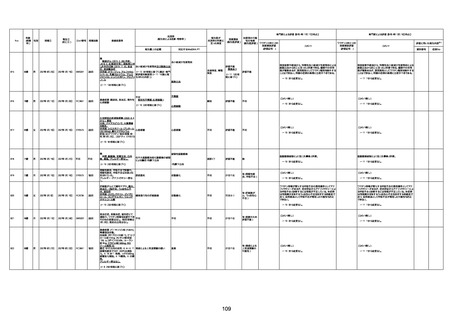
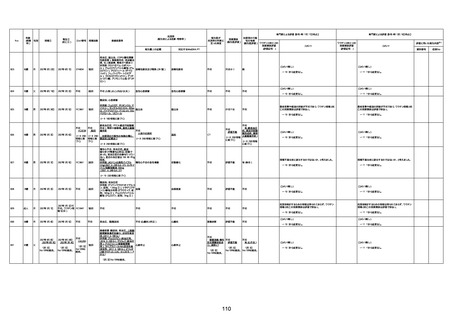
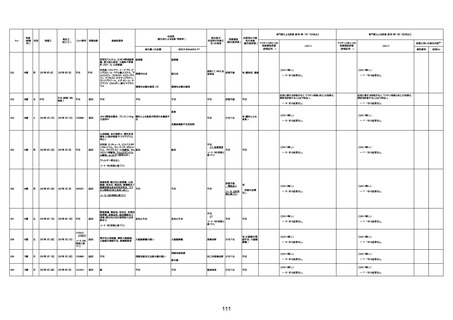
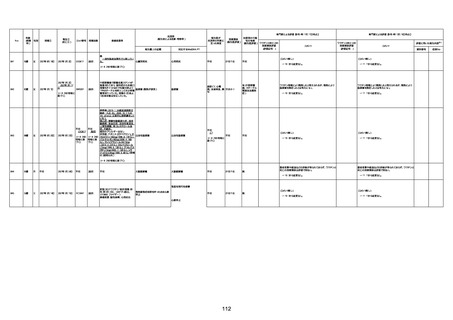
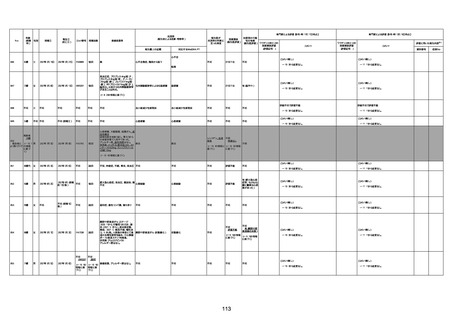
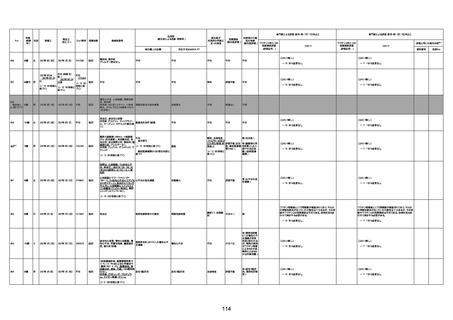
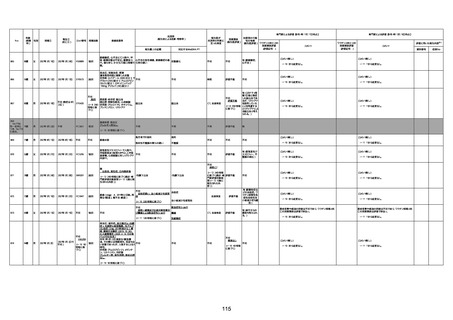
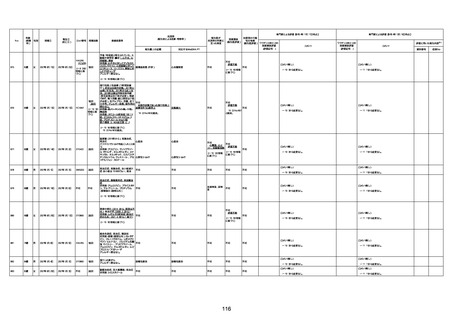
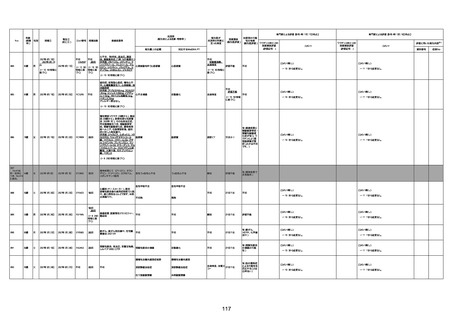
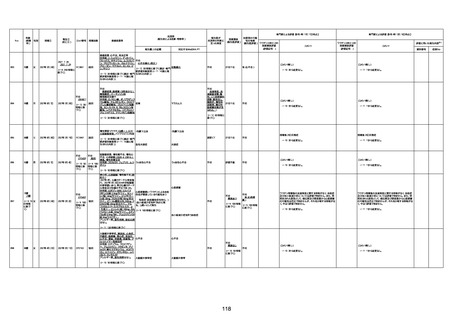
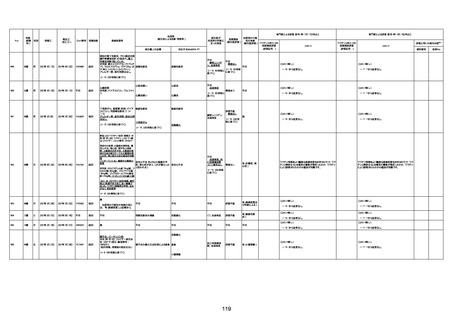
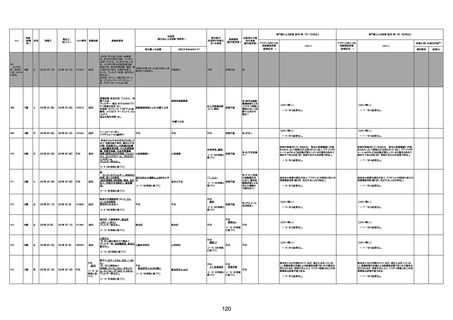
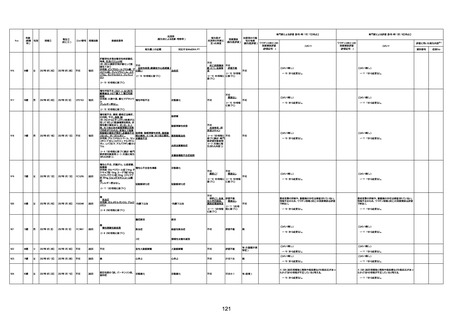
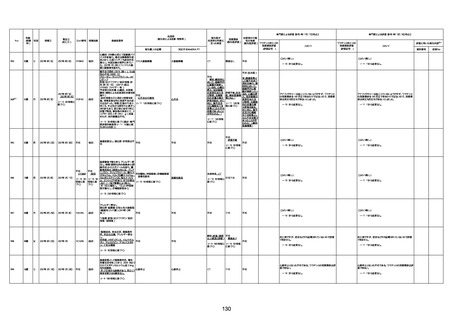
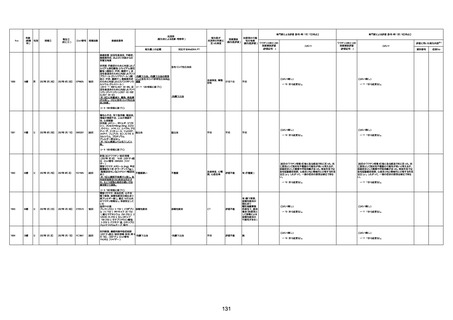
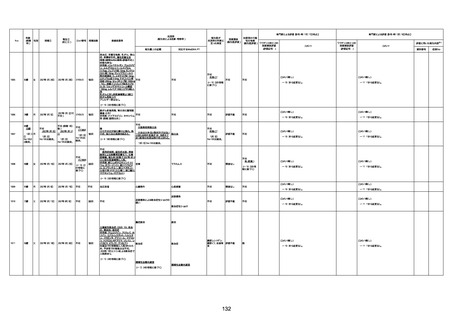
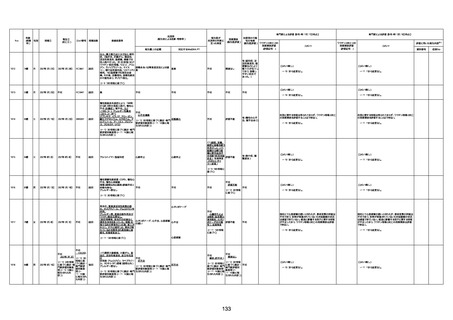
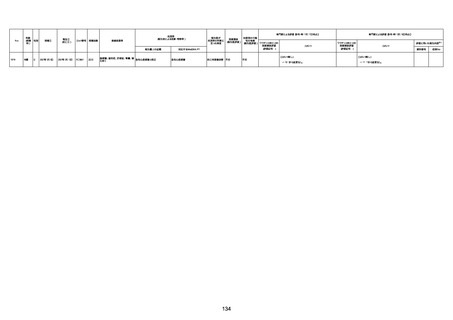
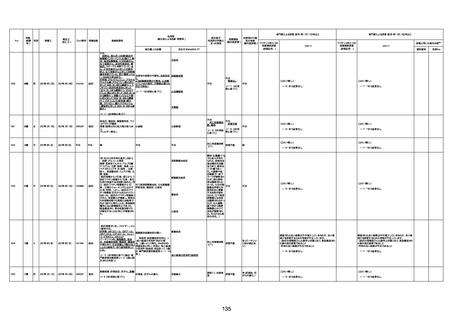
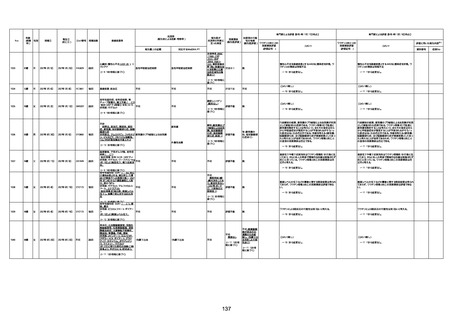
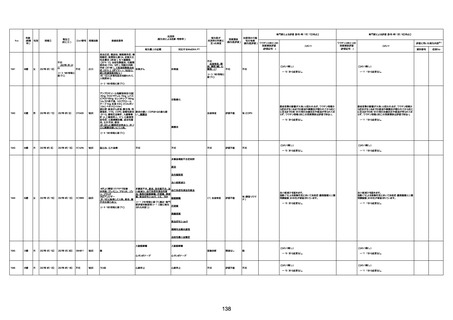
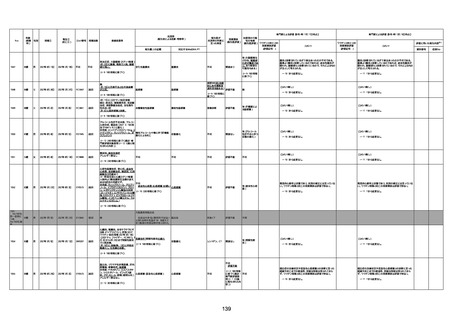
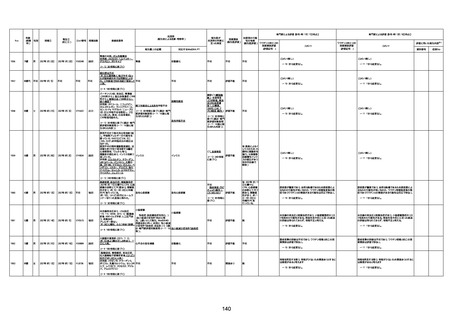
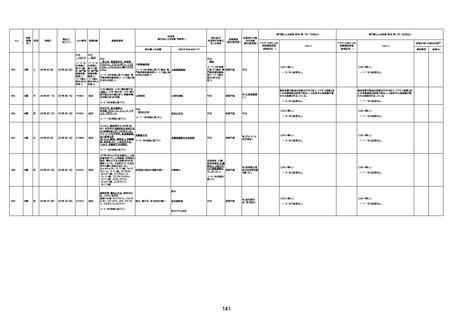
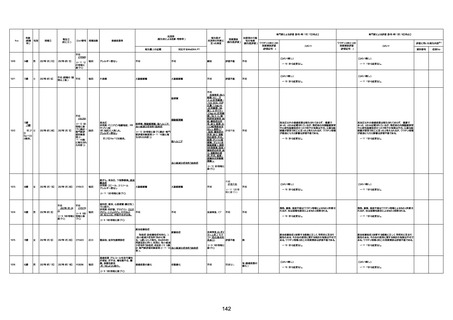
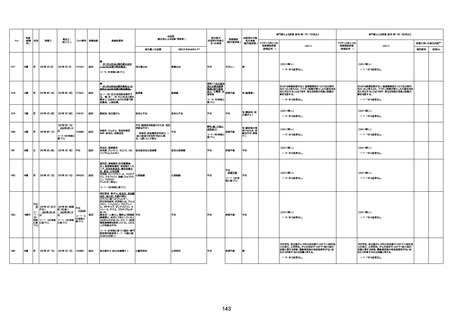
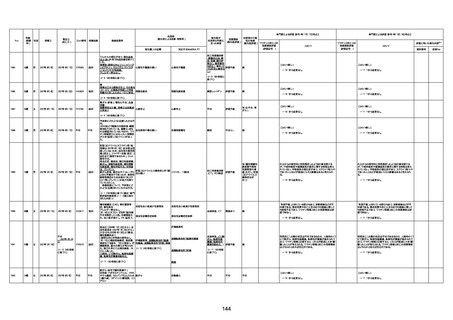
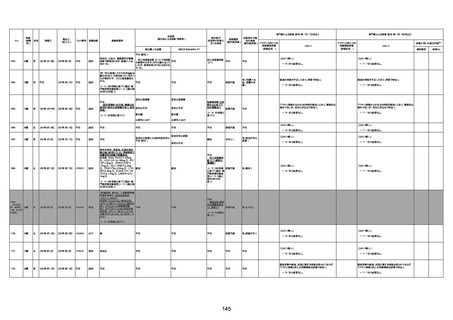
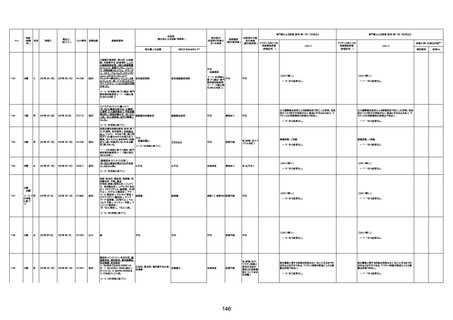
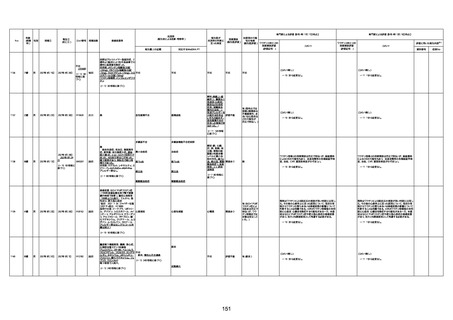
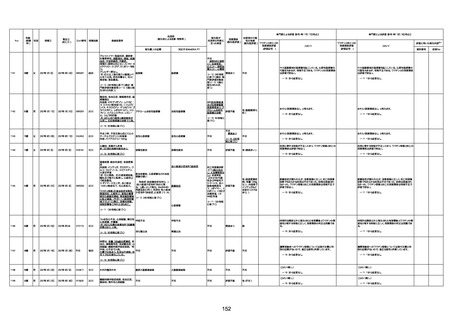
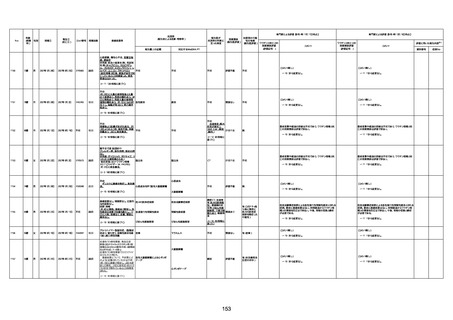
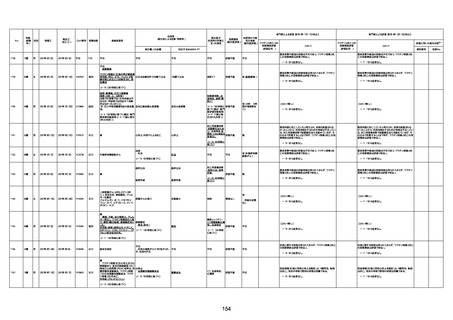
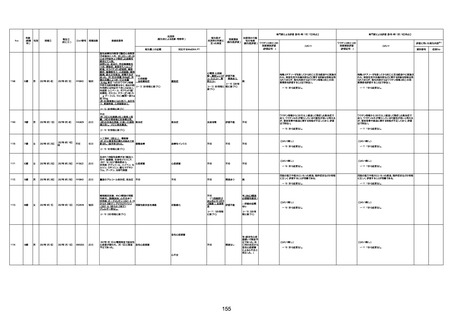
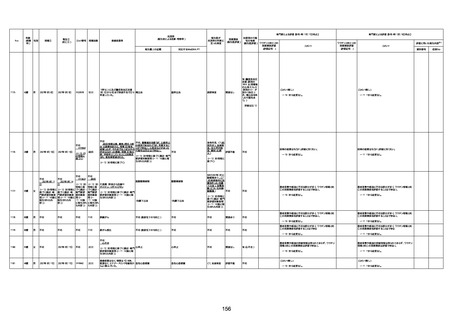
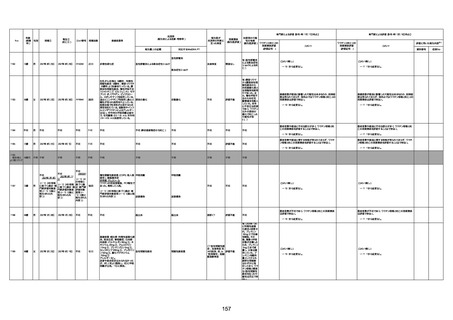
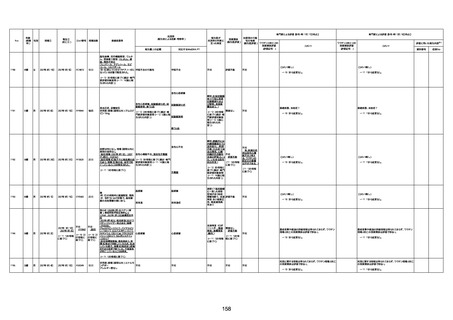
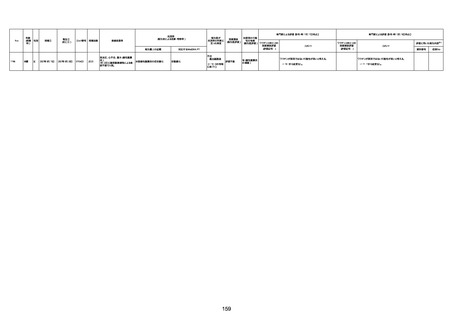
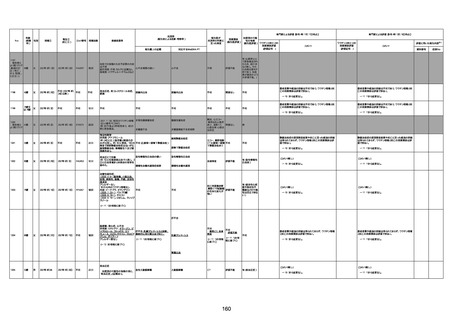
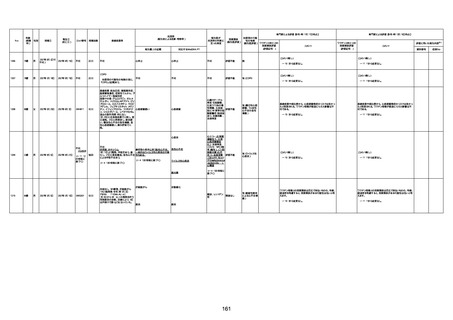
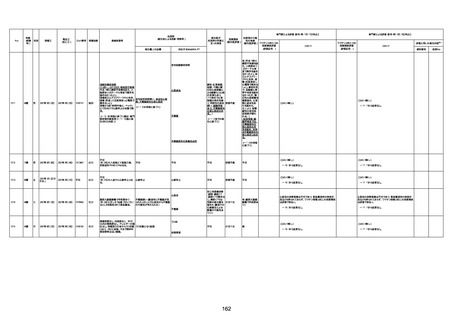
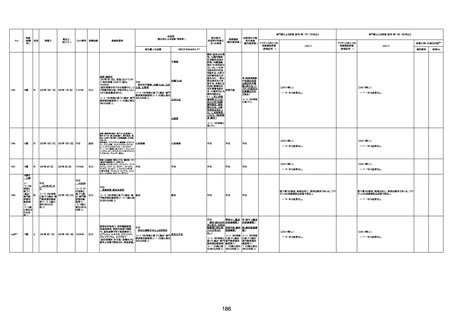
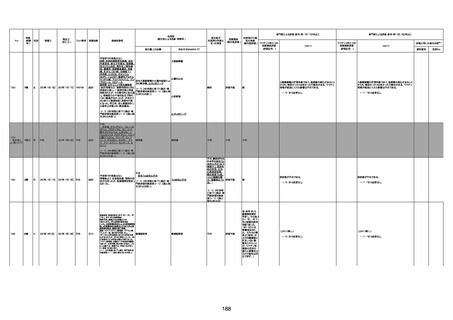
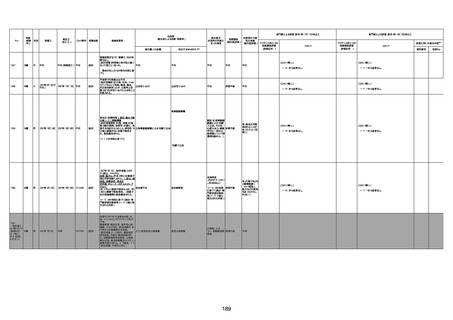
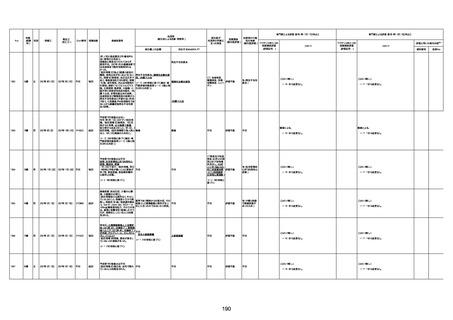
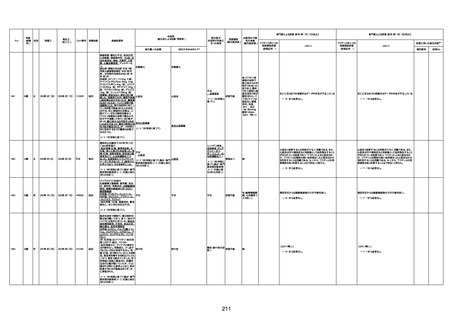
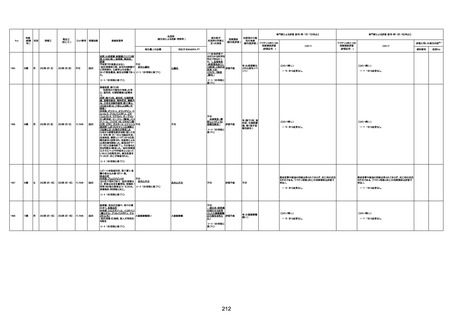
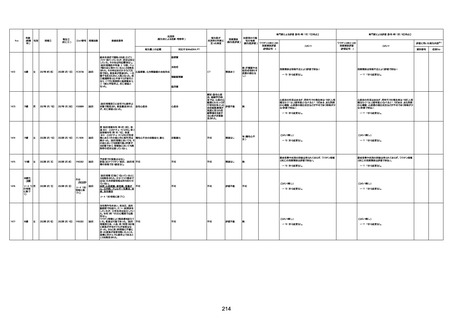
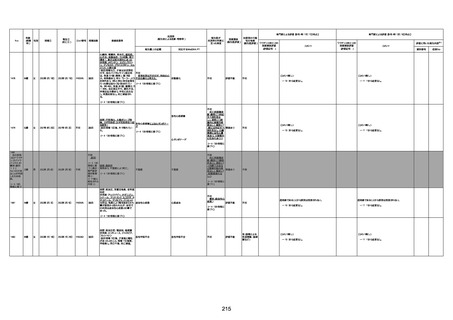
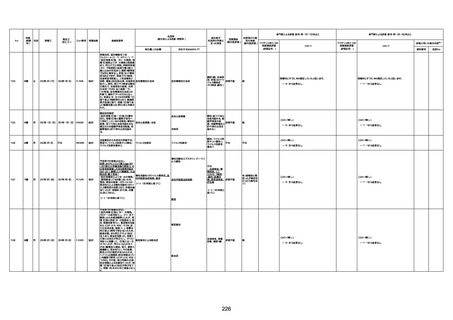
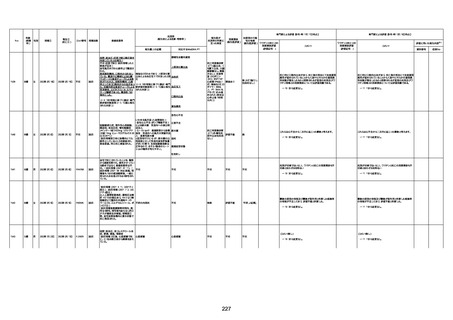
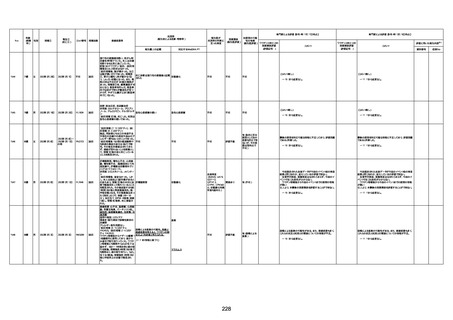
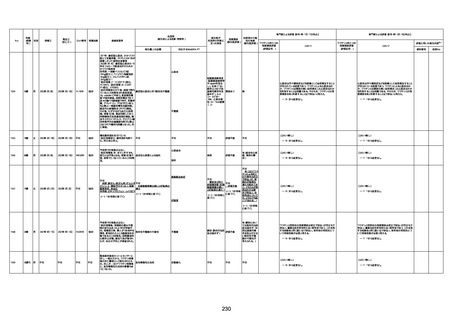
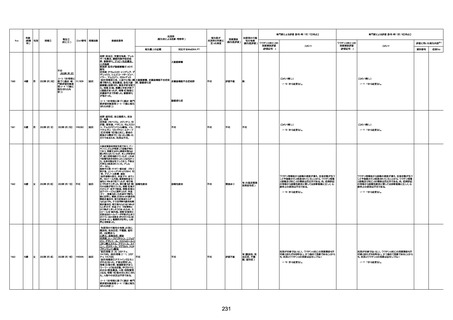
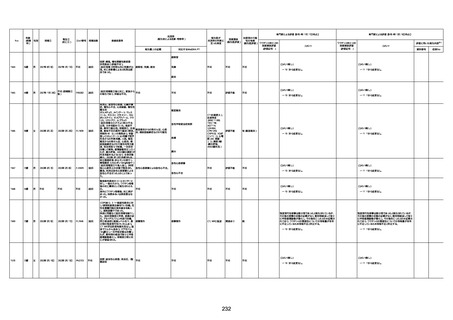
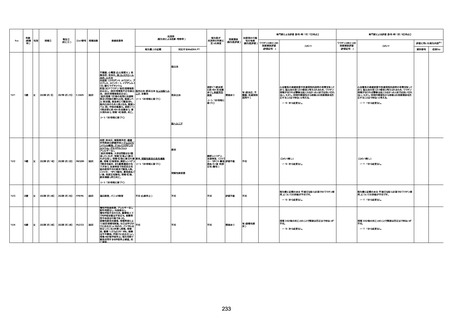
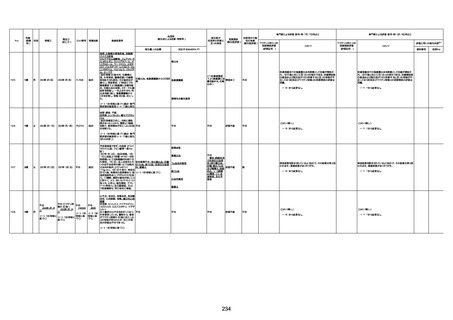
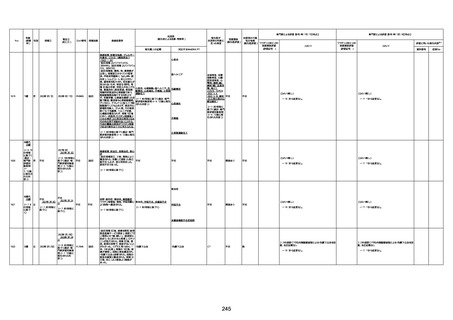
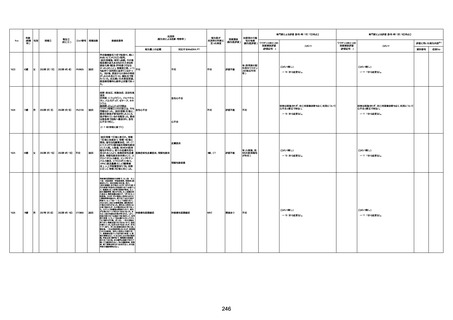
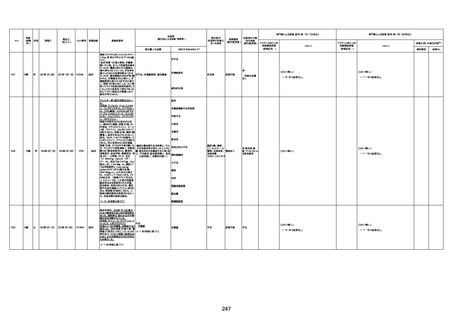
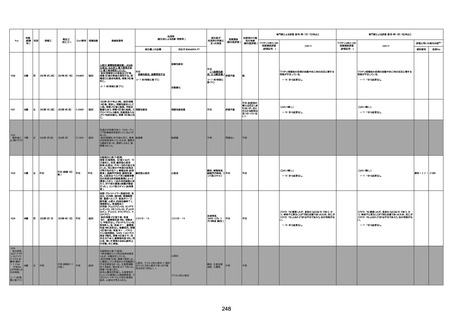
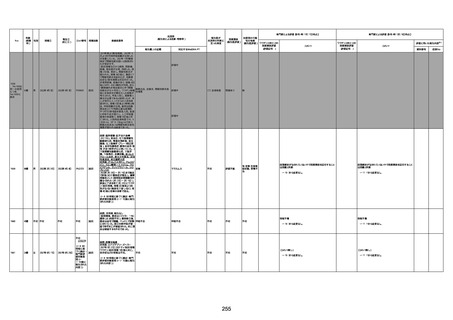
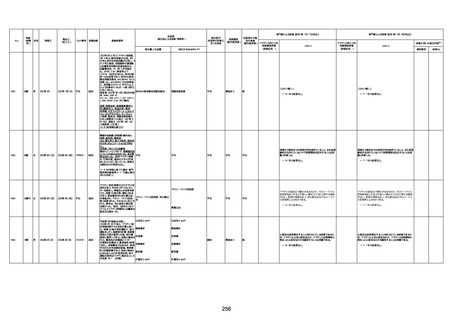
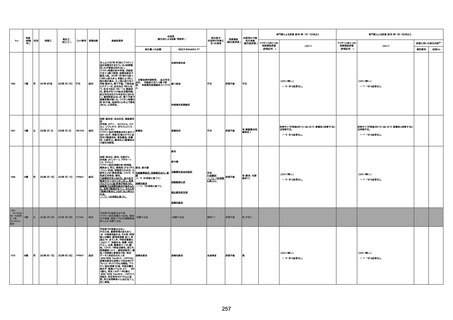
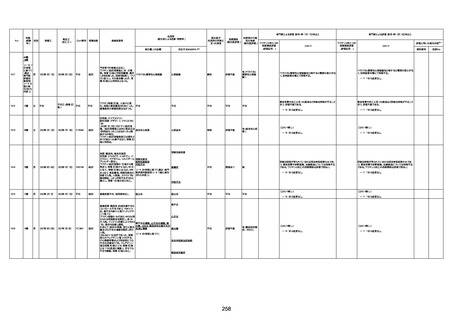
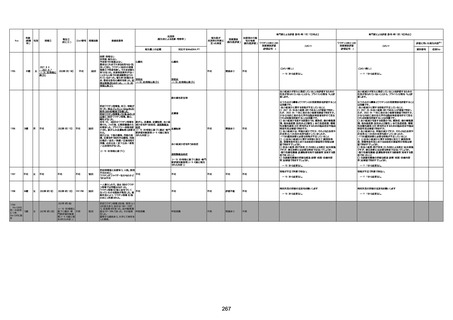
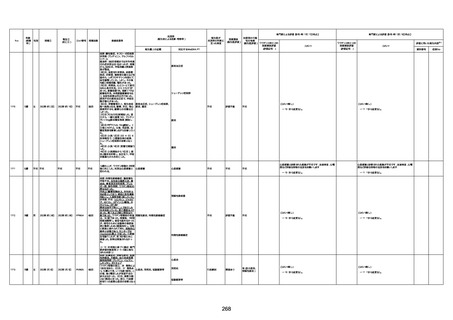
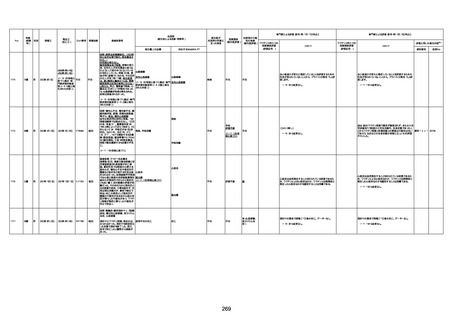
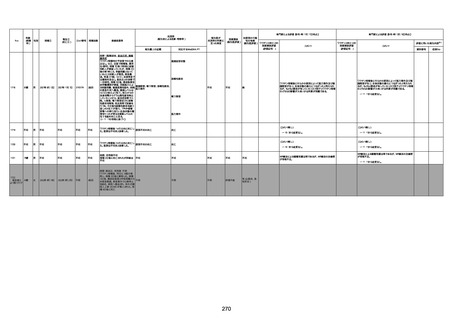
資料1-3-1 新型コロナワクチン接種後の死亡として報告された事例の概要(コミナティ筋注) (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00056.html |
| 出典情報 | 第89回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第21回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(12/16)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
反応検討部会、令和4年度第21回薬事・食品衛生審
議会薬事分科会医薬品等安全対策部会安全対策調査
会(合同開催)
資料
1-3-1
2022(令和4)年12月16日
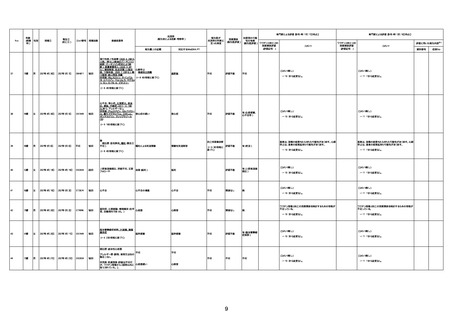
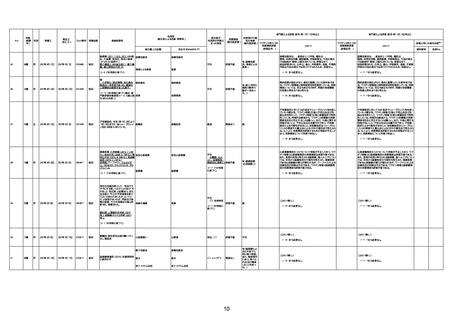
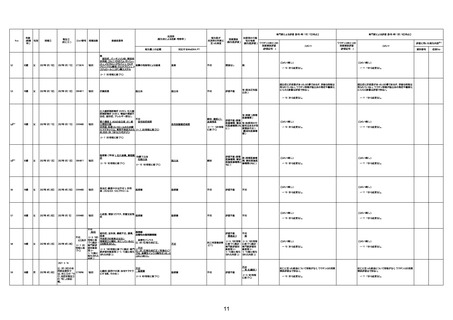
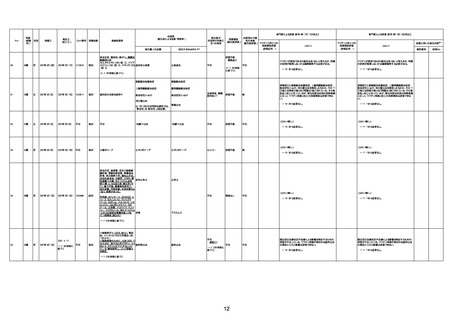
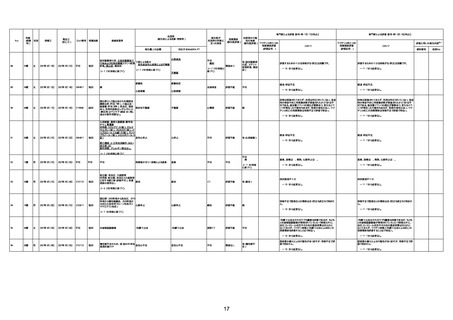
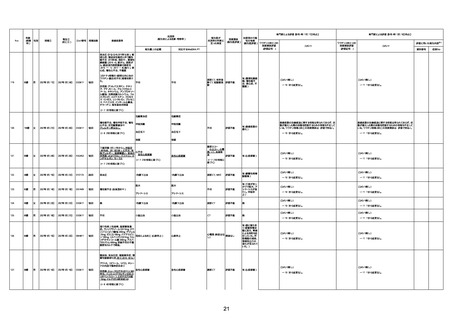
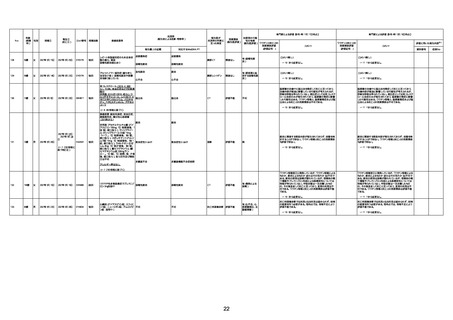
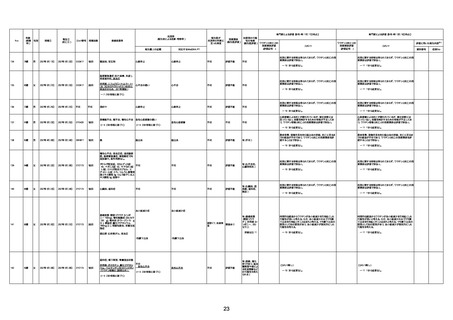
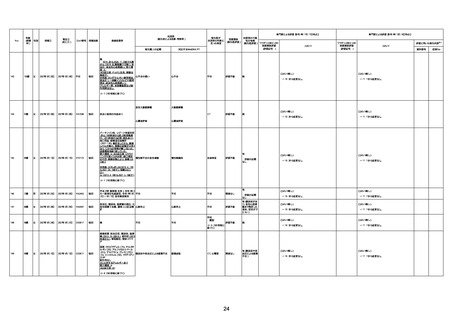
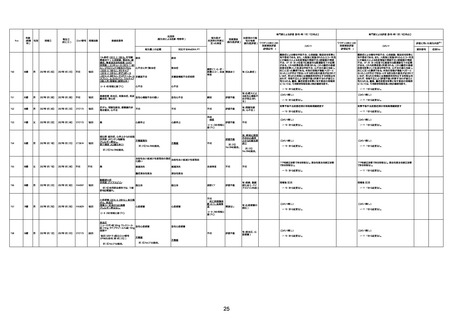
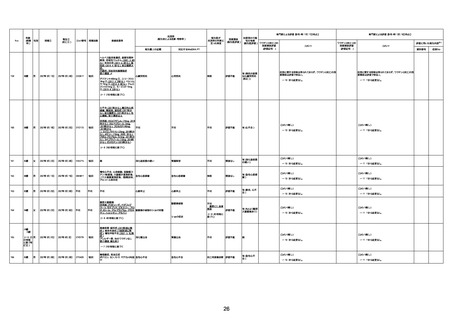
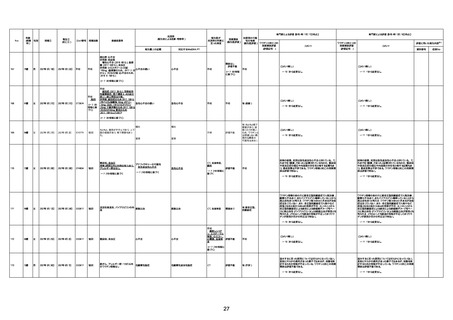
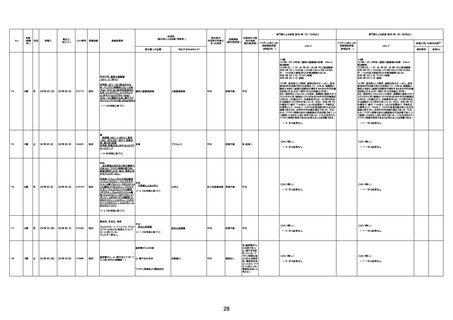
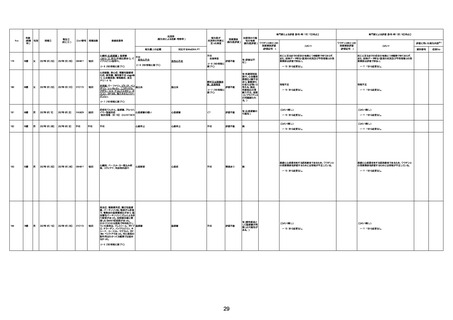
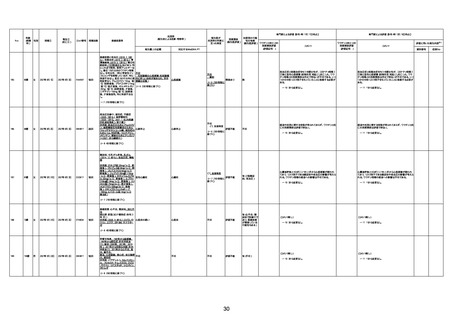
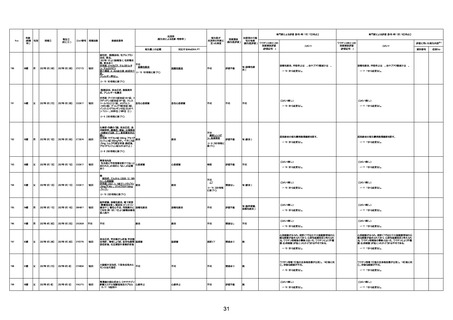
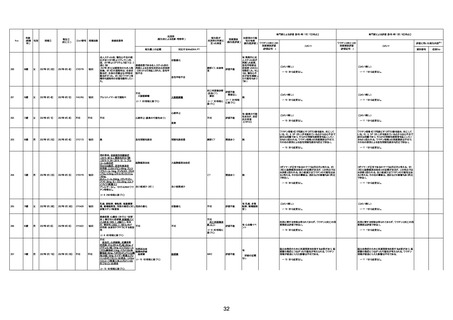
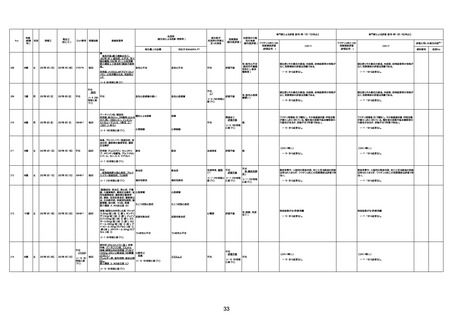
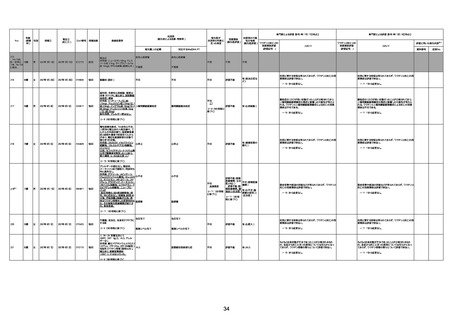
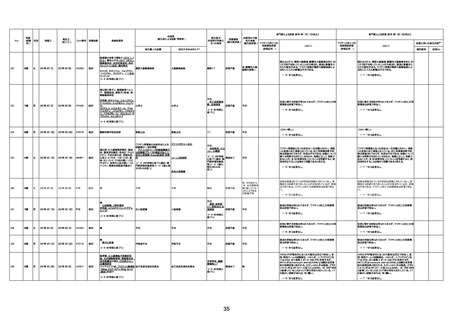
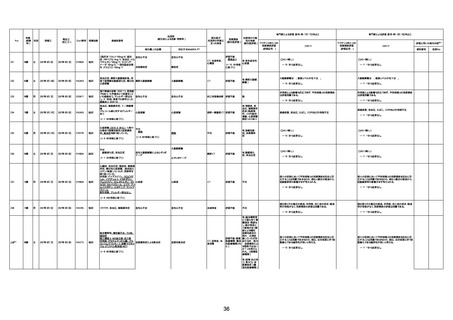
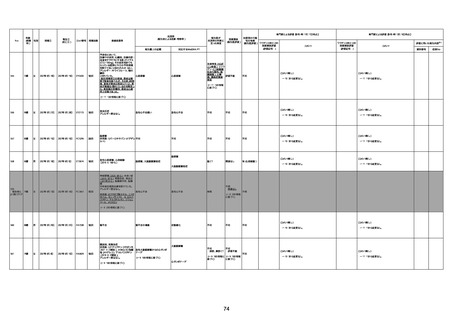
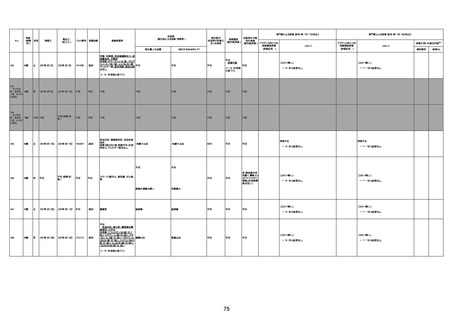
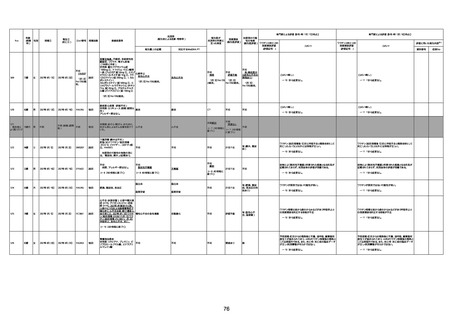
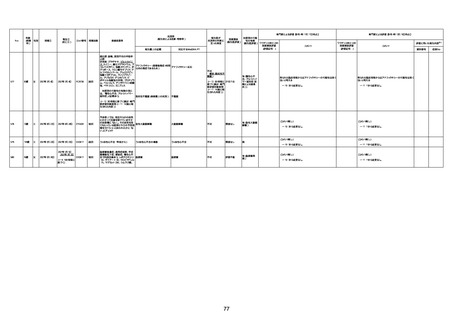
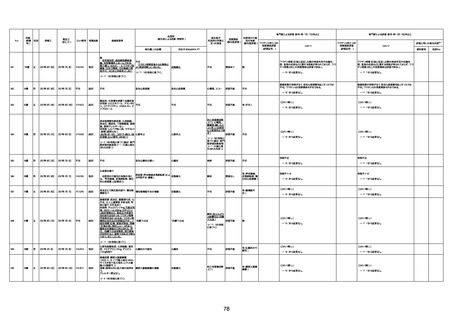
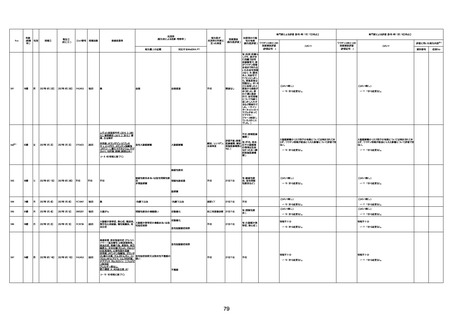
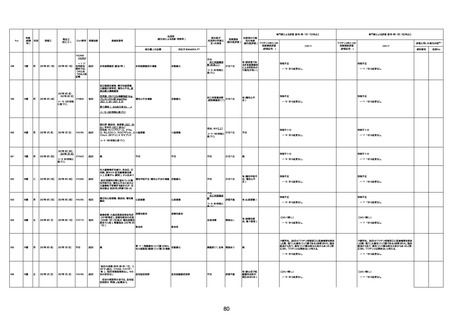
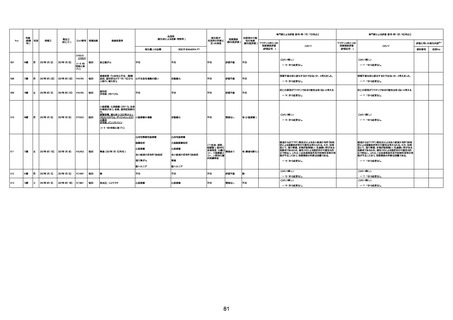
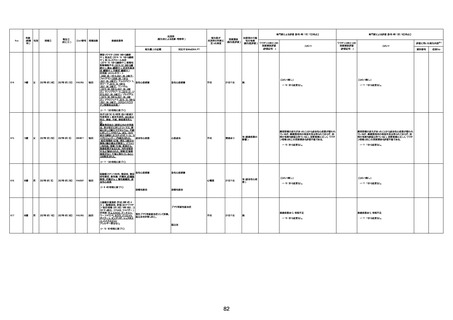
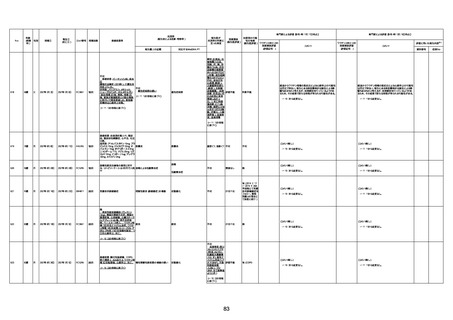
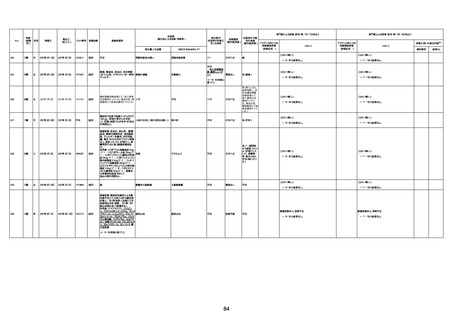
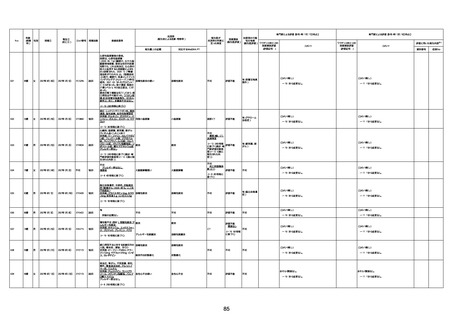
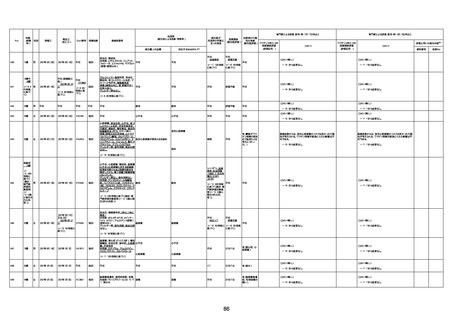
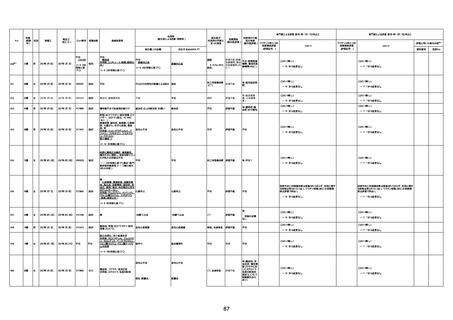
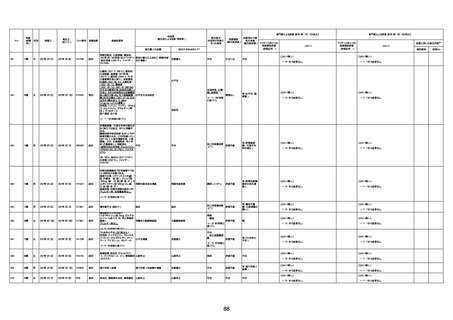
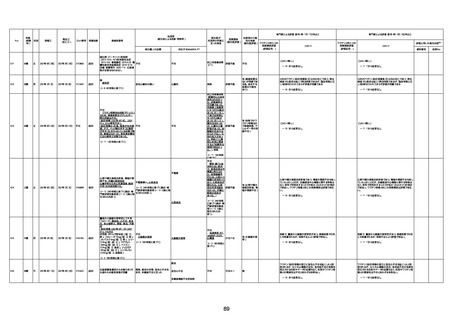
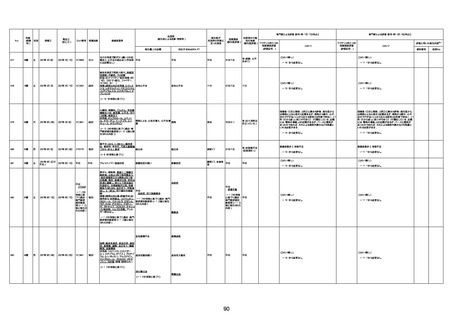
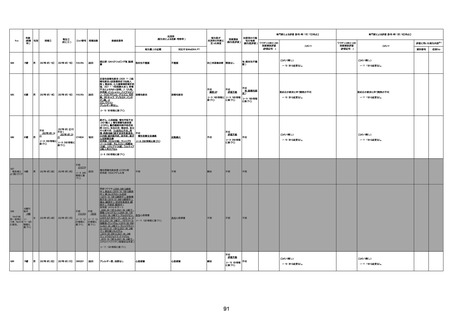
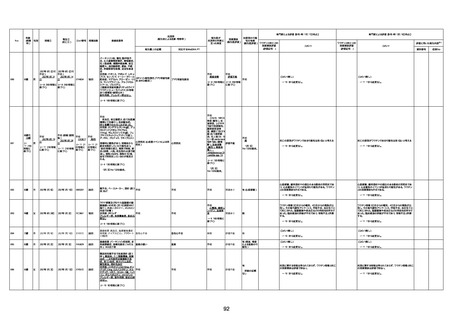
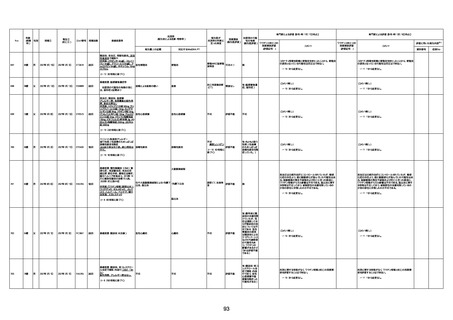
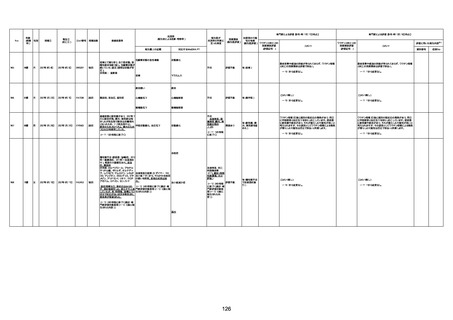
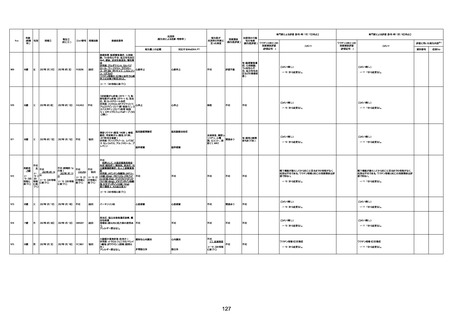
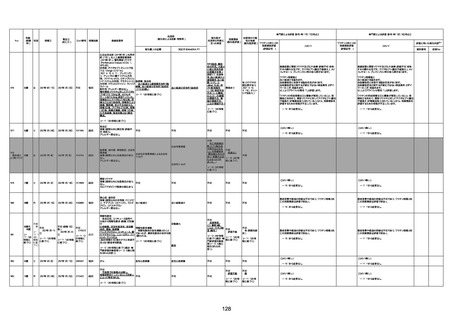
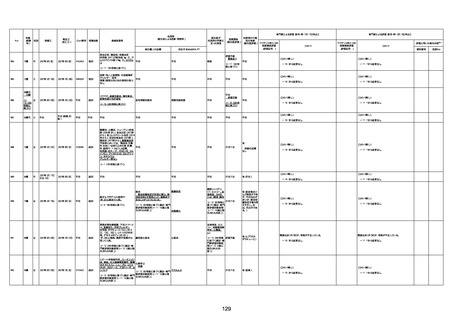
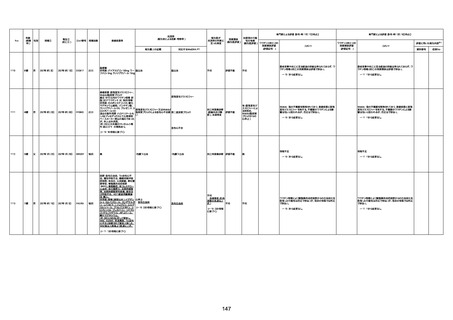
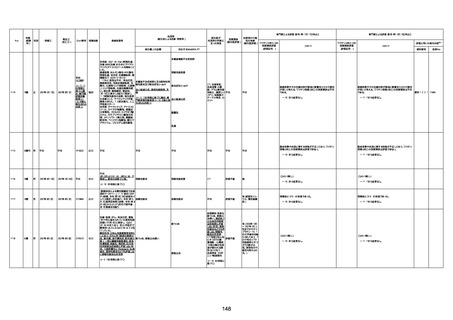
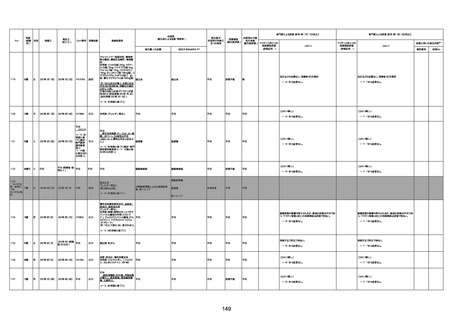
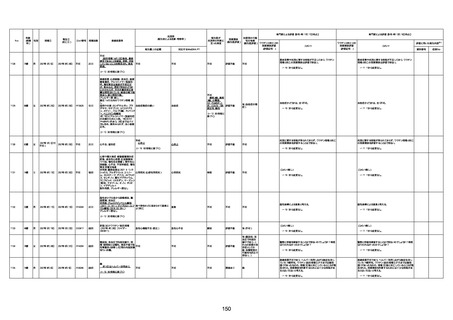
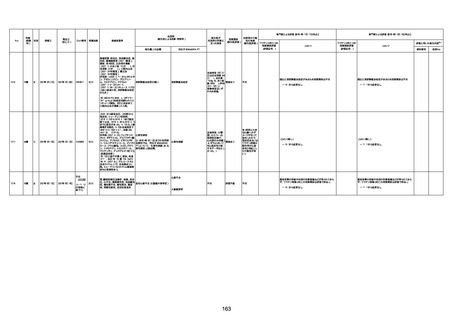
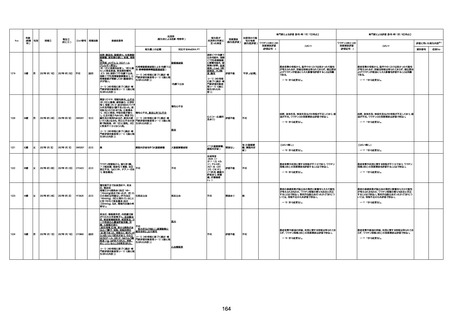
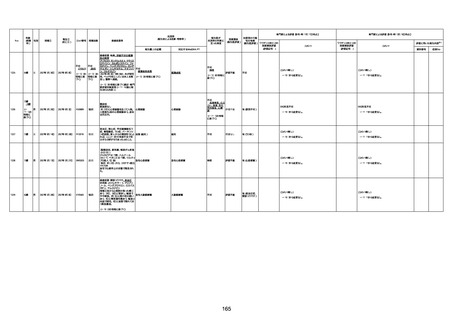
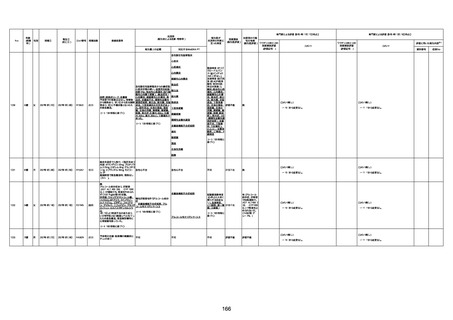
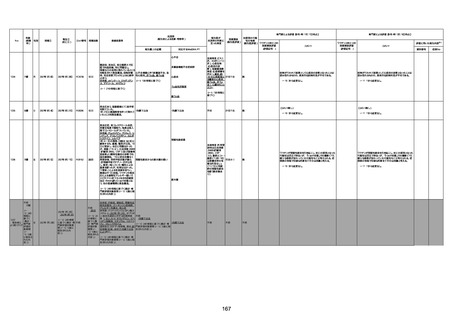
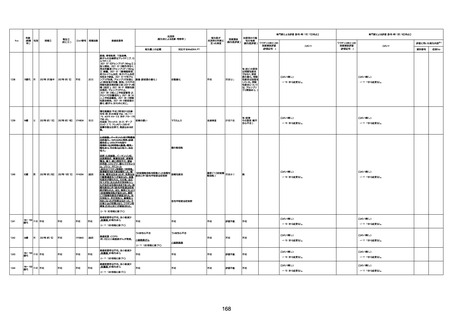
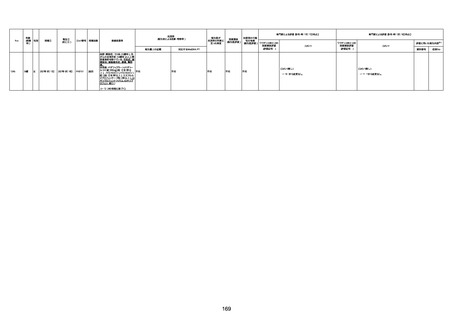
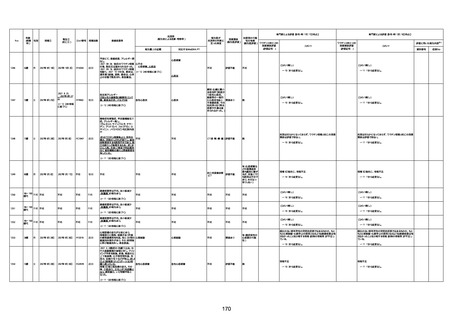
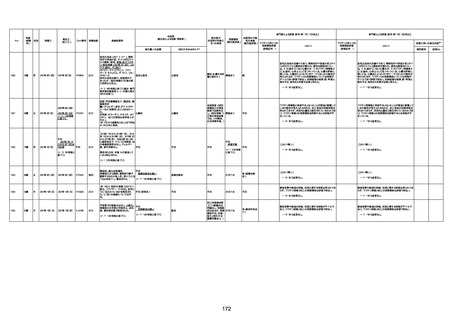
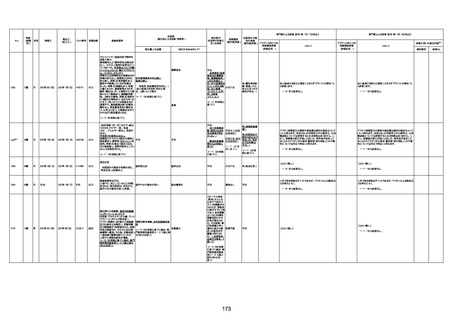
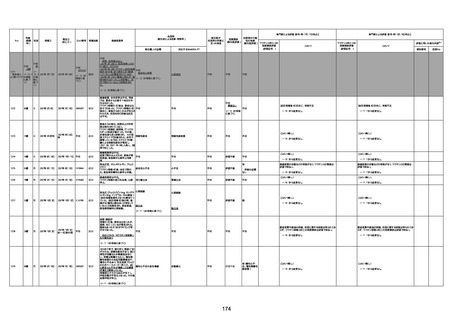
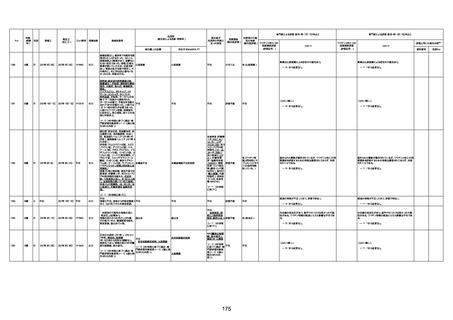
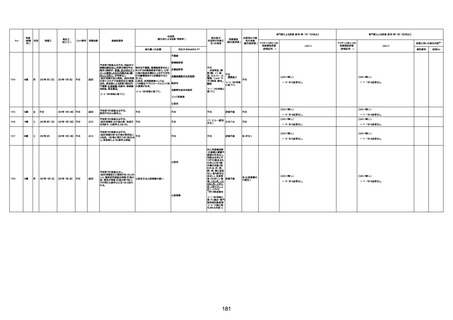
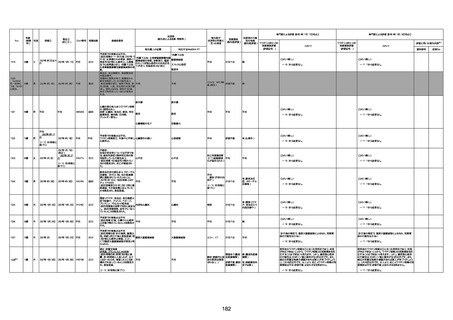
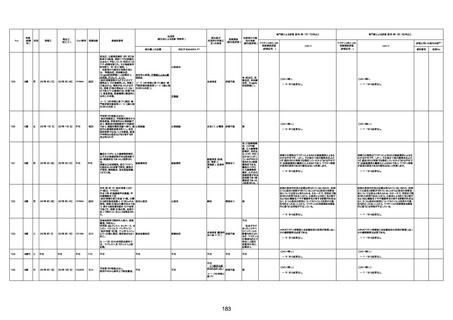
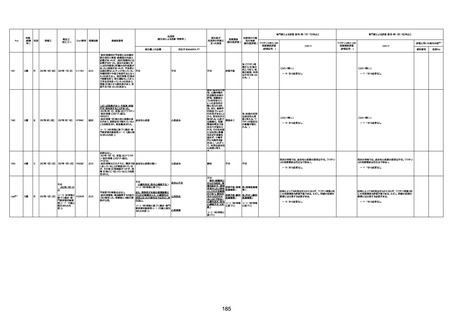
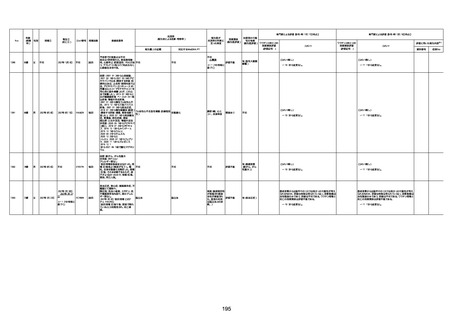
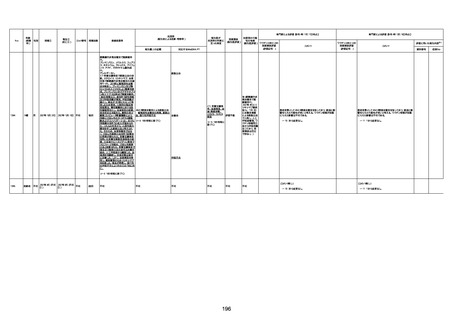
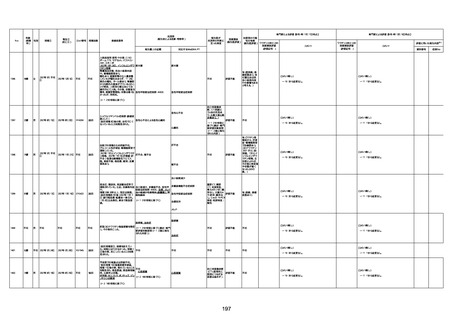
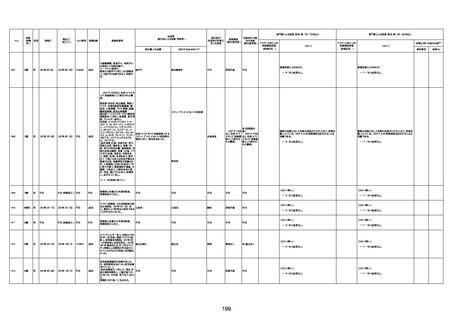
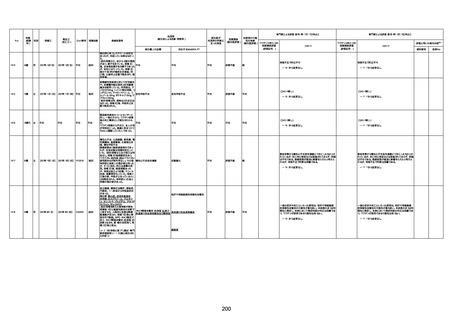
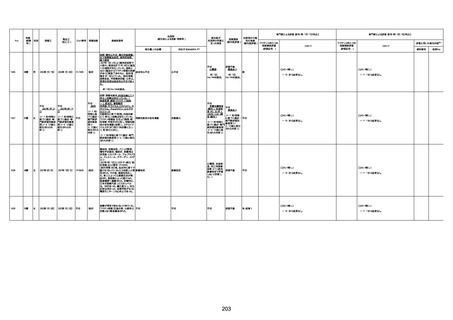
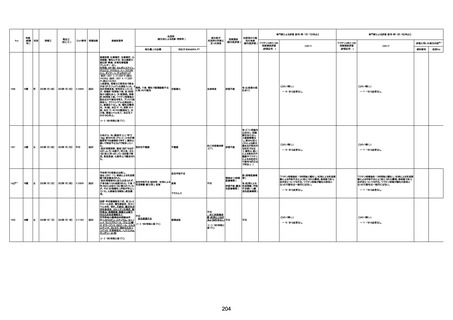
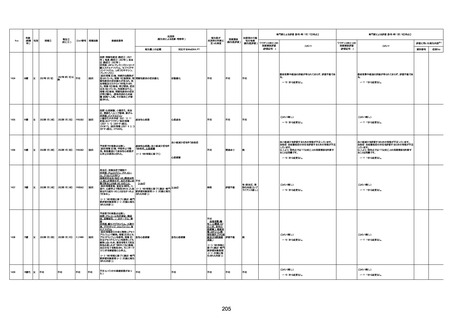
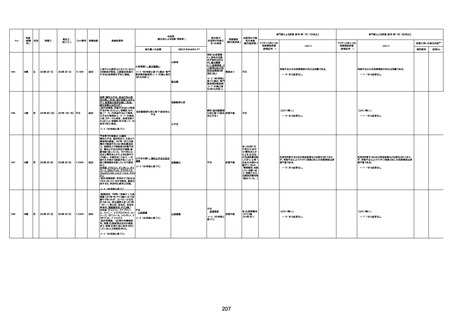
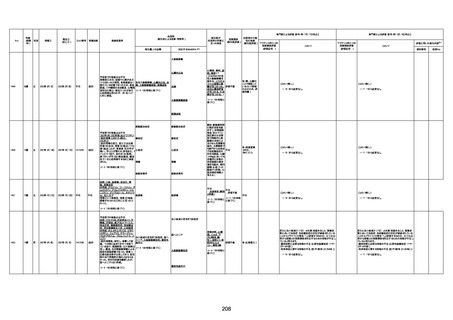
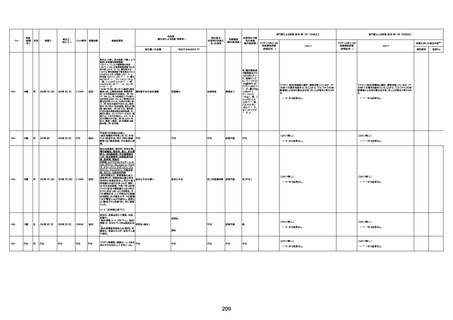
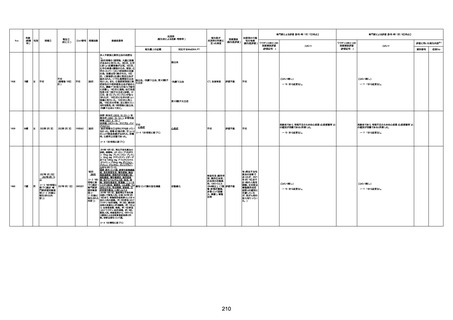
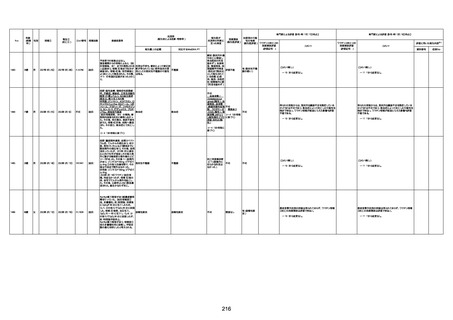
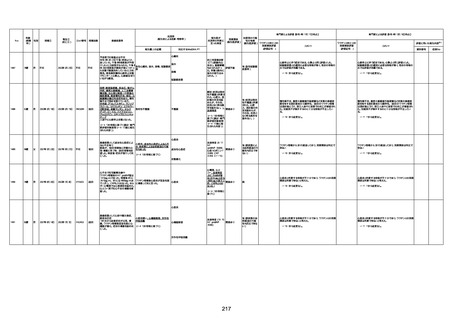
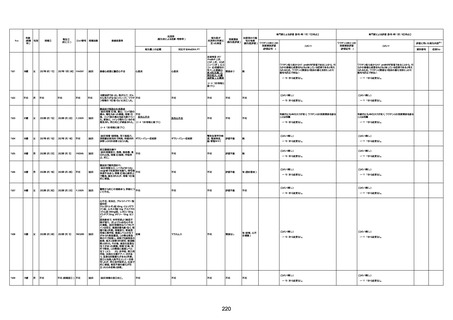
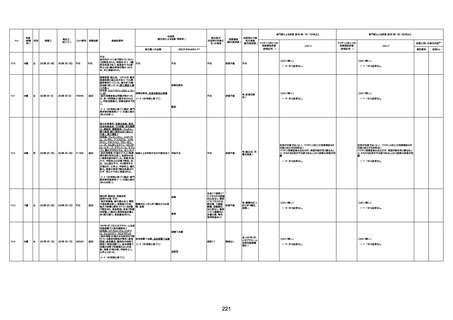
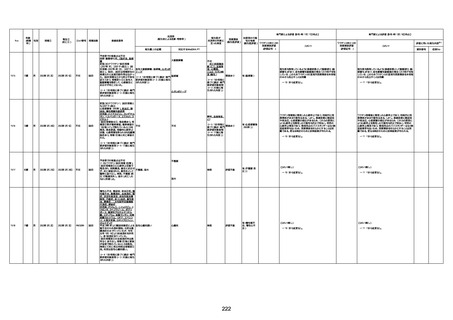
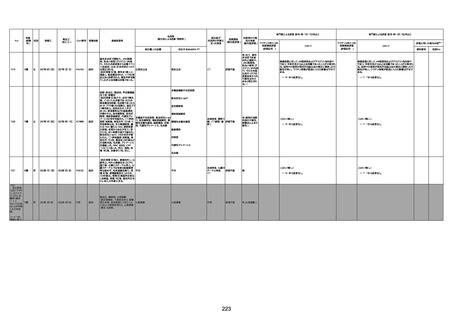
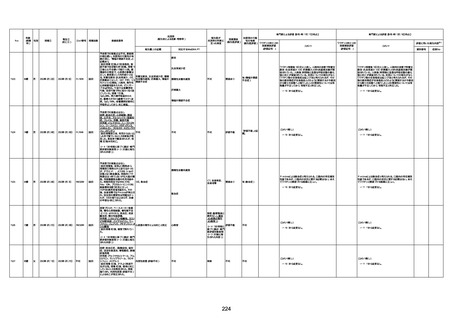
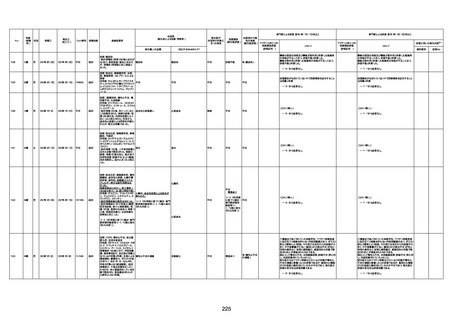
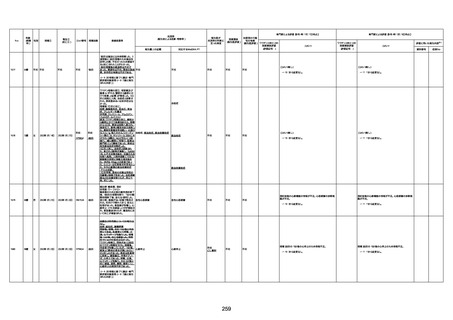
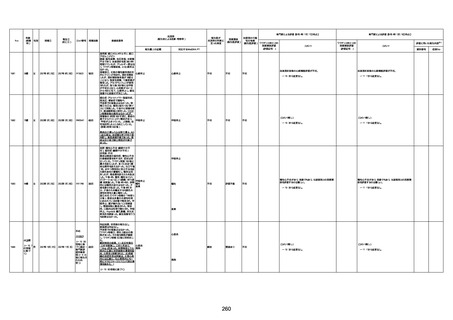
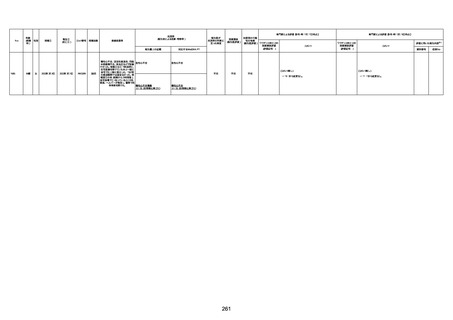
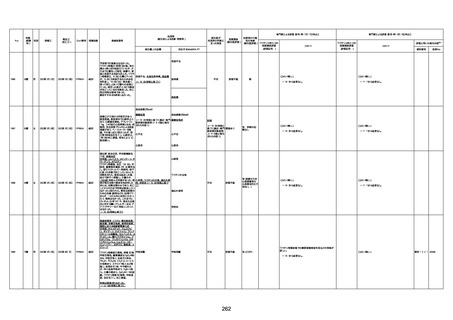
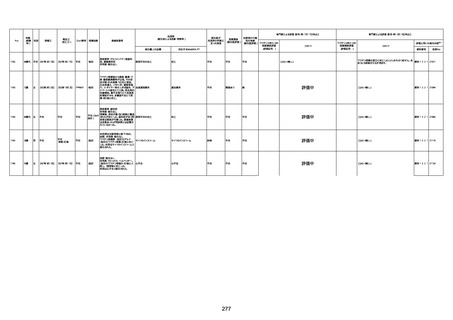
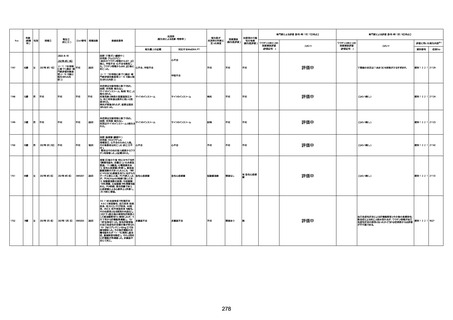
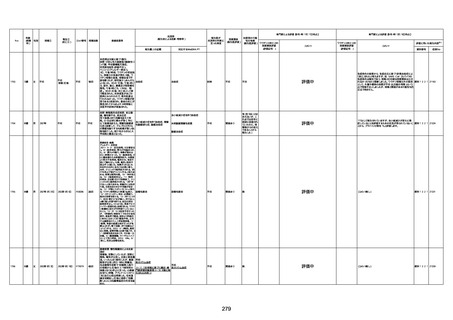
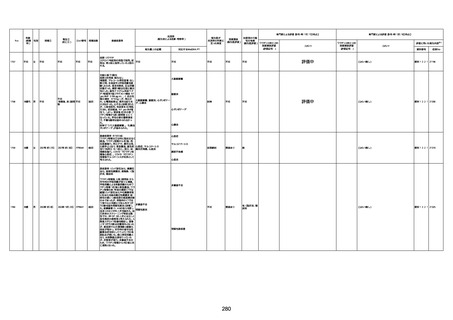
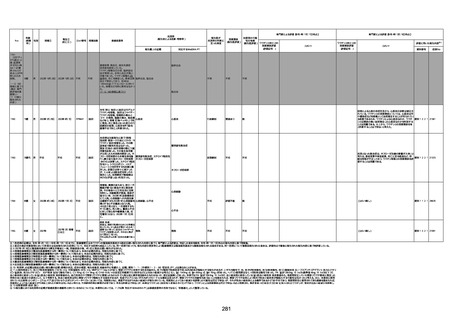
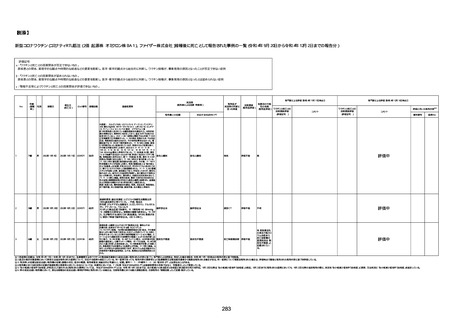
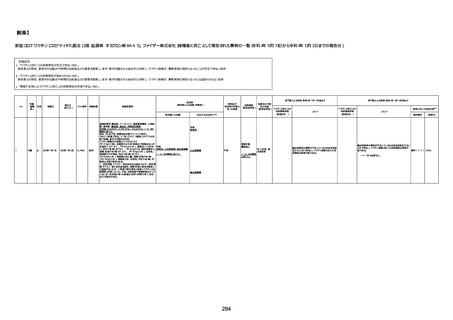
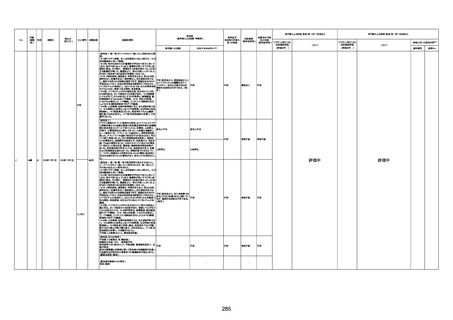
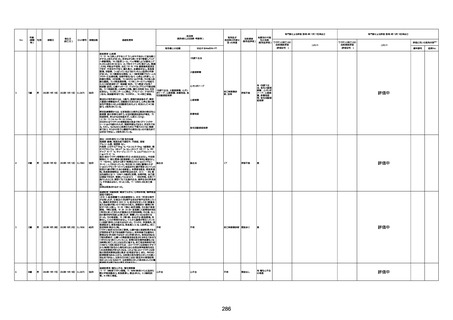
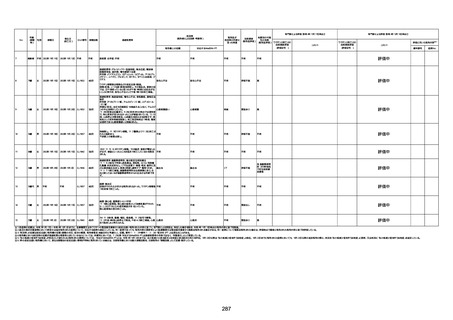
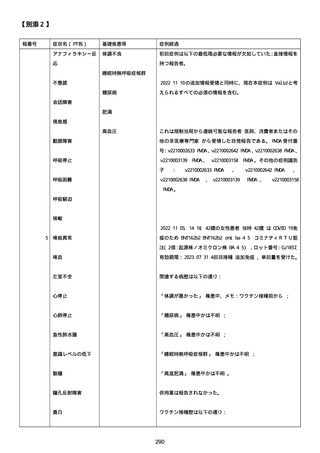
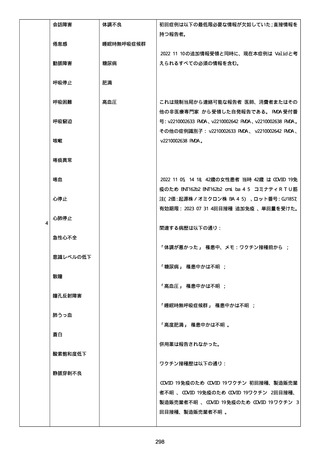
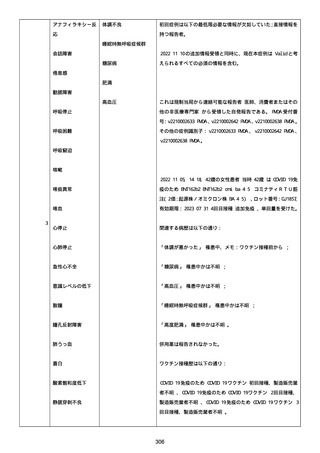
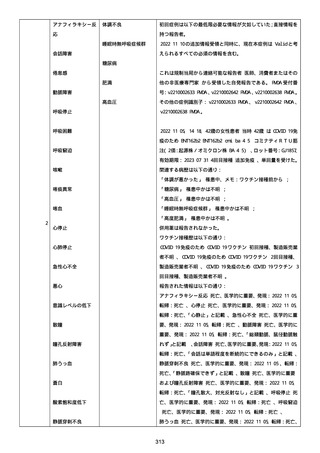
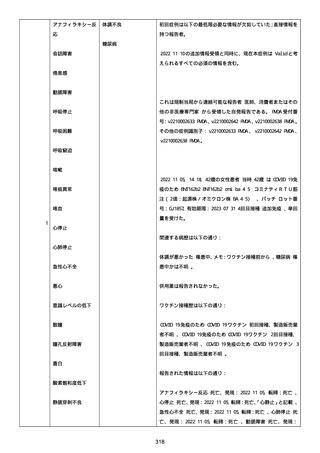
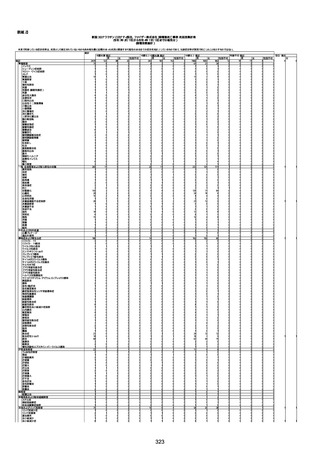
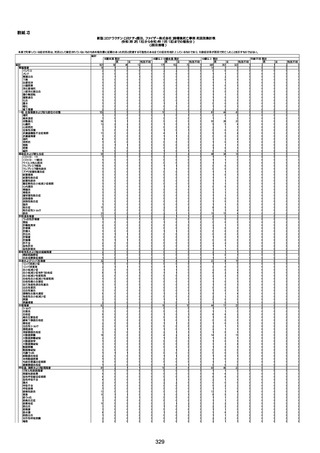
新型コロナワクチン接種後の死亡として報告された事例の概要
(コミナティ筋注、ファイザー株式会社)
1.報告状況
○ 12月16日審議会 集計期間:令和3年2月17日~令和4年11月13日
11月11日審議会時点
総件数
12月16日審議会時点
うち4回目以降
1,683
コミナティ筋注(総数)
29
総件数注2
注1
うち4回目以降
1,707
35
コミナティRTU筋注
(2価:起源株/オミクロン株BA.1)
-
-
0
0
コミナティRTU筋注
(2価:起源株/オミクロン株BA.4-5)
-
-
2
2
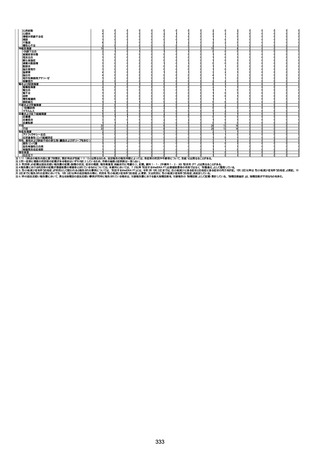
注1 製造販売業者による調査結果、症例の重複等が判明し報告が取り下げられことがある。取り下げ状況によっては、4回目以降接種後の副
反応疑い事例の増加数が1~5回目接種後の報告の増加数を上回ることや、累計報告件数が前回の集計期間時から減少することがある。
注2 コミナティ筋注(総数)について、11月13日までの調査において同一症例であることが明らかとなった25組については報告内容を統合
し、各1件として計上。また、31件の取り下げあり。他の新型コロナワクチンの症例であることが明らかとなった4件は除外。別紙1の症
例No(No.1~1,765)と報告事例数(1,707件)は一致しない。
※ コミナティ筋注(総数)の副反応疑い報告等の件数については、起源株ワクチン、2価ワクチン及び株不明のワクチンの総数として集計
している。
2.専門家の評価
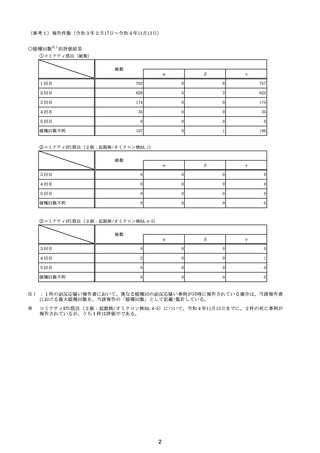
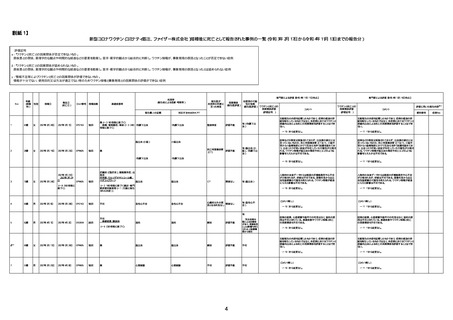
○ 令和4年11月13日までに報告された死亡事例を対象に、専門家の評価を実施(別紙1)。評価結果は、以下のとお
り。
コミナティ筋注
(総数)
因果関係評価結果(公表記号)
α(ワクチンと死亡との因果関係が否定できないもの)
0件
0件
0件
β(ワクチンと死亡との因果関係が認められないもの)
10件
0件
0件
1,696件
0件
1件
γ(情報不足等によりワクチンと死亡との因果関係が評価できないもの)
※
コミナティRTU筋注
コミナティRTU筋注
(2価:起源株/オミ (2価:起源株/オミ
クロン株BA.1)
クロン株BA.4-5)
コミナティRTU筋注(2価:起源株/オミクロン株BA.4-5)について、令和4年11月13日までに、2件の死亡事例が
報告されているが、うち1件は評価中である。
1