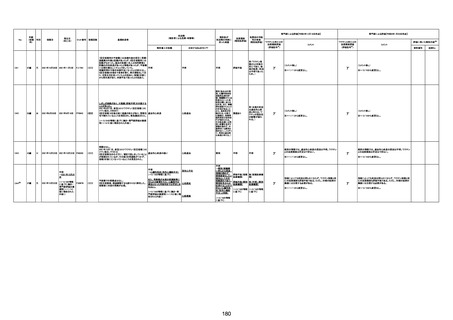
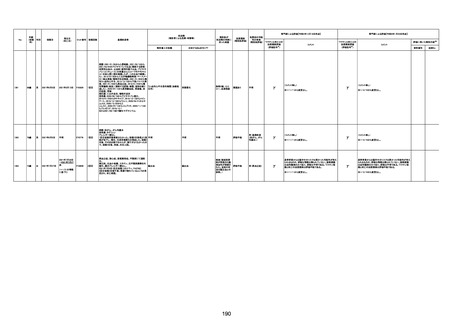
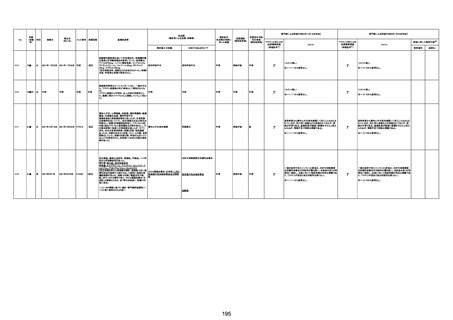
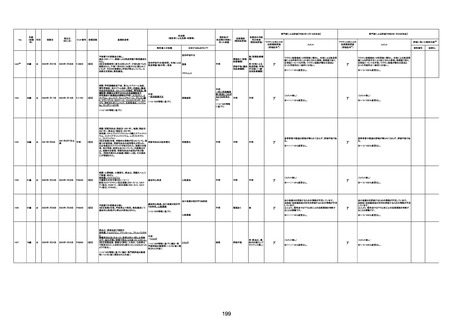
資料1-3-1 新型コロナワクチン接種後の死亡として報告された事例の概要(コミナティ筋注) (276 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/vaccine_hukuhannou-utagai-houkoku.html |
| 出典情報 | 第90回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第23回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(1/20)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
年齢
(接種
時)
性別
接種日
発生日
(死亡日)
ロット番号
接種回数
死因等
(報告者による見解・考察等)
基礎疾患等
報告書上の記載
75歳
男
不明
不明
不明
3回目
1779
67歳
男
2022年8月
不明
不明
1回目
本報告は文献に基づく情報
病歴等:喫煙、間質性肺疾患、遠隔転移を伴う結腸
がん
間質性肺疾患
剖検によって「通常の間質性肺炎に重なったびまん
性肺胞障害」が明らかになった。
薬剤歴:化学療法オキサリプラチン
5回目
2022年6月9日に脳梗塞(左前頭葉深部白質梗塞)を発症
して入院、リハビリテーションを経て退院後は抗凝固剤を
内服。2022年12月7日10:00頃に新型コロナワクチン(5回
目;ファイザー社製)の接種を受けて10時半頃に帰宅、
12:00に昼食を摂った後ソファで横になっており、一度ソ
ファーから転落して側頭部を打撲している。12:40に同居
の夫が外出した際には普段と変わりは無し。15:15に夫が
右視床出血、脳室内穿破、閉塞性
帰宅した際には意識障害を認めたために救急搬送。来院
水頭症
時意識レベルはJCS200、体温40.7度、血圧
172/133mmHgであり、直ちに頭部CT撮影を行ったところ
右視床出血、脳室内穿破、閉塞性水頭症の状態であるこ
とが確認された。CT撮影後短時間で血圧の低下、瞳孔散
大、死戦期呼吸と、救命困難な状態となり、16:43に夫立
ち会いのもと死亡が確認された。
既往:脳梗塞、高血圧
1781
1782
86歳
83歳
女
男
男
2022年12月7日
不明
2022年8月23日
2022年12月7日
2021年5月19日
2022年9月22日
不明
不明
FR4768
不明
CPAで救急搬送
4回目
基礎疾患:高血圧、前立腺がん、心筋梗塞(2009/6/11)
高血圧の定期通院にて2022年9月16日来院時、最近「息
が切れる」との訴えあり。9月17日、9月21日来院。抗生剤
等投与するも改善なく、9月22日他院紹介。他院にて間質 間質性肺炎
性肺炎の病名にてO2低下あり(87%)専門医に紹介、ほど
なく家人より死亡したとの連絡があった。
不明
因果関係
(報告医評価)
他要因の可能
性の有無
(報告医評価)
対応するMedDRA PT
本報告は文献に基づく情報
基礎疾患等:高血圧、COVID-19
抗メラノーマ分化関連蛋白5抗体陽
軽症のCOVID-19感染症に罹患した4週間後に、ファ
性皮膚筋炎
イザー社COVID-19ワクチンの3回目接種を受けた。
COVID-19ワクチン接種11週間後に、初めて23価肺
炎球菌多糖体ワクチン(PPSV23)を接種した。
抗メラノーマ分化関連蛋白5抗体陽
PPSV23接種翌日に発熱、倦怠感と食欲不振、1週
不明
性皮膚筋炎、間質性肺疾患
間後に発疹、2週間後に息切れを発現した。
その後地元の病院に入院し、抗生物質治療が行わ
れたが状態は悪化した。
PPSV23接種の4週間後に著者の病院に転院し、抗
間質性肺疾患
MDA5陽性DMRPILDと診断された。
集中治療にもかかわらず、患者は入院10日目に死
亡した。
1778
1780
※BA4-5の
No.25と同一
66歳
の症例につ
き、No.25に
統合
専門家による評価【令和4年12月16日時点】
報告医が
死因等の判断に
至った検査
ワクチンと死亡との
因果関係評価
(評価記号★)
コメント
専門家による評価【令和5年1月20日時点】
評価に用いた報告内容注2
ワクチンと死亡との
因果関係評価
(評価記号★)
コメント
資料番号
症例No
不明
不明
-
-
γ
(コメント無し)
資料1-2-2-1 21620
剖検
不明
不明
-
-
γ
(コメント無し)
資料1-2-2-1 21625
頭部CT
評価不能
有(高血圧の既
往あり。抗血小
板薬を内服され
ていた)
不明
不明
評価不能
不明
-
-
γ
(コメント無し)
資料1-1-2-1 29750
間質性肺疾患
不明
関連あり
不明
-
-
γ
(コメント無し)
資料1-1-2-1 29751
間質性肺疾患
視床出血
脳室穿破
水頭症
注1:各症例の記載は、令和3年2月17日~令和4年11月13日までに、医療機関又は本ワクチンの製造販売業者から副反応疑い報告された内容に基づく。専門家による評価は、特記した場合を除き、令和4年11月13日時点の報告内容に基づき実施。
注2:直近の集計対象期間において新規又は追加報告された症例について、対応する症例Noを記入している。同一症例であっても、報告内容の更新等により医療機関又は製造販売業者から複数回報告される場合がある。同一症例について複数回報告された場合は、評価時点で最後に報告された報告内容に基づき評価している。
注3:2021年3月30日に製造販売業者から厚生労働省に一報。詳細調査の後、4月6日に副反応疑い報告がなされた。
注4:接種医療機関及び搬送先医療機関から同一事例について報告あり。本表の記載内容は、両報告内容に基づく。
注5:接種医療機関及び解剖実施医療機関から同一事例について報告あり。本表の記載内容は、両報告内容に基づく。
注6:接種医療機関及び検視医から同一事例について報告あり。本表の記載内容は、両報告内容に基づく。
注7:接種医療機関及び主治医から同一事例について報告あり。本表の記載内容は、両報告内容に基づく。
注8:搬送先医療機関及び解剖医療機関から同一事例について報告あり。本表の記載内容は、両報告内容に基づく。
注9:主治医及び解剖医療機関から同一事例について報告あり。本表の記載内容は、両報告内容に基づく。
注10:「死因等」の記載は副反応疑い報告書の記載(接種の状況、症状の概要、報告者意見)を総合的に考慮の上、記載。資料1-1-2や資料1-2-2の「症状名(PT)」とは異なることがある。
注11:入院時検査にて、抗CCP抗体高値陽性(142.0U/ml)、RF高値陽性(87IU/ml)、MMP3(111.5ng/ml)であり、関節リウマチに合致する所見を認めた。抗TNF製剤で抗核抗体や抗dsDNA抗体が陽転化する報告があるが、いずれも陰性で、他、抗RNP抗体陰性、抗Sm抗体陰性、抗リン脂質抗体(ループスアンチコアグラント、抗カルジオリピンIgG抗体、抗カルジオリピンβ2GP1抗体)は全て陰性であり、C3 70mg/dl、C4 18mg/dl、CH50 55.0U/mlとほ
ぼ正常範囲でSLE合併などによる血小板減少は考えにくい。IgG 1547mg/dl、IgA 693mg/dl、IgM 70mg/dlであった。ヘパリン使用歴はなく、HIT抗体は陰性であった。PA-IgGが206.0ng/10^7cells(基準値46ng/10^7cells以下)で、血小板表面に結合しているIgG(抗血小板抗体)を多数認めた。自己抗体の中で関節リウマチに関連したもの以外で入院以前に異常値を認めたものはないか、測定記録無しであった。本例ではPA-IgGが206.0ng/10^7cellsで、
血小板表面に結合しているIgG(抗血小板抗体)を多数認めた。長期間安定していた関節リウマチ患者に発生した突然の血小板減少の誘因として、以下考察する。抗血小板抗体は時に関節リウマチで陽転化する場合があるが、免疫グロブリンはいずれもポリクローナルな増加は見られず、関節リウマチの活動性も高くないことを踏まえれば、関節リウマチ自体により体内で抗血小板抗体が陽転化する可能性は低かったと考える。次に、本患者に使用
されていた注射剤(シンポニー(ゴリムマブ)及びミルセラ(エポエチンベータペゴル))においては、両薬剤ともに、頻度不明ながらも血小板減少が報告されている。両薬剤によって血小板減少を誘発した可能性は否定できないが、それが抗血小板抗体による機序であるかどうか不明であり、長期間安全に使用されてきた経緯を踏まえれば、両薬剤によって血小板減少が引き起こされた可能性は低いものと考える。引き続き症例の蓄積が必要であり、
早急な判断はできないが、本例はワクチンの2回目投与直後のタイミングであり、ワクチンによる因果関係は否定できないものと推察され、発症直前(4日前及び25日前)に投与されたワクチンが、致死的な血小板減少を誘発し、その結果、くも膜下出血をきたした原因薬剤として、現時点で最も可能性が高いと考える。
注12:当院受診歴(合計3回)
注13:報告書における死因等の記載が基礎疾患の増悪等とされているものについては、本資料においては、7/21以降「対応するMedDRA PT」は基礎疾患等の名称ではなく、「状態悪化」として整理している。
注14:「血小板減少症を伴う血栓症」が死因として疑われると報告された事例については、「対応するMedDRA PT」には、令和3年10月22日までは、血小板減少に係る症状と血栓症に係る症状の両方を併記。10月22日以降は「血小板減少症を伴う血栓症」と表記。10月22日までに報告された症例においても、10月22日以降の追加報告の際に、死因を「血小板減少症を伴う血栓症」に更新、又は死因に「血小板減少症を伴う血栓症」を追加している。
注15:1件の副反応疑い報告書において、異なる接種回の副反応疑い事例が同時に報告されている場合は、当該報告書における最大接種回数を、当該報告の「接種回数」として記載・集計している。
注16:2か所の搬送先医療機関から同一症例について報告あり。本表の記載内容は、両報告内容に基づく。
276