よむ、つかう、まなぶ。
別紙1○患者申出療養に係る新規技術の科学的評価等について (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000203222_00025.html |
| 出典情報 | 患者申出療養評価会議(第41回 6/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
期に投与された試験となります。最高用量(500mg/kg/day)群では、投与早期(1 週以内)に状態
悪化が認められ、腎臓変性及び筋繊維の変性も認められたため、投与 4、5、7 日又は 11 日に安楽
死させ、500 mg/kg/日群の投与を中止しています。一方、その他すべての群(0、60、100、および
300mg/kg/day)では、いずれの検査項目においても被験薬と関連のある、又は毒性学的に意義の
ある影響は 39 週通じて認められず、24 週以上の長期投与で初めて発現した問題となる事象は認
められませんでした。
図3 反復投与後の血漿中 EPI-589 濃度の推移
EPI-589 血漿中濃度(ng/mL)
Day 7
例数
投与量
(日本人)
要約統計量
投与前
0.25 h
0.5 h
1 h
2 h
3 h
4 h
6 h
8 h
10 h
12 h
24 h
48 h
500 mg
N = 6
算術平均値
64.38
410.1
1191
2105
1427
583.7
273.2
72.55
33.82
31.27
24.92
10.24
BLQ
750 mg
N = 6
算術平均値
114.8
1037
1834
2369
2191
899.7
416.2
107.3
54.52
50.32
44.68
27.78
3.137
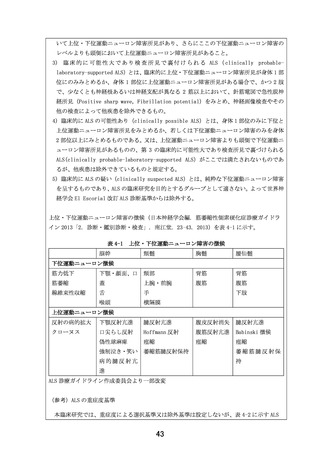
BLQ: 検出下限未満(< 1 ng/mL)
表2 投与 7 日目(1 日 2 回 5 日間の反復投与後)
、単回投与後の血漿中 EPI-589 濃度
剤型
剤型は今後変更予定ですが、新たな剤型については従前同様に経口製剤を予定しており、また本
試験で使用される錠剤と新たな経口製剤の薬物動態比較試験(jRCT2071220047)も実施済です。
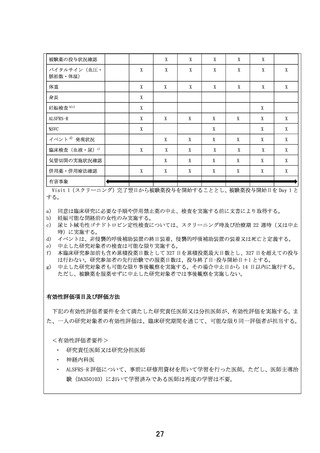
本試験では研究対象者が既に投与を受け、安全性に問題がなく、一定の効果を見込めることがわ
かっている、以前の治験で使用された剤型が用いられます。
10
悪化が認められ、腎臓変性及び筋繊維の変性も認められたため、投与 4、5、7 日又は 11 日に安楽
死させ、500 mg/kg/日群の投与を中止しています。一方、その他すべての群(0、60、100、および
300mg/kg/day)では、いずれの検査項目においても被験薬と関連のある、又は毒性学的に意義の
ある影響は 39 週通じて認められず、24 週以上の長期投与で初めて発現した問題となる事象は認
められませんでした。
図3 反復投与後の血漿中 EPI-589 濃度の推移
EPI-589 血漿中濃度(ng/mL)
Day 7
例数
投与量
(日本人)
要約統計量
投与前
0.25 h
0.5 h
1 h
2 h
3 h
4 h
6 h
8 h
10 h
12 h
24 h
48 h
500 mg
N = 6
算術平均値
64.38
410.1
1191
2105
1427
583.7
273.2
72.55
33.82
31.27
24.92
10.24
BLQ
750 mg
N = 6
算術平均値
114.8
1037
1834
2369
2191
899.7
416.2
107.3
54.52
50.32
44.68
27.78
3.137
BLQ: 検出下限未満(< 1 ng/mL)
表2 投与 7 日目(1 日 2 回 5 日間の反復投与後)
、単回投与後の血漿中 EPI-589 濃度
剤型
剤型は今後変更予定ですが、新たな剤型については従前同様に経口製剤を予定しており、また本
試験で使用される錠剤と新たな経口製剤の薬物動態比較試験(jRCT2071220047)も実施済です。
本試験では研究対象者が既に投与を受け、安全性に問題がなく、一定の効果を見込めることがわ
かっている、以前の治験で使用された剤型が用いられます。
10