よむ、つかう、まなぶ。
別紙1○患者申出療養に係る新規技術の科学的評価等について (30 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000203222_00025.html |
| 出典情報 | 患者申出療養評価会議(第41回 6/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
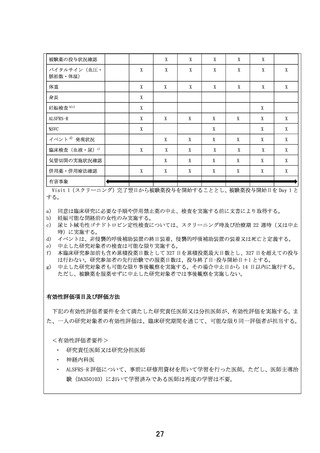
等を他科・他院の担当医に確認し、症例報告書に有害事象、併用治療等の情報を記録する。
リルゾールの使用状況
リルゾールの使用状況については投与開始日及び投与終了日(臨床研究中に終了した場合は年月日
又は「継続」)を調査し、症例報告書に記録する。リルゾールを投与中止した場合は、中止理由を記
録する。
気管切開の実施状況
気管切開の実施状況(実施の有無、及び実施日)を症例報告書に記録する。
被験薬の投与状況
被験薬投与期間中 Visit ごと(又は中止時)に被験薬の服薬状況を調査し、症例報告書に被験薬の
処方日、服薬開始日、服薬終了日、1 日投与量、処方錠数、返却錠数及び紛失錠数を記録する。また、
被験薬を休薬した場合は、休薬開始日及び終了日、休薬理由を症例報告書に記録する。服薬中止に関
しては、服薬中止の有無及び中止理由を記録する。
併用薬・併用療法
併用治療の禁止規定の遵守を研究対象者に指導する。また、以下に基づいて併用治療を調査する。
1)
併用薬
同意取得時から事後観察期完了時、又は中止時(事後観察期後に追跡調査が必要な場合は、追跡
調査完了)までに使用した全ての薬剤について、以下の項目を調査し、症例報告書に記録する。た
だし、各種検査・診断のために使用した薬剤、処置薬、消毒薬、麻酔薬、輸液、溶解又はフラッシ
ュ用の生理食塩水は除くが、有害事象の処置である場合及び有害事象との因果関係が否定できない
場合は症例報告書へ記録する。
薬剤名、投与開始日(
「同意取得前から継続」又は同意取得時以降の場合は年月日)
、投与終了日
(臨床研究中に終了した場合は年月日又は「継続」
)、投与経路、投与理由(原疾患、合併症、有害
事象、その他)
2)
併用療法
同意取得時から事後観察期完了時、又は中止時(事後観察期後に追跡調査が必要な場合は、追跡調
査完了)までに施行された全ての治療法について、療法名、治療理由、治療開始日(
「同意取得前か
ら継続」又は同意取得時以降の場合は年月日)、及び治療終了日(臨床研究中に終了した場合は年月
日又は「継続」
)を調査し、症例報告書に記録する。
30
リルゾールの使用状況
リルゾールの使用状況については投与開始日及び投与終了日(臨床研究中に終了した場合は年月日
又は「継続」)を調査し、症例報告書に記録する。リルゾールを投与中止した場合は、中止理由を記
録する。
気管切開の実施状況
気管切開の実施状況(実施の有無、及び実施日)を症例報告書に記録する。
被験薬の投与状況
被験薬投与期間中 Visit ごと(又は中止時)に被験薬の服薬状況を調査し、症例報告書に被験薬の
処方日、服薬開始日、服薬終了日、1 日投与量、処方錠数、返却錠数及び紛失錠数を記録する。また、
被験薬を休薬した場合は、休薬開始日及び終了日、休薬理由を症例報告書に記録する。服薬中止に関
しては、服薬中止の有無及び中止理由を記録する。
併用薬・併用療法
併用治療の禁止規定の遵守を研究対象者に指導する。また、以下に基づいて併用治療を調査する。
1)
併用薬
同意取得時から事後観察期完了時、又は中止時(事後観察期後に追跡調査が必要な場合は、追跡
調査完了)までに使用した全ての薬剤について、以下の項目を調査し、症例報告書に記録する。た
だし、各種検査・診断のために使用した薬剤、処置薬、消毒薬、麻酔薬、輸液、溶解又はフラッシ
ュ用の生理食塩水は除くが、有害事象の処置である場合及び有害事象との因果関係が否定できない
場合は症例報告書へ記録する。
薬剤名、投与開始日(
「同意取得前から継続」又は同意取得時以降の場合は年月日)
、投与終了日
(臨床研究中に終了した場合は年月日又は「継続」
)、投与経路、投与理由(原疾患、合併症、有害
事象、その他)
2)
併用療法
同意取得時から事後観察期完了時、又は中止時(事後観察期後に追跡調査が必要な場合は、追跡調
査完了)までに施行された全ての治療法について、療法名、治療理由、治療開始日(
「同意取得前か
ら継続」又は同意取得時以降の場合は年月日)、及び治療終了日(臨床研究中に終了した場合は年月
日又は「継続」
)を調査し、症例報告書に記録する。
30