よむ、つかう、まなぶ。
別紙1○患者申出療養に係る新規技術の科学的評価等について (28 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000203222_00025.html |
| 出典情報 | 患者申出療養評価会議(第41回 6/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
ALSFRS-R
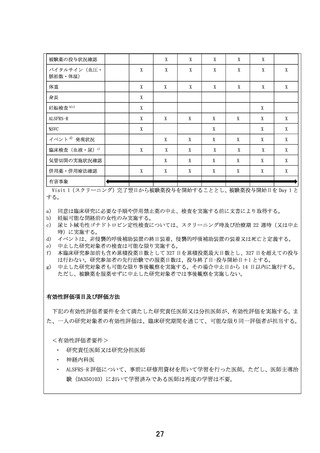
研究責任医師又は研究分担医師は、表 9-1 に従って、日常生活動作及び呼吸機能の状態等を調査
し、「ALSFRS-R 評価の手引き」に従って、ALSFRS-R(Kollewe K et al. ALSFRS-R score and its
ratio: A useful predictor for ALS-progression. J Neurol. 275: 69–73. 2008)を評価する。ま
た、評価実施日、評価者、回答者及び各 Item の点数を症例報告書に記録する。
%SVC
%SVC を測定し、測定日及び測定結果を症例報告書に記録する。なお、可能な限り同一評価者が計測
することとする。
イベント
研究責任医師又は研究分担医師は、表 9-1 に従って、原疾患の進行による「非侵襲的呼吸補助装置
の終日装着」、「侵襲的呼吸補助装置の装着」又は「死亡」をイベントと定義し、その発現状況を調
査する。ただし、「死亡」については、原因に関わらず全てをイベントとする。イベントが発現した
場合は、イベント名及びイベント発生日を症例報告書に記録する。イベント発生日は、非侵襲的呼吸
補助装置の終日装着(22 時間以上の装着)が開始された日、侵襲的呼吸補助装置の装着が開始された
日、又は死亡日とする。
なお、本臨床研究では、不慮の事故、偶発的な合併症等により発生した「非侵襲的呼吸補助装置の
終日装着」又は「侵襲的呼吸補助装置の装着」はイベントとして取り扱わないこととし、当該事象の
内容、発生日、及び原疾患の進行によらないと判断した理由を症例報告書に記録する。
また、可能な限り、同一評価者が同一研究対象者のイベント発生を評価することとする。
安全性評価のための調査項目及び調査方法
臨床検査
研究責任医師又は研究分担医師は、表 9-1 に従って、以下の項目についての臨床検査を行い、検体
採取日(血液及び尿)及び検査結果を症例報告書に記録する。
測定項目:
・血液学的検査:白血球数、赤血球数、ヘモグロビン、ヘマトクリット、血小板数、白血球分
画(好中球、好酸球、好塩基球、単球、リンパ球)
、平均赤血球容積、平均赤血球ヘモグロビン
量、平均赤血球ヘモグロビン濃度
・血液生化学検査:総蛋白、アルブミン、総ビリルビン、AST、ALT、ALP、γ-GTP、CK、CK 分
28
研究責任医師又は研究分担医師は、表 9-1 に従って、日常生活動作及び呼吸機能の状態等を調査
し、「ALSFRS-R 評価の手引き」に従って、ALSFRS-R(Kollewe K et al. ALSFRS-R score and its
ratio: A useful predictor for ALS-progression. J Neurol. 275: 69–73. 2008)を評価する。ま
た、評価実施日、評価者、回答者及び各 Item の点数を症例報告書に記録する。
%SVC
%SVC を測定し、測定日及び測定結果を症例報告書に記録する。なお、可能な限り同一評価者が計測
することとする。
イベント
研究責任医師又は研究分担医師は、表 9-1 に従って、原疾患の進行による「非侵襲的呼吸補助装置
の終日装着」、「侵襲的呼吸補助装置の装着」又は「死亡」をイベントと定義し、その発現状況を調
査する。ただし、「死亡」については、原因に関わらず全てをイベントとする。イベントが発現した
場合は、イベント名及びイベント発生日を症例報告書に記録する。イベント発生日は、非侵襲的呼吸
補助装置の終日装着(22 時間以上の装着)が開始された日、侵襲的呼吸補助装置の装着が開始された
日、又は死亡日とする。
なお、本臨床研究では、不慮の事故、偶発的な合併症等により発生した「非侵襲的呼吸補助装置の
終日装着」又は「侵襲的呼吸補助装置の装着」はイベントとして取り扱わないこととし、当該事象の
内容、発生日、及び原疾患の進行によらないと判断した理由を症例報告書に記録する。
また、可能な限り、同一評価者が同一研究対象者のイベント発生を評価することとする。
安全性評価のための調査項目及び調査方法
臨床検査
研究責任医師又は研究分担医師は、表 9-1 に従って、以下の項目についての臨床検査を行い、検体
採取日(血液及び尿)及び検査結果を症例報告書に記録する。
測定項目:
・血液学的検査:白血球数、赤血球数、ヘモグロビン、ヘマトクリット、血小板数、白血球分
画(好中球、好酸球、好塩基球、単球、リンパ球)
、平均赤血球容積、平均赤血球ヘモグロビン
量、平均赤血球ヘモグロビン濃度
・血液生化学検査:総蛋白、アルブミン、総ビリルビン、AST、ALT、ALP、γ-GTP、CK、CK 分
28