よむ、つかう、まなぶ。
【資料3-1】新型コロナワクチン(コミナティ筋注5~ 11 歳用)の承認について(医薬・生活衛生局の説明資料) (14 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_24538.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第7回 3/18)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
治験薬 2 回目接種 1 カ月後の中和抗体価は表 4 のとおりであり、GMR について、事前に設定された
成功基準(両側 95%CI の下限値が 0.67 を上回り、点推定値は 0.8 以上)が達成された。
表 4 中和抗体価(評価可能免疫原性集団)
C4591007 試験(5~11 歳)
C4591001 試験(16~25 歳)
本薬 10 µg
プラセボ
本薬 30 µg
プラセボ
GMTa)
GMT a)
GMT a)
GMT a)
N
N
N
N
[両側 95%CI]
[両側 95%CI]
[両側 95%CI]
[両側 95%CI]
1197.6
10.7
1146.5
10.0
264
130
253
45
[1106.1, 1296.6]
[9.7, 11.8]
[1045.5, 1257.2]
[10.0, 10.0]
N=解析対象例数
a)抗体価が LLOQ 未満の場合、解析には 0.5×LLOQ の値が用いられた。
GMR
[両側 95%CI]
(5~11 歳本薬群/
16~25 歳本薬群)
1.04[0.93, 1.18]
また、治験薬 2 回目接種 1 カ月後の中和抗体応答率は表 5 のとおりであり、抗体応答率の差につい
て、事前に設定された成功基準(両側 95%CI の下限値が-10%を上回る)が達成された。
表5
C4591007 試験(5~11 歳)
本薬 10 µg
プラセボ
%(n/N)
%(n/N)
中和抗体応答率(評価可能免疫原性集団)
C4591001 試験(16~25 歳)
本薬 30 µg
プラセボ
%(n/N)
%(n/N)
抗体応答率の差[両側 95%CI]a)
(5~11 歳本薬群-16~25 歳本薬群)
99.2%(262/264 例) 1.5%(2/130 例) 99.2%(251/253 例)
0%(0/45 例)
0.0%[-2.0, 2.2]
N=解析対象例数、n=抗体価がベースライン値(ベースライン値が LLOQ 未満の場合は LLOQ 値)から 4 倍以上に上昇した例数
a)Miettinen and Nurminen 法
安全性について、有害事象の重症度評価に用いた評価尺度及び各観察期間は、第Ⅰ相パートと同様と
された(7.1.1 参照)。
安全性解析対象集団における治験薬 2 回目接種からデータカットオフ日(2021 年 9 月 6 日)までの観
察期間の中央値は、2.3 カ月(範囲 0.0~2.5 カ月)であった。
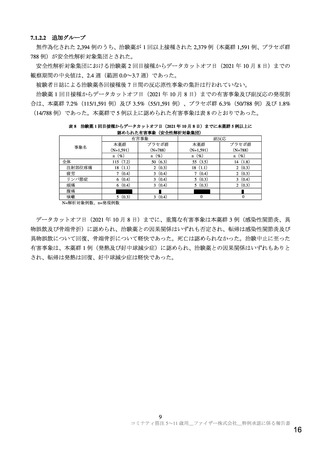
治験薬各回接種後 7 日間に認められた反応原性事象は表 6 のとおりであった。
7
コミナティ筋注 5~11 歳用_ファイザー株式会社_特例承認に係る報告書
14
成功基準(両側 95%CI の下限値が 0.67 を上回り、点推定値は 0.8 以上)が達成された。
表 4 中和抗体価(評価可能免疫原性集団)
C4591007 試験(5~11 歳)
C4591001 試験(16~25 歳)
本薬 10 µg
プラセボ
本薬 30 µg
プラセボ
GMTa)
GMT a)
GMT a)
GMT a)
N
N
N
N
[両側 95%CI]
[両側 95%CI]
[両側 95%CI]
[両側 95%CI]
1197.6
10.7
1146.5
10.0
264
130
253
45
[1106.1, 1296.6]
[9.7, 11.8]
[1045.5, 1257.2]
[10.0, 10.0]
N=解析対象例数
a)抗体価が LLOQ 未満の場合、解析には 0.5×LLOQ の値が用いられた。
GMR
[両側 95%CI]
(5~11 歳本薬群/
16~25 歳本薬群)
1.04[0.93, 1.18]
また、治験薬 2 回目接種 1 カ月後の中和抗体応答率は表 5 のとおりであり、抗体応答率の差につい
て、事前に設定された成功基準(両側 95%CI の下限値が-10%を上回る)が達成された。
表5
C4591007 試験(5~11 歳)
本薬 10 µg
プラセボ
%(n/N)
%(n/N)
中和抗体応答率(評価可能免疫原性集団)
C4591001 試験(16~25 歳)
本薬 30 µg
プラセボ
%(n/N)
%(n/N)
抗体応答率の差[両側 95%CI]a)
(5~11 歳本薬群-16~25 歳本薬群)
99.2%(262/264 例) 1.5%(2/130 例) 99.2%(251/253 例)
0%(0/45 例)
0.0%[-2.0, 2.2]
N=解析対象例数、n=抗体価がベースライン値(ベースライン値が LLOQ 未満の場合は LLOQ 値)から 4 倍以上に上昇した例数
a)Miettinen and Nurminen 法
安全性について、有害事象の重症度評価に用いた評価尺度及び各観察期間は、第Ⅰ相パートと同様と
された(7.1.1 参照)。
安全性解析対象集団における治験薬 2 回目接種からデータカットオフ日(2021 年 9 月 6 日)までの観
察期間の中央値は、2.3 カ月(範囲 0.0~2.5 カ月)であった。
治験薬各回接種後 7 日間に認められた反応原性事象は表 6 のとおりであった。
7
コミナティ筋注 5~11 歳用_ファイザー株式会社_特例承認に係る報告書
14