よむ、つかう、まなぶ。
【資料3-1】新型コロナワクチン(コミナティ筋注5~ 11 歳用)の承認について(医薬・生活衛生局の説明資料) (21 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_24538.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第7回 3/18)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
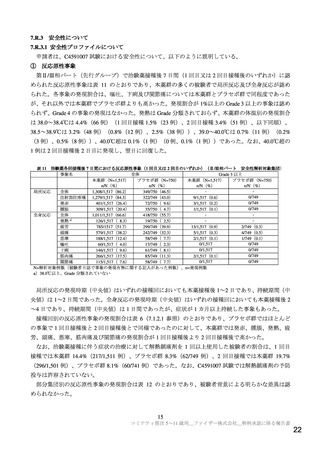
16/736 例)集積された。治験薬接種前から 2 回目接種後 7 日以前の SARS-CoV-2 感染歴がない集団(本
薬群 1,305 例、プラセボ群 663 例)における VE[両側 95%CI]は 90.7%[67.4, 98.3]であった。SARSCoV-2 感染歴がある被験者で COVID-19 確定例は認められなかった。COVID-19 確定例において、本薬
群及びプラセボ群のいずれでも重症例15)は報告されず、MIS-C の発現も報告されなかった。
以上、C4591007 試験の第Ⅱ/Ⅲ相パートの結果より、C4591001 試験の 16~25 歳の集団との免疫ブリ
ッジングに係る成功基準が達成されたこと、予備的なデータであるがデルタ株流行時期を含む期間に実
施した本試験で高い VE が確認され、デルタ株に対する中和抗体価の上昇も確認されたことから、
C4591001 試験で確認されている本薬の COVID-19 発症予防効果を踏まえると、5~11 歳の小児における
本薬の一定の有効性は期待できると考えられる。
なお、現時点で得られている 5~11 歳における免疫原性データは本薬 2 回目接種後 1 カ月時点のデー
タのみであるが、C4591007 試験では本薬 2 回目接種後 6 カ月時点等においても、今後免疫原性データを
取得する計画である。
機構は、以下のように考える。
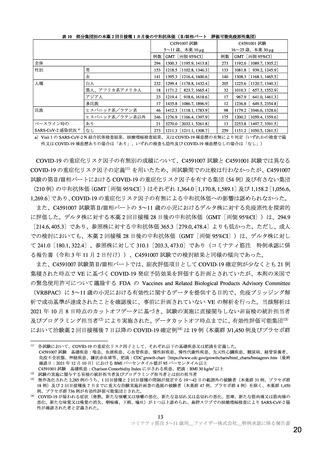
C4591007 試験の第Ⅱ/Ⅲ相パートと C4591001 試験の 16~25 歳の集団の免疫原性データを比較するこ
とについて、両集団の一部の被験者背景の分布は異なっていたものの(表 9)、C4591001 試験で本薬の
高い COVID-19 発症予防効果及び中和抗体価の上昇が確認され、部分集団解析でも被験者背景を問わず
高い COVID-19 発症予防効果が確認されていることを踏まえると(コミナティ筋注
特例承認に係る報
告書(令和 3 年 2 月 8 日付け)、N Engl J Med 2021; 384: 1576-7)、被験者背景の違いにより臨床的に意
味のある免疫応答の違いが生じる可能性は低く、両集団の免疫原性データの比較は可能と判断した。
C4591007 試験の第Ⅱ/Ⅲ相パートにおいて、本薬 2 回目接種後 1 カ月時点の中和抗体価の GMR 及び
抗体応答率の差について、免疫ブリッジングに係る成功基準が達成されたこと、中和抗体価の部分集団
解析でも被験者背景による大きな差異は認められなかったこと等から、C4591001 試験で確認されている
本薬の COVID-19 発症予防効果を踏まえると、5~11 歳の小児における本薬の一定の有効性は期待でき
ると判断する。ただし、本申請で提出された免疫原性データは本薬 2 回目接種後 1 カ月時点までのデー
タであり、5~11 歳の小児における本薬接種後の時間経過に伴う中和抗体価の推移は不明である。
C4591001 試験等で本薬接種後の中和抗体価が時間経過と共に低下することが確認されており(コミナテ
ィ筋注
特例承認に係る報告書(令和 3 年 11 月 2 日付け))、5~11 歳の小児における免疫原性データ
の推移については引き続き情報収集し、得られた情報に基づき対応を検討する必要がある。また、今後
も変異株の発現状況及び流行状況に注視し、変異株に対する本薬の有効性や免疫原性について情報収集
し、適宜状況に応じた対応を検討する必要がある。
15)
以下の一つ以上の状態が認められる COVID-19 確定例:重度全身性疾患を示唆する安静時の臨床的徴候(呼吸数増加、心拍数増加、
SpO2 低下又は PaO2/ FiO2 低下)、呼吸不全(高流量酸素療法、非侵襲的換気療法、機械換気又は体外式膜型人工肺による治療を要
する)、ショック又は心不全、急性腎不全、肝不全又は神経系機能障害、集中治療室への入室、死亡
14
コミナティ筋注 5~11 歳用_ファイザー株式会社_特例承認に係る報告書
21
薬群 1,305 例、プラセボ群 663 例)における VE[両側 95%CI]は 90.7%[67.4, 98.3]であった。SARSCoV-2 感染歴がある被験者で COVID-19 確定例は認められなかった。COVID-19 確定例において、本薬
群及びプラセボ群のいずれでも重症例15)は報告されず、MIS-C の発現も報告されなかった。
以上、C4591007 試験の第Ⅱ/Ⅲ相パートの結果より、C4591001 試験の 16~25 歳の集団との免疫ブリ
ッジングに係る成功基準が達成されたこと、予備的なデータであるがデルタ株流行時期を含む期間に実
施した本試験で高い VE が確認され、デルタ株に対する中和抗体価の上昇も確認されたことから、
C4591001 試験で確認されている本薬の COVID-19 発症予防効果を踏まえると、5~11 歳の小児における
本薬の一定の有効性は期待できると考えられる。
なお、現時点で得られている 5~11 歳における免疫原性データは本薬 2 回目接種後 1 カ月時点のデー
タのみであるが、C4591007 試験では本薬 2 回目接種後 6 カ月時点等においても、今後免疫原性データを
取得する計画である。
機構は、以下のように考える。
C4591007 試験の第Ⅱ/Ⅲ相パートと C4591001 試験の 16~25 歳の集団の免疫原性データを比較するこ
とについて、両集団の一部の被験者背景の分布は異なっていたものの(表 9)、C4591001 試験で本薬の
高い COVID-19 発症予防効果及び中和抗体価の上昇が確認され、部分集団解析でも被験者背景を問わず
高い COVID-19 発症予防効果が確認されていることを踏まえると(コミナティ筋注
特例承認に係る報
告書(令和 3 年 2 月 8 日付け)、N Engl J Med 2021; 384: 1576-7)、被験者背景の違いにより臨床的に意
味のある免疫応答の違いが生じる可能性は低く、両集団の免疫原性データの比較は可能と判断した。
C4591007 試験の第Ⅱ/Ⅲ相パートにおいて、本薬 2 回目接種後 1 カ月時点の中和抗体価の GMR 及び
抗体応答率の差について、免疫ブリッジングに係る成功基準が達成されたこと、中和抗体価の部分集団
解析でも被験者背景による大きな差異は認められなかったこと等から、C4591001 試験で確認されている
本薬の COVID-19 発症予防効果を踏まえると、5~11 歳の小児における本薬の一定の有効性は期待でき
ると判断する。ただし、本申請で提出された免疫原性データは本薬 2 回目接種後 1 カ月時点までのデー
タであり、5~11 歳の小児における本薬接種後の時間経過に伴う中和抗体価の推移は不明である。
C4591001 試験等で本薬接種後の中和抗体価が時間経過と共に低下することが確認されており(コミナテ
ィ筋注
特例承認に係る報告書(令和 3 年 11 月 2 日付け))、5~11 歳の小児における免疫原性データ
の推移については引き続き情報収集し、得られた情報に基づき対応を検討する必要がある。また、今後
も変異株の発現状況及び流行状況に注視し、変異株に対する本薬の有効性や免疫原性について情報収集
し、適宜状況に応じた対応を検討する必要がある。
15)
以下の一つ以上の状態が認められる COVID-19 確定例:重度全身性疾患を示唆する安静時の臨床的徴候(呼吸数増加、心拍数増加、
SpO2 低下又は PaO2/ FiO2 低下)、呼吸不全(高流量酸素療法、非侵襲的換気療法、機械換気又は体外式膜型人工肺による治療を要
する)、ショック又は心不全、急性腎不全、肝不全又は神経系機能障害、集中治療室への入室、死亡
14
コミナティ筋注 5~11 歳用_ファイザー株式会社_特例承認に係る報告書
21