よむ、つかう、まなぶ。
【資料3-1】新型コロナワクチン(コミナティ筋注5~ 11 歳用)の承認について(医薬・生活衛生局の説明資料) (19 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_24538.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第7回 3/18)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
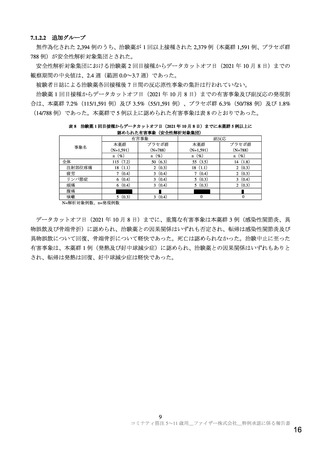
比較するために 25 歳を上限として設定した。両試験の実施国は一部異なるが(C4591007 試験は米国、
フィンランド、ポーランド及びスペイン、C4591001 試験は米国、ドイツ、トルコ、ブラジル、アルゼン
チン及び南アフリカ)、被験者の主な選択・除外基準は年齢に関する基準を除き同様であった。また、
両試験の SARS-CoV-2 の感染歴のない被験者から得られた血清サンプルを用いて、同一の方法により同
時に中和抗体価を測定することで、両試験間の免疫原性データの比較は可能と考えた。
C4591007 試験の第Ⅱ/Ⅲ相パートを実施し、主要評価項目である本薬 2 回目接種後 1 カ月時点の中和
抗体価を指標とする C4591001 試験の 16~25 歳の集団との比較の結果、GMR 及び抗体応答率の差につ
いて、いずれも事前に設定した成功基準が達成された(7.1.2.1 参照)。
C4591007 試験の第Ⅱ/Ⅲ相パートと比較対照の C4591001 試験の 16~25 歳の集団の評価可能免疫原性
集団について、被験者背景は表 9 のとおりであった。
表9
性別
人種
被験者背景の比較(Ⅱ/Ⅲ相パート
男
女
白人
黒人、アフリカ系アメリカ人
評価可能免疫原性集団)
C4591007 試験
5~11 歳、本薬 10 µg
N=294
n(%)
153(52.0)
141(48.0)
232(78.9)
18( 6.1)
C4591001 試験
16~25 歳、本薬 30 µg
N=273
n(%)
133(48.7)
140(51.3)
205(75.1)
32(11.7)
アジア人
23( 7.8)
17( 6.2)
多民族
17( 5.8)
12( 4.4)
その他 a)・不明
4( 1.3)
7( 2.6)
民族
ヒスパニック系/ラテン系
46(15.6)
98(35.9)
ヒスパニック系/ラテン系以外
246(83.7)
175(64.1)
0
不明
2( 0.7)
肥満 b)
あり
25( 8.5)
44(16.1)
なし
269(91.5)
229(83.9)
ベースライン時の
あり
21( 7.1)
13( 4.8)
SARS-CoV-2 感染状況 c) なし
273(92.9)
259(94.9)
0
不明
1( 0.4)
N=解析対象例数、n=該当する例数
a)アメリカ系インディアン、アラスカ原住民、ハワイ原住民、その他太平洋諸国民
b)C4591007 試験:BMI パーセンタイル値が 95 パーセンタイル以上、C4591001 試験:BMI 30 kg/m2 以上
c)Visit 1 の SARS-CoV-2 N 結合抗体検査結果、核酸増幅検査結果、又は COVID-19 罹患歴の有無により判定(いずれかの検
査で陽性又は COVID-19 罹患歴ありの場合は「あり」、いずれの検査も陰性及び COVID-19 罹患歴なしの場合は「なし」)
また、部分集団別の本薬 2 回目接種 1 カ月後の中和抗体価は表 10 のとおりであった。また、抗体応答
率はいずれの集団及びいずれの年齢層でも 98.6~100%と高かった。一部の部分集団では例数が限られて
おり、中和抗体価の結果の解釈には注意が必要であるが、性別、人種及び民族によらず GMT は概ね同
様であった。ベースライン時の SARS-CoV-2 感染状況別の中和抗体価は「あり」集団で「なし」集団よ
りも高かったが、いずれの部分集団でも抗体応答率は高かった。
12
コミナティ筋注 5~11 歳用_ファイザー株式会社_特例承認に係る報告書
19
フィンランド、ポーランド及びスペイン、C4591001 試験は米国、ドイツ、トルコ、ブラジル、アルゼン
チン及び南アフリカ)、被験者の主な選択・除外基準は年齢に関する基準を除き同様であった。また、
両試験の SARS-CoV-2 の感染歴のない被験者から得られた血清サンプルを用いて、同一の方法により同
時に中和抗体価を測定することで、両試験間の免疫原性データの比較は可能と考えた。
C4591007 試験の第Ⅱ/Ⅲ相パートを実施し、主要評価項目である本薬 2 回目接種後 1 カ月時点の中和
抗体価を指標とする C4591001 試験の 16~25 歳の集団との比較の結果、GMR 及び抗体応答率の差につ
いて、いずれも事前に設定した成功基準が達成された(7.1.2.1 参照)。
C4591007 試験の第Ⅱ/Ⅲ相パートと比較対照の C4591001 試験の 16~25 歳の集団の評価可能免疫原性
集団について、被験者背景は表 9 のとおりであった。
表9
性別
人種
被験者背景の比較(Ⅱ/Ⅲ相パート
男
女
白人
黒人、アフリカ系アメリカ人
評価可能免疫原性集団)
C4591007 試験
5~11 歳、本薬 10 µg
N=294
n(%)
153(52.0)
141(48.0)
232(78.9)
18( 6.1)
C4591001 試験
16~25 歳、本薬 30 µg
N=273
n(%)
133(48.7)
140(51.3)
205(75.1)
32(11.7)
アジア人
23( 7.8)
17( 6.2)
多民族
17( 5.8)
12( 4.4)
その他 a)・不明
4( 1.3)
7( 2.6)
民族
ヒスパニック系/ラテン系
46(15.6)
98(35.9)
ヒスパニック系/ラテン系以外
246(83.7)
175(64.1)
0
不明
2( 0.7)
肥満 b)
あり
25( 8.5)
44(16.1)
なし
269(91.5)
229(83.9)
ベースライン時の
あり
21( 7.1)
13( 4.8)
SARS-CoV-2 感染状況 c) なし
273(92.9)
259(94.9)
0
不明
1( 0.4)
N=解析対象例数、n=該当する例数
a)アメリカ系インディアン、アラスカ原住民、ハワイ原住民、その他太平洋諸国民
b)C4591007 試験:BMI パーセンタイル値が 95 パーセンタイル以上、C4591001 試験:BMI 30 kg/m2 以上
c)Visit 1 の SARS-CoV-2 N 結合抗体検査結果、核酸増幅検査結果、又は COVID-19 罹患歴の有無により判定(いずれかの検
査で陽性又は COVID-19 罹患歴ありの場合は「あり」、いずれの検査も陰性及び COVID-19 罹患歴なしの場合は「なし」)
また、部分集団別の本薬 2 回目接種 1 カ月後の中和抗体価は表 10 のとおりであった。また、抗体応答
率はいずれの集団及びいずれの年齢層でも 98.6~100%と高かった。一部の部分集団では例数が限られて
おり、中和抗体価の結果の解釈には注意が必要であるが、性別、人種及び民族によらず GMT は概ね同
様であった。ベースライン時の SARS-CoV-2 感染状況別の中和抗体価は「あり」集団で「なし」集団よ
りも高かったが、いずれの部分集団でも抗体応答率は高かった。
12
コミナティ筋注 5~11 歳用_ファイザー株式会社_特例承認に係る報告書
19