よむ、つかう、まなぶ。
【資料3-1】新型コロナワクチン(コミナティ筋注5~ 11 歳用)の承認について(医薬・生活衛生局の説明資料) (16 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_24538.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第7回 3/18)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
7.1.2.2
追加グループ
無作為化された 2,394 例のうち、治験薬が 1 回以上接種された 2,379 例(本薬群 1,591 例、プラセボ群
788 例)が安全性解析対象集団とされた。
安全性解析対象集団における治験薬 2 回目接種からデータカットオフ日(2021 年 10 月 8 日)までの
観察期間の中央値は、2.4 週(範囲 0.0~3.7 週)であった。
被験者日誌による治験薬各回接種後 7 日間の反応原性事象の集計は行われていない。
治験薬 1 回目接種からデータカットオフ日(2021 年 10 月 8 日)までの有害事象及び副反応の発現割
合は、本薬群 7.2%(115/1,591 例)及び 3.5%(55/1,591 例)、プラセボ群 6.3%(50/788 例)及び 1.8%
(14/788 例)であった。本薬群で 5 例以上に認められた有害事象は表 8 のとおりであった。
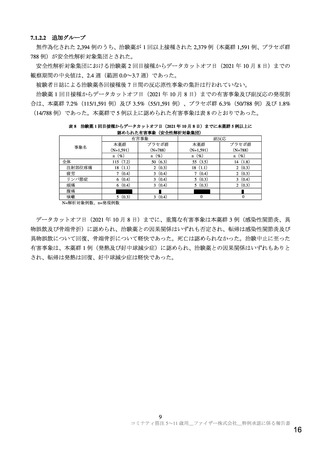
表8
治験薬 1 回目接種からデータカットオフ日(2021 年 10 月 8 日)までに本薬群 5 例以上に
事象名
認められた有害事象(安全性解析対象集団)
有害事象
副反応
本薬群
プラセボ群
本薬群
プラセボ群
(N=1,591)
(N=788)
(N=1,591)
(N=788)
n(%)
n(%)
n(%)
n(%)
115(7.2)
50(6.3)
55(3.5)
14(1.8)
18(1.1)
2(0.3)
18(1.1)
2(0.3)
7(0.4)
3(0.4)
7(0.4)
2(0.3)
6(0.4)
3(0.4)
5(0.3)
3(0.4)
6(0.4)
3(0.4)
5(0.3)
2(0.3)
全体
注射部位疼痛
疲労
リンパ節症
頭痛
腹痛
咳嗽
5(0.3)
N=解析対象例数、n=発現例数
3(0.4)
0
0
データカットオフ日(2021 年 10 月 8 日)までに、重篤な有害事象は本薬群 3 例(感染性関節炎、異
物誤飲及び骨端骨折)に認められ、治験薬との因果関係はいずれも否定され、転帰は感染性関節炎及び
異物誤飲について回復、骨端骨折について軽快であった。死亡は認められなかった。治験中止に至った
有害事象は、本薬群 1 例(発熱及び好中球減少症)に認められ、治験薬との因果関係はいずれもありと
され、転帰は発熱は回復、好中球減少症は軽快であった。
9
コミナティ筋注 5~11 歳用_ファイザー株式会社_特例承認に係る報告書
16
追加グループ
無作為化された 2,394 例のうち、治験薬が 1 回以上接種された 2,379 例(本薬群 1,591 例、プラセボ群
788 例)が安全性解析対象集団とされた。
安全性解析対象集団における治験薬 2 回目接種からデータカットオフ日(2021 年 10 月 8 日)までの
観察期間の中央値は、2.4 週(範囲 0.0~3.7 週)であった。
被験者日誌による治験薬各回接種後 7 日間の反応原性事象の集計は行われていない。
治験薬 1 回目接種からデータカットオフ日(2021 年 10 月 8 日)までの有害事象及び副反応の発現割
合は、本薬群 7.2%(115/1,591 例)及び 3.5%(55/1,591 例)、プラセボ群 6.3%(50/788 例)及び 1.8%
(14/788 例)であった。本薬群で 5 例以上に認められた有害事象は表 8 のとおりであった。
表8
治験薬 1 回目接種からデータカットオフ日(2021 年 10 月 8 日)までに本薬群 5 例以上に
事象名
認められた有害事象(安全性解析対象集団)
有害事象
副反応
本薬群
プラセボ群
本薬群
プラセボ群
(N=1,591)
(N=788)
(N=1,591)
(N=788)
n(%)
n(%)
n(%)
n(%)
115(7.2)
50(6.3)
55(3.5)
14(1.8)
18(1.1)
2(0.3)
18(1.1)
2(0.3)
7(0.4)
3(0.4)
7(0.4)
2(0.3)
6(0.4)
3(0.4)
5(0.3)
3(0.4)
6(0.4)
3(0.4)
5(0.3)
2(0.3)
全体
注射部位疼痛
疲労
リンパ節症
頭痛
腹痛
咳嗽
5(0.3)
N=解析対象例数、n=発現例数
3(0.4)
0
0
データカットオフ日(2021 年 10 月 8 日)までに、重篤な有害事象は本薬群 3 例(感染性関節炎、異
物誤飲及び骨端骨折)に認められ、治験薬との因果関係はいずれも否定され、転帰は感染性関節炎及び
異物誤飲について回復、骨端骨折について軽快であった。死亡は認められなかった。治験中止に至った
有害事象は、本薬群 1 例(発熱及び好中球減少症)に認められ、治験薬との因果関係はいずれもありと
され、転帰は発熱は回復、好中球減少症は軽快であった。
9
コミナティ筋注 5~11 歳用_ファイザー株式会社_特例承認に係る報告書
16