よむ、つかう、まなぶ。
資料2-1:前回部会における主な指摘事項への対応(臨床研究中核病院の承認要件見直しについて) (12 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第38回 11/28)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
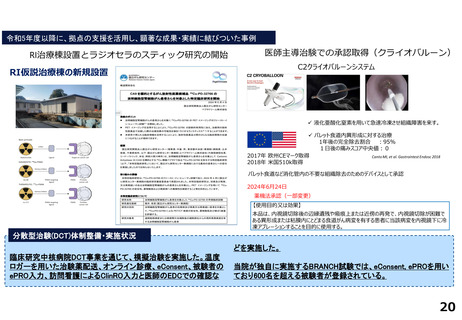
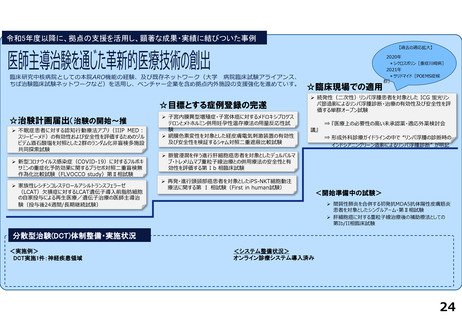
令和5年度以降に、拠点の支援を活用し、顕著な成果・実績に結びついた事例
1.企業と連携し、薬事承認申請に向けて大きく進捗した課題
常染色体優性多発性嚢胞腎(ADPKD)患者の肝嚢胞に対する球状塞栓物質による治療法開発
巨大肝嚢胞を有する常染色体優性多発性嚢胞腎患者あるいは多発性肝嚢胞患者に対して球状塞栓物質
(エンボスフィア)を用いた頸動脈的塞栓(TAE)治療の有用性と安全性を検討することを目的とし、医師
主導治験を平成30年1月に終了済みである。令和6年8月に薬事承認申請する予定である。
2.先進医療Bの試験
食道表在癌に対するアルゴンプラズマ併用高周波凝固焼灼療法の有効性及び安全性を検討する臨床試験
切除が不可能な食道表在癌を対象に、アルゴンプラズマ併用高周波凝固焼灼療法による有効性と安全性を
検討することを目的としている。令和5年3月に本院の認定臨床研究審査委員会で承認され、令和6年4月に
先進医療会議で承認された。令和6年5月、先進医療Bとして告示されたのを受けて試験を開始した。
分散型治験(DCT)体制整備・実施状況
<実施例>
・遠隔でのパーソナル・ヘルス・レコード (PHR) 取得
① 高血圧患者を対象としたAppCare-HT試験
② 慢性心不全患者を対象としたAppCare-HF試験
<システム整備状況>
オンライン診療・DCTツール: MiROHA、Viedoc導入済み
12
1.企業と連携し、薬事承認申請に向けて大きく進捗した課題
常染色体優性多発性嚢胞腎(ADPKD)患者の肝嚢胞に対する球状塞栓物質による治療法開発
巨大肝嚢胞を有する常染色体優性多発性嚢胞腎患者あるいは多発性肝嚢胞患者に対して球状塞栓物質
(エンボスフィア)を用いた頸動脈的塞栓(TAE)治療の有用性と安全性を検討することを目的とし、医師
主導治験を平成30年1月に終了済みである。令和6年8月に薬事承認申請する予定である。
2.先進医療Bの試験
食道表在癌に対するアルゴンプラズマ併用高周波凝固焼灼療法の有効性及び安全性を検討する臨床試験
切除が不可能な食道表在癌を対象に、アルゴンプラズマ併用高周波凝固焼灼療法による有効性と安全性を
検討することを目的としている。令和5年3月に本院の認定臨床研究審査委員会で承認され、令和6年4月に
先進医療会議で承認された。令和6年5月、先進医療Bとして告示されたのを受けて試験を開始した。
分散型治験(DCT)体制整備・実施状況
<実施例>
・遠隔でのパーソナル・ヘルス・レコード (PHR) 取得
① 高血圧患者を対象としたAppCare-HT試験
② 慢性心不全患者を対象としたAppCare-HF試験
<システム整備状況>
オンライン診療・DCTツール: MiROHA、Viedoc導入済み
12