よむ、つかう、まなぶ。
資料2-1:前回部会における主な指摘事項への対応(臨床研究中核病院の承認要件見直しについて) (52 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第38回 11/28)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
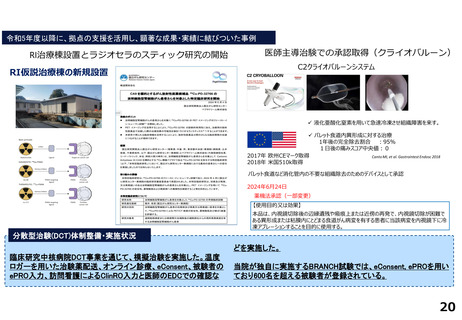
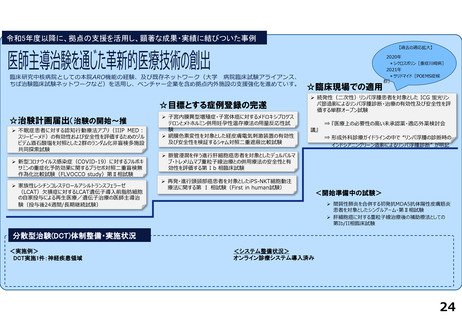
令和5年度以降に、拠点の支援を活用し、顕著な成果・実績に結びついた事例
医師主導治験
➢ 敗血症又は敗血症性ショックと診断された患者を対象とした,トシリズマブの単施設,非盲検,第IIa相臨
床試験当院IRBにおいて審議し令和5年12月に承認され、同月に治験届を提出。
先進医療
➢ 着床前胚異数性検査(PGT-A)の検討
先進医療会議での承認の後、令和6年4月より先進医療Bとして公示され患者登録を開始。
患者申出療養
➢ 筋萎縮性側索硬化症に対するEPI-589の再投与の安全性に関する研究
患者申出療養評価会議(令和5年6月開催)において審議され、患者申出療養として承認される。
分散型治験(DCT)体制整備・実施状況
①特定臨床研究 フルリモート型DCT
エンシトレルビル フマル酸のCOVID-19罹患後症状に対する有効性の検証
研究責任医師:忽那賢志(感染制御部)
研究内容:軽症新型コロナウイルス感染症(COVID-19)患者を対象として、エ
ンシトレルビル フマル酸を5日間投与した時の罹患後症状に対する有効性及
び安全性を、プラセボを対照薬として検証的に比較検討する。
研究対象者数:2,000例
パートナー医療機関数(パートナーサイト):200機関(予定)
<システム整備状況>
オンライン診療、eConsent、eSource:MiROHA(Micin社)を導入し、整備済
み
52
医師主導治験
➢ 敗血症又は敗血症性ショックと診断された患者を対象とした,トシリズマブの単施設,非盲検,第IIa相臨
床試験当院IRBにおいて審議し令和5年12月に承認され、同月に治験届を提出。
先進医療
➢ 着床前胚異数性検査(PGT-A)の検討
先進医療会議での承認の後、令和6年4月より先進医療Bとして公示され患者登録を開始。
患者申出療養
➢ 筋萎縮性側索硬化症に対するEPI-589の再投与の安全性に関する研究
患者申出療養評価会議(令和5年6月開催)において審議され、患者申出療養として承認される。
分散型治験(DCT)体制整備・実施状況
①特定臨床研究 フルリモート型DCT
エンシトレルビル フマル酸のCOVID-19罹患後症状に対する有効性の検証
研究責任医師:忽那賢志(感染制御部)
研究内容:軽症新型コロナウイルス感染症(COVID-19)患者を対象として、エ
ンシトレルビル フマル酸を5日間投与した時の罹患後症状に対する有効性及
び安全性を、プラセボを対照薬として検証的に比較検討する。
研究対象者数:2,000例
パートナー医療機関数(パートナーサイト):200機関(予定)
<システム整備状況>
オンライン診療、eConsent、eSource:MiROHA(Micin社)を導入し、整備済
み
52