よむ、つかう、まなぶ。
資料2-1:前回部会における主な指摘事項への対応(臨床研究中核病院の承認要件見直しについて) (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第38回 11/28)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
令和6年4月1日時点
※人員体制、研究、研修実績については、
令和4年度業務報告書に基づき記載
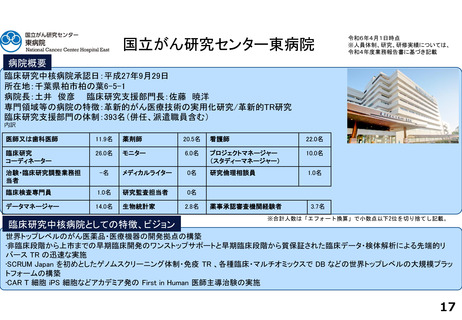
東北大学病院
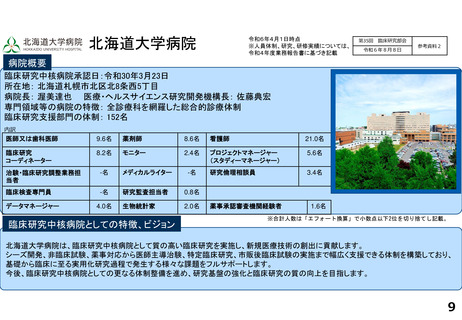
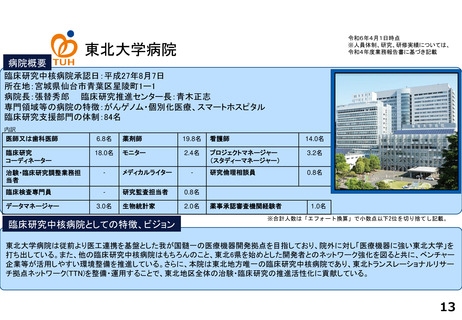
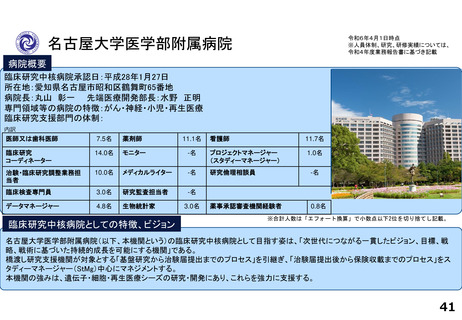
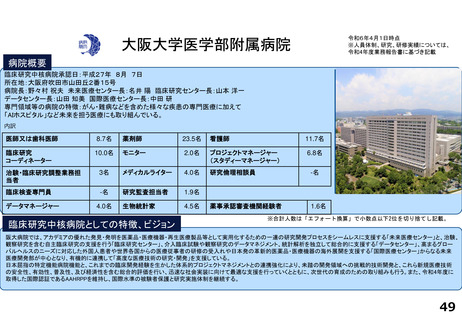
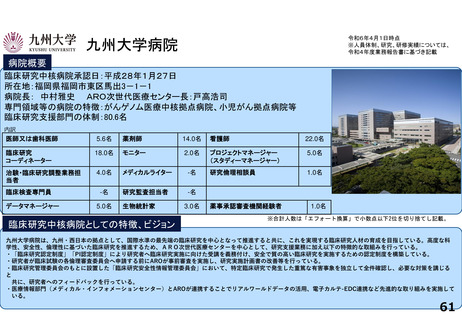
病院概要
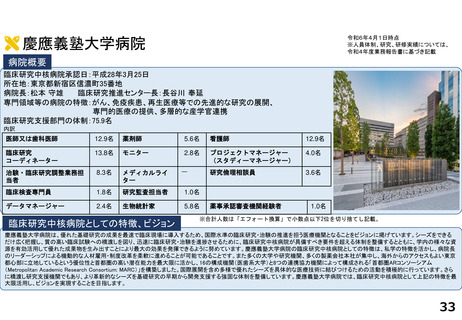
臨床研究中核病院承認日:平成27年8月7日
所在地:宮城県仙台市青葉区星陵町1ー1
病院長:張替秀郎 臨床研究推進センター長:青木正志
専門領域等の病院の特徴:がんゲノム・個別化医療、スマートホスピタル
臨床研究支援部門の体制:84名
病院の画像
内訳
医師又は歯科医師
6.8名
薬剤師
19.8名
看護師
14.0名
臨床研究
コーディネーター
18.0名
モニター
2.4名
プロジェクトマネージャー
(スタディーマネージャー)
3.2名
研究倫理相談員
0.8名
薬事承認審査機関経験者
1.0名
治験・臨床研究調整業務担
当者
-
メディカルライター
-
臨床検査専門員
-
研究監査担当者
0.8名
データマネージャー
3.0名
生物統計家
2.0名
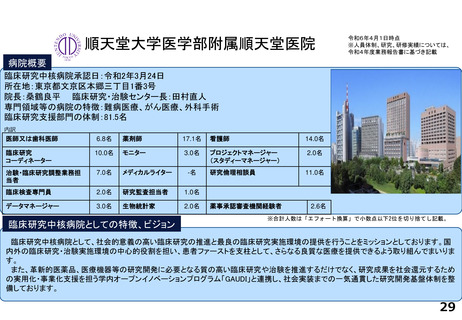
臨床研究中核病院としての特徴、ビジョン
※合計人数は「エフォート換算」で小数点以下2位を切り捨てし記載。
東北大学病院は従前より医工連携を基盤とした我が国髄一の医療機器開発拠点を目指しており、院外に対し「医療機器に強い東北大学」を
打ち出している。また、他の臨床研究中核病院はもちろんのこと、東北6県を始めとした開発者とのネットワーク強化を図ると共に、ベンチャー
企業等が活用しやすい環境整備を推進している。さらに、本院は東北地方唯一の臨床研究中核病院であり、東北トランスレーショナルリサー
チ拠点ネットワーク(TTN)を整備・運用することで、東北地区全体の治験・臨床研究の推進活性化に貢献している。
13
※人員体制、研究、研修実績については、
令和4年度業務報告書に基づき記載
東北大学病院
病院概要
臨床研究中核病院承認日:平成27年8月7日
所在地:宮城県仙台市青葉区星陵町1ー1
病院長:張替秀郎 臨床研究推進センター長:青木正志
専門領域等の病院の特徴:がんゲノム・個別化医療、スマートホスピタル
臨床研究支援部門の体制:84名
病院の画像
内訳
医師又は歯科医師
6.8名
薬剤師
19.8名
看護師
14.0名
臨床研究
コーディネーター
18.0名
モニター
2.4名
プロジェクトマネージャー
(スタディーマネージャー)
3.2名
研究倫理相談員
0.8名
薬事承認審査機関経験者
1.0名
治験・臨床研究調整業務担
当者
-
メディカルライター
-
臨床検査専門員
-
研究監査担当者
0.8名
データマネージャー
3.0名
生物統計家
2.0名
臨床研究中核病院としての特徴、ビジョン
※合計人数は「エフォート換算」で小数点以下2位を切り捨てし記載。
東北大学病院は従前より医工連携を基盤とした我が国髄一の医療機器開発拠点を目指しており、院外に対し「医療機器に強い東北大学」を
打ち出している。また、他の臨床研究中核病院はもちろんのこと、東北6県を始めとした開発者とのネットワーク強化を図ると共に、ベンチャー
企業等が活用しやすい環境整備を推進している。さらに、本院は東北地方唯一の臨床研究中核病院であり、東北トランスレーショナルリサー
チ拠点ネットワーク(TTN)を整備・運用することで、東北地区全体の治験・臨床研究の推進活性化に貢献している。
13