よむ、つかう、まなぶ。
資料2-1:前回部会における主な指摘事項への対応(臨床研究中核病院の承認要件見直しについて) (29 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第38回 11/28)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
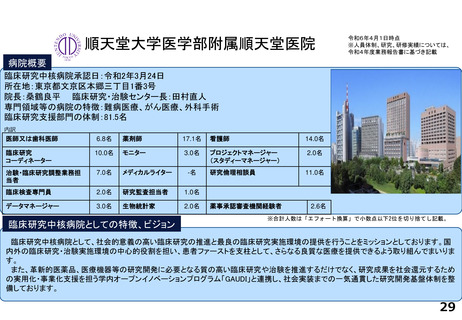
順天堂大学医学部附属順天堂医院
令和6年4月1日時点
※人員体制、研究、研修実績については、
令和4年度業務報告書に基づき記載
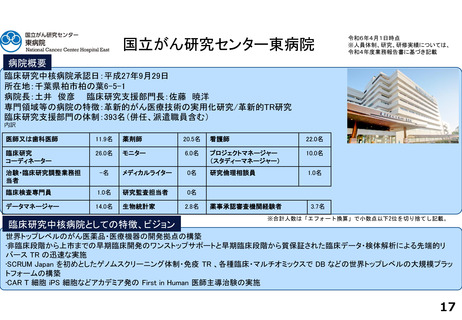
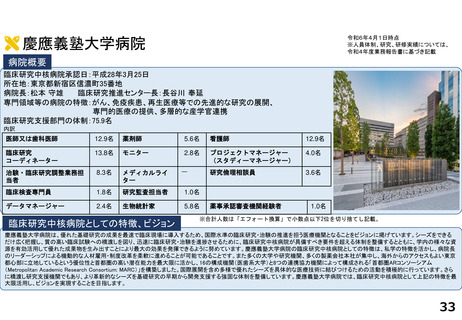
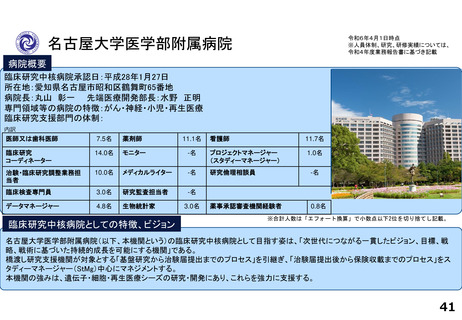
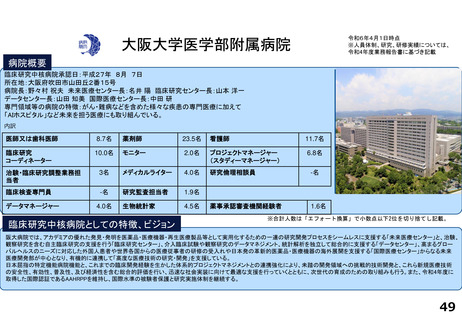
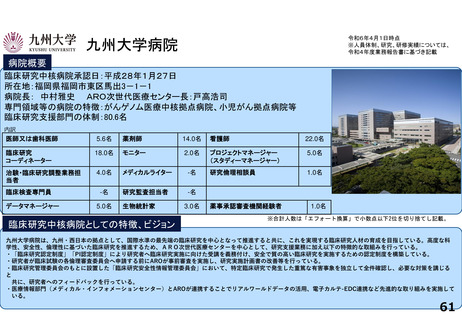
病院概要
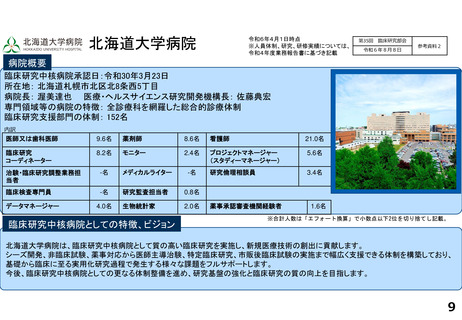
臨床研究中核病院承認日:令和2年3月24日
所在地:東京都文京区本郷三丁目1番3号
院長:桑鶴良平 臨床研究・治験センター長:田村直人
専門領域等の病院の特徴:難病医療、がん医療、外科手術
臨床研究支援部門の体制:81.5名
病院の画像
内訳
医師又は歯科医師
6.8名
薬剤師
17.1名
看護師
14.0名
臨床研究
コーディネーター
10.0名
モニター
3.0名
プロジェクトマネージャー
(スタディーマネージャー)
2.0名
治験・臨床研究調整業務担
当者
7.0名
メディカルライター
-名
研究倫理相談員
11.0名
臨床検査専門員
2.0名
研究監査担当者
1.0名
データマネージャー
3.0名
生物統計家
2.0名
臨床研究中核病院としての特徴、ビジョン
薬事承認審査機関経験者
2.6名
※合計人数は「エフォート換算」で小数点以下2位を切り捨てし記載。
臨床研究中核病院として、社会的意義の高い臨床研究の推進と最良の臨床研究実施環境の提供を行うことをミッションとしております。国
内外の臨床研究・治験実施環境の中心的役割を担い、患者ファーストを支柱として、さらなる良質な医療を提供できるよう取り組んでまいりま
す。
また、革新的医薬品、医療機器等の研究開発に必要となる質の高い臨床研究や治験を推進するだけでなく、研究成果を社会還元するため
の実用化・事業化支援を担う学内オープンイノベーションプログラム「GAUDI」と連携し、社会実装までの一気通貫した研究開発基盤体制を整
備しております。
29
令和6年4月1日時点
※人員体制、研究、研修実績については、
令和4年度業務報告書に基づき記載
病院概要
臨床研究中核病院承認日:令和2年3月24日
所在地:東京都文京区本郷三丁目1番3号
院長:桑鶴良平 臨床研究・治験センター長:田村直人
専門領域等の病院の特徴:難病医療、がん医療、外科手術
臨床研究支援部門の体制:81.5名
病院の画像
内訳
医師又は歯科医師
6.8名
薬剤師
17.1名
看護師
14.0名
臨床研究
コーディネーター
10.0名
モニター
3.0名
プロジェクトマネージャー
(スタディーマネージャー)
2.0名
治験・臨床研究調整業務担
当者
7.0名
メディカルライター
-名
研究倫理相談員
11.0名
臨床検査専門員
2.0名
研究監査担当者
1.0名
データマネージャー
3.0名
生物統計家
2.0名
臨床研究中核病院としての特徴、ビジョン
薬事承認審査機関経験者
2.6名
※合計人数は「エフォート換算」で小数点以下2位を切り捨てし記載。
臨床研究中核病院として、社会的意義の高い臨床研究の推進と最良の臨床研究実施環境の提供を行うことをミッションとしております。国
内外の臨床研究・治験実施環境の中心的役割を担い、患者ファーストを支柱として、さらなる良質な医療を提供できるよう取り組んでまいりま
す。
また、革新的医薬品、医療機器等の研究開発に必要となる質の高い臨床研究や治験を推進するだけでなく、研究成果を社会還元するため
の実用化・事業化支援を担う学内オープンイノベーションプログラム「GAUDI」と連携し、社会実装までの一気通貫した研究開発基盤体制を整
備しております。
29