よむ、つかう、まなぶ。
資料2-1:前回部会における主な指摘事項への対応(臨床研究中核病院の承認要件見直しについて) (43 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第38回 11/28)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
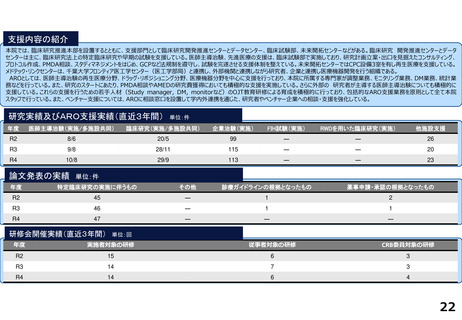
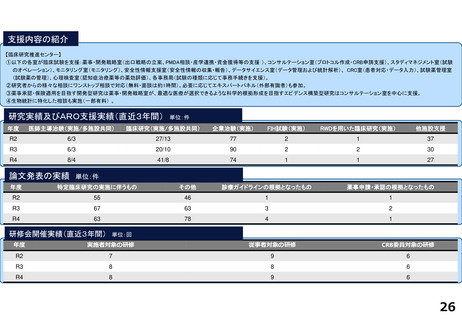
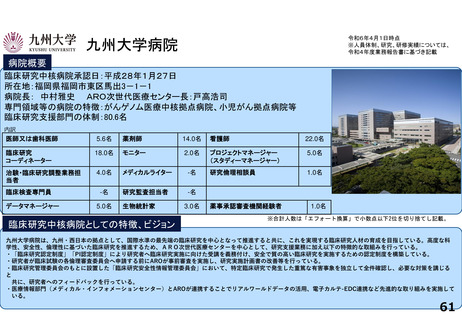
先進医療への対応
①相談窓口機能の整備:先進医療に関する院内外からの相談を受けるため先端医療開発部(臨床研究相談窓口)及び地域連携・患者相談センター
(患者申出療養相談窓口)にそれぞれ相談窓口を設置し、先端医療開発部、経営企画課、医事課のスタッフが連携して相談者の要望に応じた対応を行っている。
②相談体制の整備:先端医療開発部に寄せられた相談案件の中で先進医療Bに関係する案件に関しては、昨年度に引き続き、事前相談を厚生労働省研究開発
振興課のご指導を受けながら行っている。2023年度は5件の先進医療関連の相談案件の中で、新たに3件の支援を開始した。2022年先進医療Bとして告示を得
た一件に関しては変更届などの事務的な業務の支援を行っていたが、症例登録は終了し、総括報告書等の準備を行っている。
患者申出療養への対応
①インフィグラチニブ経口投与療法(官報告示平成30年12月13日):最終観察を終了し、総括報告書を作成中である。
②免疫グロブリンGサブクラス4自己抗体陽性難治性慢性炎症性脱髄性多発神経炎患者に対するリツキシマブ追加投与療法(官報告示令和3年8月11日):総括
報告書を作成、終了届を提出した。
③ペミガチニブ経口投与療法(官報告示令和5年11月15日):症例登録は終了し、継続投与中である。
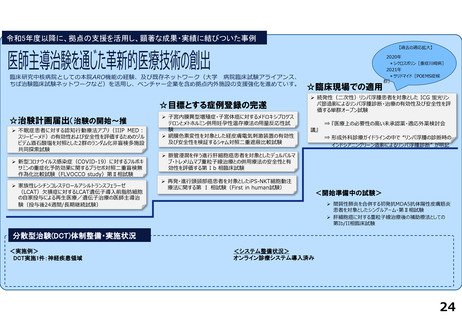
国際共同臨床研究・治験の実施状況
① 「piggyBac トランスポゾン法によるキメラ抗原受容体遺伝子改変自己 T 細胞療法」:名大病院では急性リンパ性白血病に対して、名大が技術提供したタイ王
国チュラロンコン大学では悪性リンパ腫に対してそれぞれ臨床試験を行った。成績は良好で、特にタイでは再発・難治例に対しての著効例も認められたことから、
その成果はタイでの日本との共同記者会見につながった。これらの成果を受け、国内でも悪性リンパ腫及び急性リンパ性白血病に対する多施設共同医師主導
治験(名古屋大学医学部附属病院、国立がん研究センター東病院、九州大学病院、北海道大学病院、京都大学医学部附属病院)を実施のを計画し、悪性リンパ
腫に関しては2024年3月治験届提出が終了し、急性リンパ性白血病に関しても来年度には治験がスタートできるように準備を進めている。引き続き、タイとは有効
性や有害事象などの情報を共有しつつ臨床試験を進めて行く予定である。
ベンチャー企業への支援実施状況
①先端医療開発部内に医療系ベンチャー支援窓口を設置し、各種実施フィールドの提供、クリニカルニーズや臨床実態を踏まえた学術コンサルティング、医学的
評価、プロトコル作成支援、薬事相談等へのサポート支援等を学内外問わず対応している。
②学内では、シーズ育成・起業支援ファンド、名古屋大学発ベンチャー称号授与制度などを各種整備。また、医学系との連携強化を目的としたメディカルイノベー
ション推進室を鶴舞キャンパス内に設置し、バイオデザインや医療系のベンチャー育成関連セミナーを行なっている。
③学外向けでは、MEDISOとの連携による各種支援、ジャパン・ヘルスケアベンチャー・サミットなどへの出展を活用したアウトリーチ、MIUやSTATION Aiと連携し
た名古屋大学発スタートアップショーケース等を行っている。
43
①相談窓口機能の整備:先進医療に関する院内外からの相談を受けるため先端医療開発部(臨床研究相談窓口)及び地域連携・患者相談センター
(患者申出療養相談窓口)にそれぞれ相談窓口を設置し、先端医療開発部、経営企画課、医事課のスタッフが連携して相談者の要望に応じた対応を行っている。
②相談体制の整備:先端医療開発部に寄せられた相談案件の中で先進医療Bに関係する案件に関しては、昨年度に引き続き、事前相談を厚生労働省研究開発
振興課のご指導を受けながら行っている。2023年度は5件の先進医療関連の相談案件の中で、新たに3件の支援を開始した。2022年先進医療Bとして告示を得
た一件に関しては変更届などの事務的な業務の支援を行っていたが、症例登録は終了し、総括報告書等の準備を行っている。
患者申出療養への対応
①インフィグラチニブ経口投与療法(官報告示平成30年12月13日):最終観察を終了し、総括報告書を作成中である。
②免疫グロブリンGサブクラス4自己抗体陽性難治性慢性炎症性脱髄性多発神経炎患者に対するリツキシマブ追加投与療法(官報告示令和3年8月11日):総括
報告書を作成、終了届を提出した。
③ペミガチニブ経口投与療法(官報告示令和5年11月15日):症例登録は終了し、継続投与中である。
国際共同臨床研究・治験の実施状況
① 「piggyBac トランスポゾン法によるキメラ抗原受容体遺伝子改変自己 T 細胞療法」:名大病院では急性リンパ性白血病に対して、名大が技術提供したタイ王
国チュラロンコン大学では悪性リンパ腫に対してそれぞれ臨床試験を行った。成績は良好で、特にタイでは再発・難治例に対しての著効例も認められたことから、
その成果はタイでの日本との共同記者会見につながった。これらの成果を受け、国内でも悪性リンパ腫及び急性リンパ性白血病に対する多施設共同医師主導
治験(名古屋大学医学部附属病院、国立がん研究センター東病院、九州大学病院、北海道大学病院、京都大学医学部附属病院)を実施のを計画し、悪性リンパ
腫に関しては2024年3月治験届提出が終了し、急性リンパ性白血病に関しても来年度には治験がスタートできるように準備を進めている。引き続き、タイとは有効
性や有害事象などの情報を共有しつつ臨床試験を進めて行く予定である。
ベンチャー企業への支援実施状況
①先端医療開発部内に医療系ベンチャー支援窓口を設置し、各種実施フィールドの提供、クリニカルニーズや臨床実態を踏まえた学術コンサルティング、医学的
評価、プロトコル作成支援、薬事相談等へのサポート支援等を学内外問わず対応している。
②学内では、シーズ育成・起業支援ファンド、名古屋大学発ベンチャー称号授与制度などを各種整備。また、医学系との連携強化を目的としたメディカルイノベー
ション推進室を鶴舞キャンパス内に設置し、バイオデザインや医療系のベンチャー育成関連セミナーを行なっている。
③学外向けでは、MEDISOとの連携による各種支援、ジャパン・ヘルスケアベンチャー・サミットなどへの出展を活用したアウトリーチ、MIUやSTATION Aiと連携し
た名古屋大学発スタートアップショーケース等を行っている。
43