よむ、つかう、まなぶ。
資料2-1:前回部会における主な指摘事項への対応(臨床研究中核病院の承認要件見直しについて) (46 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第38回 11/28)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
支援内容の紹介
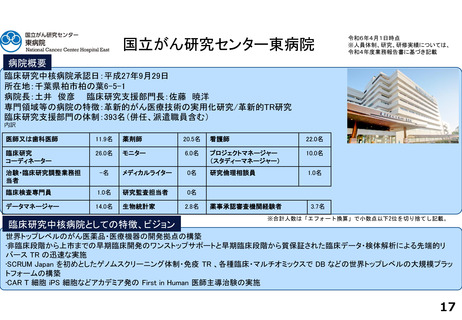
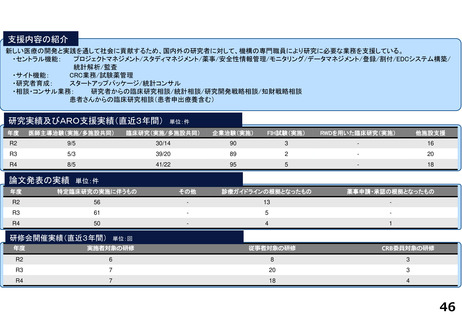
新しい医療の開発と実践を通して社会に貢献するため、国内外の研究者に対して、機構の専門職員により研究に必要な業務を支援している。
・セントラル機能:
プロジェクトマネジメント/スタディマネジメント/薬事/安全性情報管理/モニタリング/データマネジメント/登録/割付/EDCシステム構築/
統計解析/監査
・サイト機能:
CRC業務/試験薬管理
・研究者育成:
スタートアップパッケージ/統計コンサル
・相談・コンサル業務:
研究者からの臨床研究相談/統計相談/研究開発戦略相談/知財戦略相談
患者さんからの臨床研究相談(患者申出療養含む)
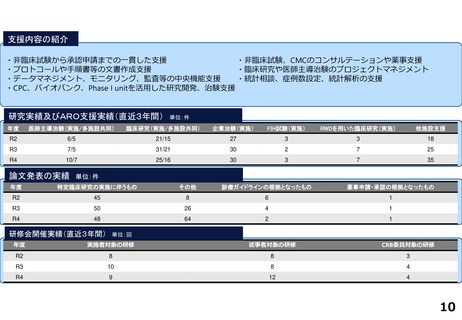
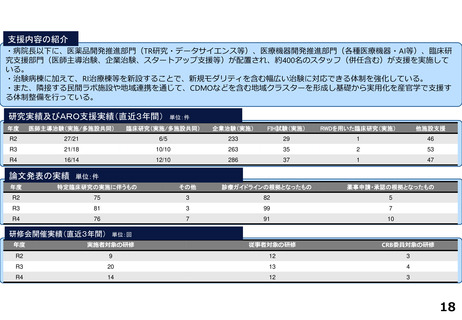
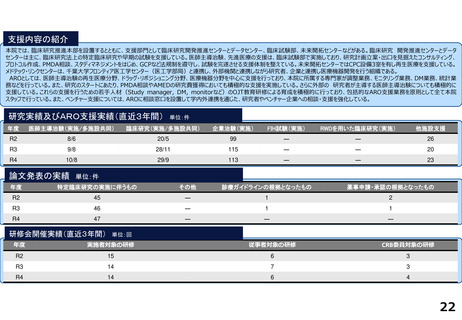
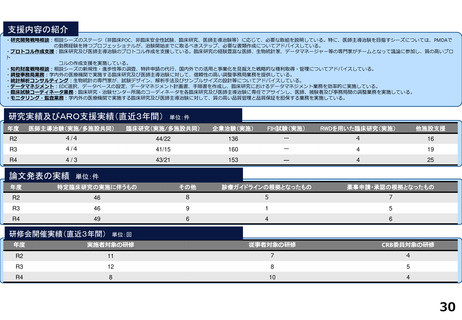
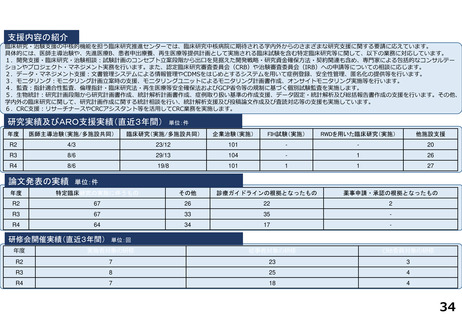
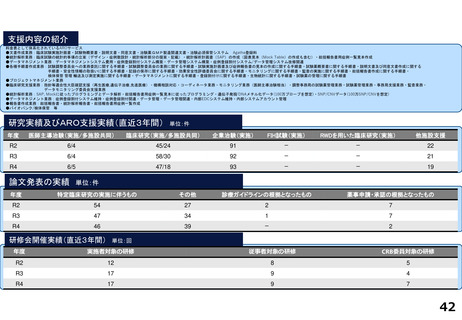
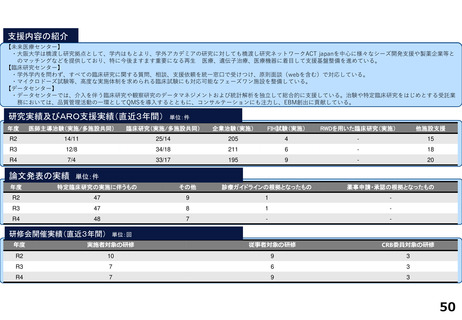
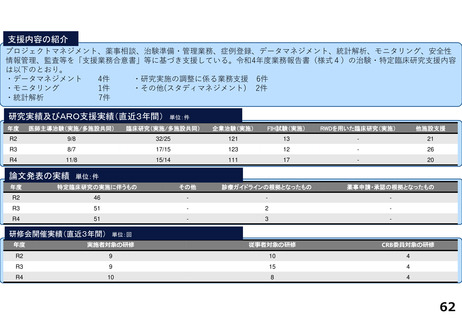
研究実績及びARO支援実績(直近3年間) 単位:件
年度
医師主導治験(実施/多施設共同)
臨床研究(実施/多施設共同)
企業治験(実施)
FIH試験(実施)
RWDを用いた臨床研究(実施)
他施設支援
R2
9/5
30/14
90
3
-
16
R3
5/3
39/20
89
2
-
20
R4
8/5
41/22
95
5
-
18
論文発表の実績 単位:件
年度
特定臨床研究の実施に伴うもの
その他
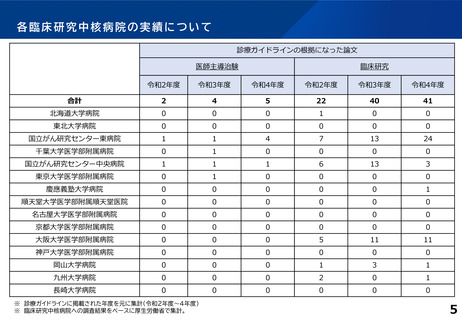
診療ガイドラインの根拠となったもの
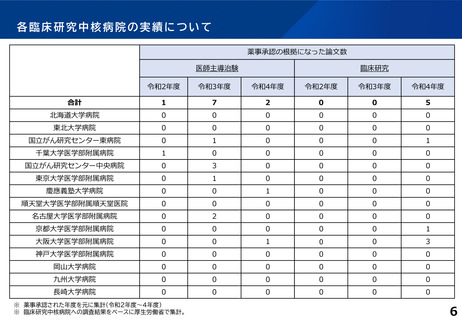
薬事申請・承認の根拠となったもの
R2
56
-
13
-
R3
61
-
5
-
R4
50
-
4
1
研修会開催実績(直近3年間)
単位:回
年度
実施者対象の研修
従事者対象の研修
CRB委員対象の研修
R2
6
8
3
R3
7
20
3
R4
7
18
4
46
新しい医療の開発と実践を通して社会に貢献するため、国内外の研究者に対して、機構の専門職員により研究に必要な業務を支援している。
・セントラル機能:
プロジェクトマネジメント/スタディマネジメント/薬事/安全性情報管理/モニタリング/データマネジメント/登録/割付/EDCシステム構築/
統計解析/監査
・サイト機能:
CRC業務/試験薬管理
・研究者育成:
スタートアップパッケージ/統計コンサル
・相談・コンサル業務:
研究者からの臨床研究相談/統計相談/研究開発戦略相談/知財戦略相談
患者さんからの臨床研究相談(患者申出療養含む)
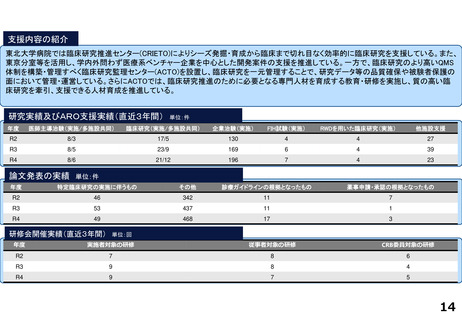
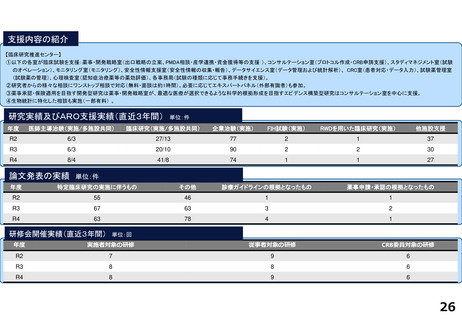
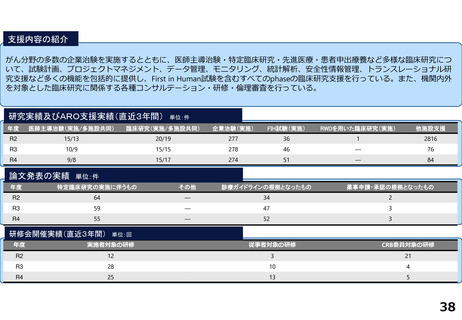
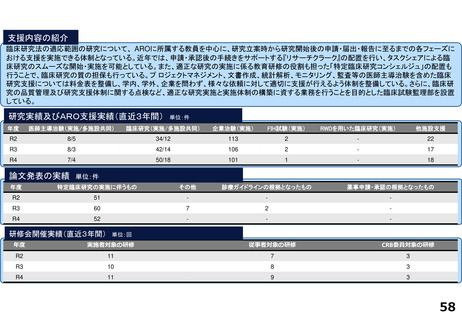
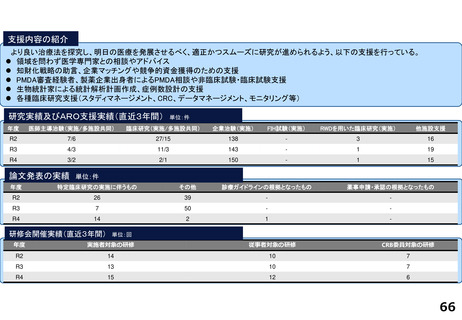
研究実績及びARO支援実績(直近3年間) 単位:件
年度
医師主導治験(実施/多施設共同)
臨床研究(実施/多施設共同)
企業治験(実施)
FIH試験(実施)
RWDを用いた臨床研究(実施)
他施設支援
R2
9/5
30/14
90
3
-
16
R3
5/3
39/20
89
2
-
20
R4
8/5
41/22
95
5
-
18
論文発表の実績 単位:件
年度
特定臨床研究の実施に伴うもの
その他
診療ガイドラインの根拠となったもの
薬事申請・承認の根拠となったもの
R2
56
-
13
-
R3
61
-
5
-
R4
50
-
4
1
研修会開催実績(直近3年間)
単位:回
年度
実施者対象の研修
従事者対象の研修
CRB委員対象の研修
R2
6
8
3
R3
7
20
3
R4
7
18
4
46