よむ、つかう、まなぶ。
資料2-1:前回部会における主な指摘事項への対応(臨床研究中核病院の承認要件見直しについて) (42 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第38回 11/28)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
支援内容の紹介
料金表として体系化されているAROサービス
●文書作成業務:臨床試験実施計画書・試験物概要書・説明文書・同意文書・治験薬GMP製造関連文書・治験必須保管システム Agatha登録料
●統計解析業務:臨床試験の統計的事項の立案(デザイン・症例数設計・統計解析部分の提案・記載)・統計解析計画書(SAP)の作成(図表見本(Mock Table)の作成も含む)・総括報告書用症例一覧見本作成
●データマネジメント業務:データマネジメントシステム費用・症例登録割付システム構築・データ管理システム構築・症例登録割付システム/データ管理システム改修関連
●各種手順書作成業務:試験調整委員会への業務委託に関する手順書・試験調整委員会の業務に関する手順書・試験実施計画書及び症例報告書の見本の作成に関する手順書・試験薬概要書に関する手順書・説明文書及び同意文書作成に関する
手順書・安全性情報の取扱いに関する手順書・記録の保存に関する手順書・効果安全性評価委員会に関する手順書・モニタリングに関する手順書・監査の実施に関する手順書・総括報告書作成に関する手順書・
検体保管 管理 輸送及び測定実施に関する手順書・データマネジメントに関する手順書・登録割付けに関する手順書・生物統計に関する手順書・試験薬の管理に関する手順書
●プロジェクトマネジメント業務
●臨床研究支援業務:指針等適合性大臣確認支援(再生医療,遺伝子治療,先進医療)・機構相談対応・コーディネータ業務・モニタリング業務(医師主導治験相当)・調整事務局の試験薬管理業務・試験薬管理業務・事務局支援業務・監査業務・
データモニタリング委員会支援業務
●統計解析業務:SAP, Mockに従ったプログラミングとデータ解析・総括報告書用症例一覧見本に従ったプログラミング・遺伝子発現/DNAメチル化データ(100万プローブを想定)・SNP/CNVデータ(100万SNP/CNVを想定)
●データマネジメント業務:症例登録割付システム維持・症例登録割付関連・データ管理・データ管理関連・内部EDCシステム維持・内部システムアカウント管理
●報告書作成業務:総括報告書・統計解析報告書・総括報告書用症例一覧作成
●バイオバンク/検体保管 等
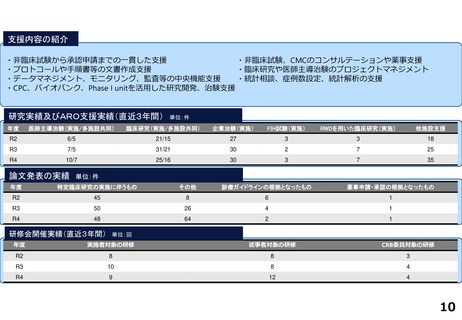
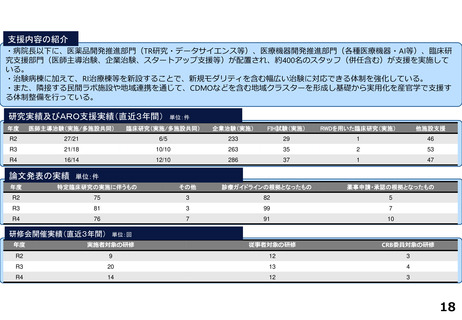
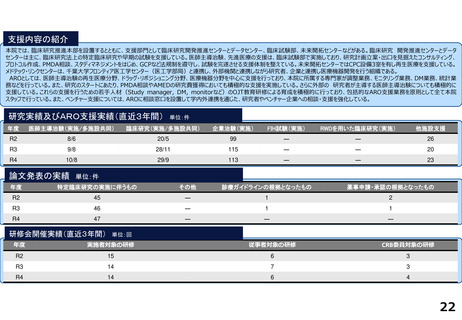
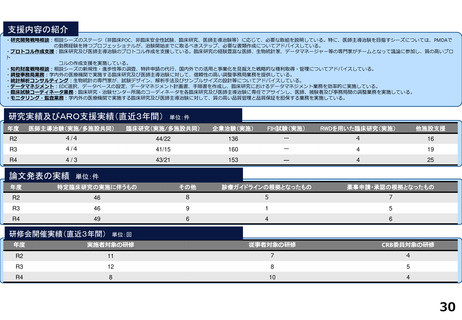
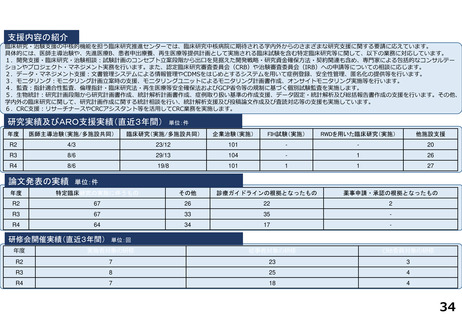
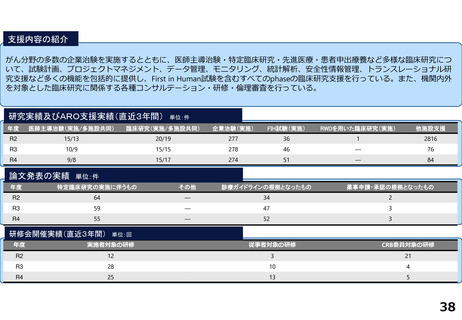
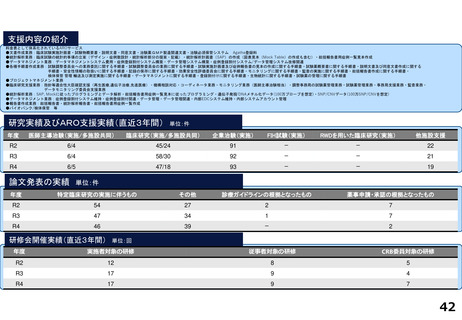
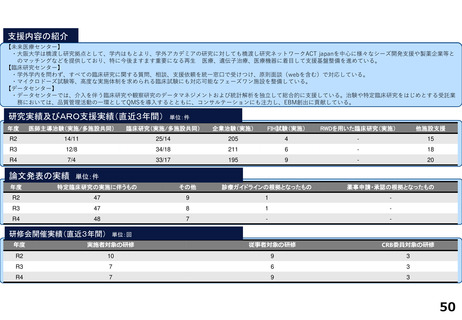
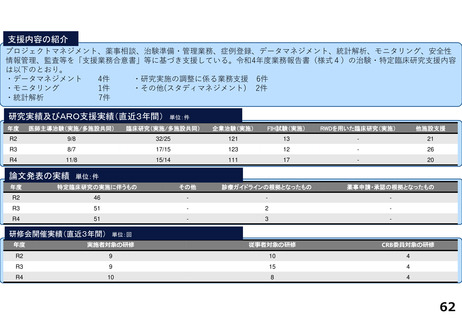
研究実績及びARO支援実績(直近3年間) 単位:件
年度
医師主導治験(実施/多施設共同)
臨床研究(実施/多施設共同)
企業治験(実施)
FIH試験(実施)
RWDを用いた臨床研究(実施)
他施設支援
R2
6/4
45/24
91
-
-
22
R3
6/4
58/30
92
-
-
21
R4
6/5
47/18
93
-
-
19
論文発表の実績 単位:件
年度
特定臨床研究の実施に伴うもの
その他
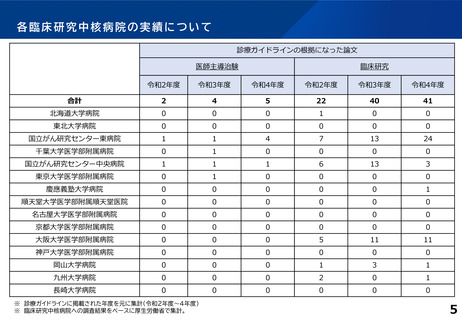
診療ガイドラインの根拠となったもの
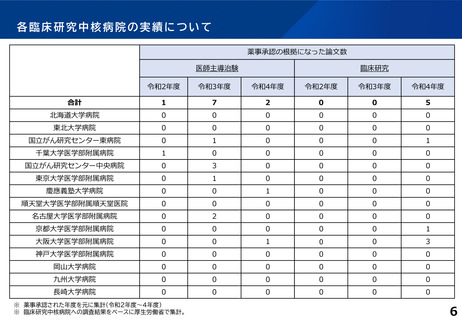
薬事申請・承認の根拠となったもの
R2
54
27
2
7
R3
47
34
1
7
R4
46
39
-
2
研修会開催実績(直近3年間)
単位:回
年度
実施者対象の研修
従事者対象の研修
CRB委員対象の研修
R2
12
8
5
R3
17
9
4
R4
17
9
7
42
料金表として体系化されているAROサービス
●文書作成業務:臨床試験実施計画書・試験物概要書・説明文書・同意文書・治験薬GMP製造関連文書・治験必須保管システム Agatha登録料
●統計解析業務:臨床試験の統計的事項の立案(デザイン・症例数設計・統計解析部分の提案・記載)・統計解析計画書(SAP)の作成(図表見本(Mock Table)の作成も含む)・総括報告書用症例一覧見本作成
●データマネジメント業務:データマネジメントシステム費用・症例登録割付システム構築・データ管理システム構築・症例登録割付システム/データ管理システム改修関連
●各種手順書作成業務:試験調整委員会への業務委託に関する手順書・試験調整委員会の業務に関する手順書・試験実施計画書及び症例報告書の見本の作成に関する手順書・試験薬概要書に関する手順書・説明文書及び同意文書作成に関する
手順書・安全性情報の取扱いに関する手順書・記録の保存に関する手順書・効果安全性評価委員会に関する手順書・モニタリングに関する手順書・監査の実施に関する手順書・総括報告書作成に関する手順書・
検体保管 管理 輸送及び測定実施に関する手順書・データマネジメントに関する手順書・登録割付けに関する手順書・生物統計に関する手順書・試験薬の管理に関する手順書
●プロジェクトマネジメント業務
●臨床研究支援業務:指針等適合性大臣確認支援(再生医療,遺伝子治療,先進医療)・機構相談対応・コーディネータ業務・モニタリング業務(医師主導治験相当)・調整事務局の試験薬管理業務・試験薬管理業務・事務局支援業務・監査業務・
データモニタリング委員会支援業務
●統計解析業務:SAP, Mockに従ったプログラミングとデータ解析・総括報告書用症例一覧見本に従ったプログラミング・遺伝子発現/DNAメチル化データ(100万プローブを想定)・SNP/CNVデータ(100万SNP/CNVを想定)
●データマネジメント業務:症例登録割付システム維持・症例登録割付関連・データ管理・データ管理関連・内部EDCシステム維持・内部システムアカウント管理
●報告書作成業務:総括報告書・統計解析報告書・総括報告書用症例一覧作成
●バイオバンク/検体保管 等
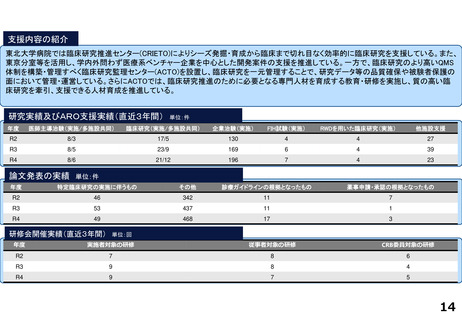
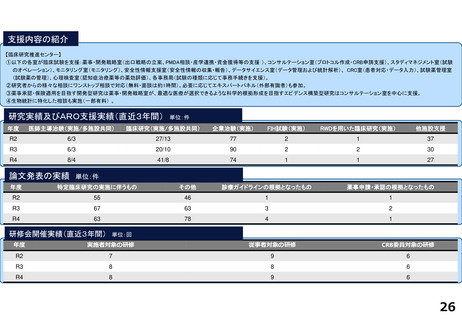
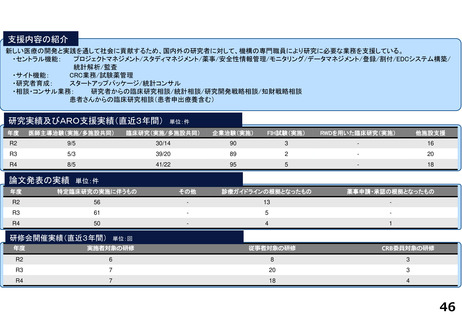
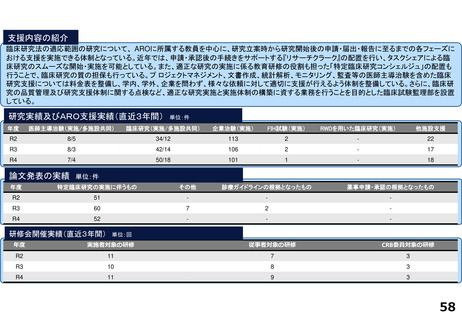
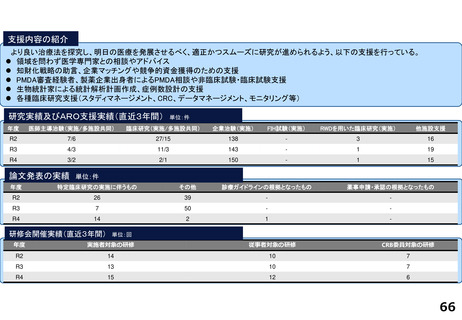
研究実績及びARO支援実績(直近3年間) 単位:件
年度
医師主導治験(実施/多施設共同)
臨床研究(実施/多施設共同)
企業治験(実施)
FIH試験(実施)
RWDを用いた臨床研究(実施)
他施設支援
R2
6/4
45/24
91
-
-
22
R3
6/4
58/30
92
-
-
21
R4
6/5
47/18
93
-
-
19
論文発表の実績 単位:件
年度
特定臨床研究の実施に伴うもの
その他
診療ガイドラインの根拠となったもの
薬事申請・承認の根拠となったもの
R2
54
27
2
7
R3
47
34
1
7
R4
46
39
-
2
研修会開催実績(直近3年間)
単位:回
年度
実施者対象の研修
従事者対象の研修
CRB委員対象の研修
R2
12
8
5
R3
17
9
4
R4
17
9
7
42