よむ、つかう、まなぶ。
資料2-1:前回部会における主な指摘事項への対応(臨床研究中核病院の承認要件見直しについて) (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第38回 11/28)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
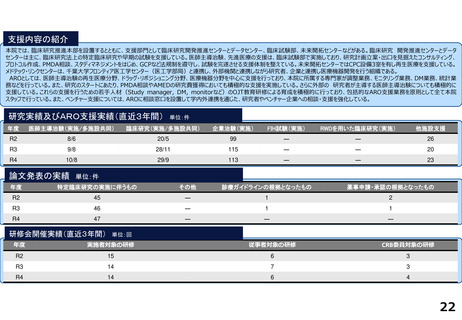
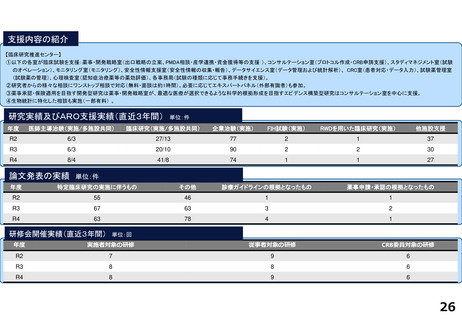
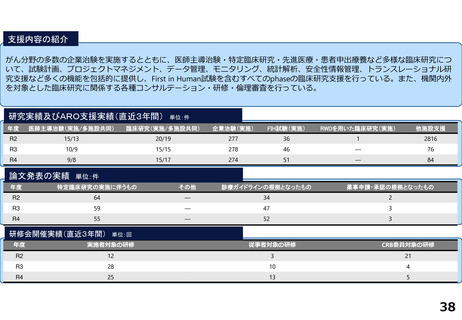
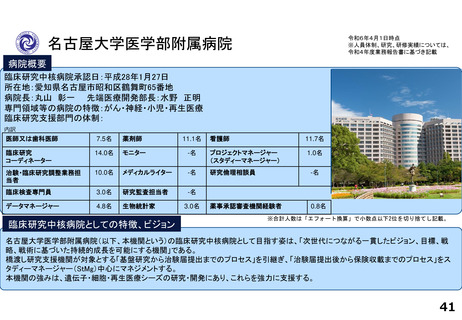
支援内容の紹介
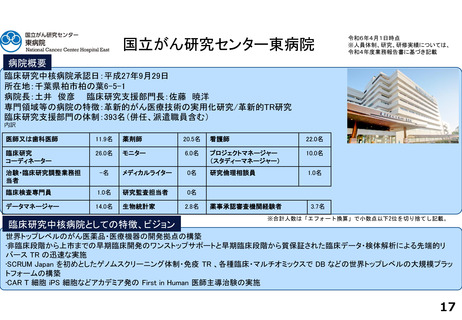
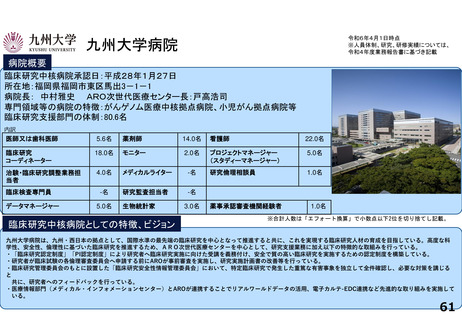
・病院長以下に、医薬品開発推進部門(TR研究・データサイエンス等)、医療機器開発推進部門(各種医療機器・AI等)、臨床研
究支援部門(医師主導治験、企業治験、スタートアップ支援等)が配置され、約400名のスタッフ(併任含む)が支援を実施して
いる。
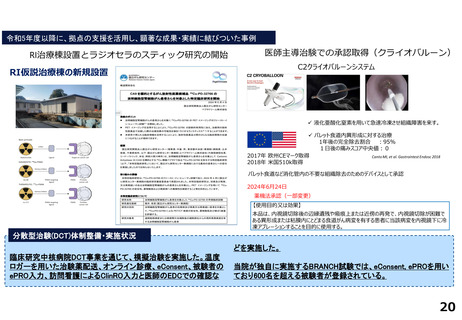
・治験病棟に加えて、RI治療棟等を新設することで、新規モダリティを含む幅広い治験に対応できる体制を強化している。
・また、隣接する民間ラボ施設や地域連携を通じて、CDMOなどを含む地域クラスターを形成し基礎から実用化を産官学で支援す
る体制整備を行っている。
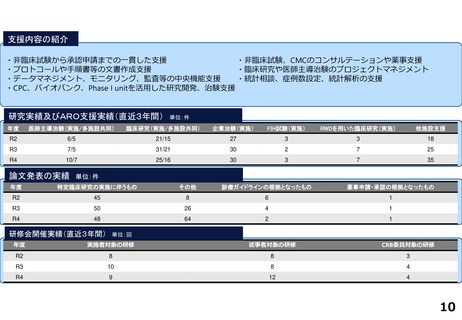
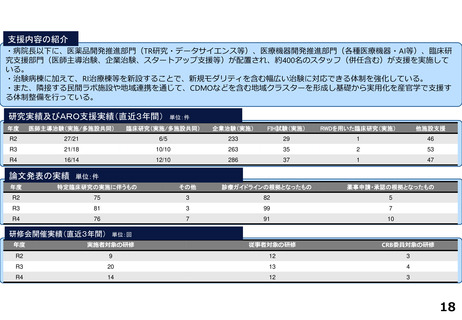
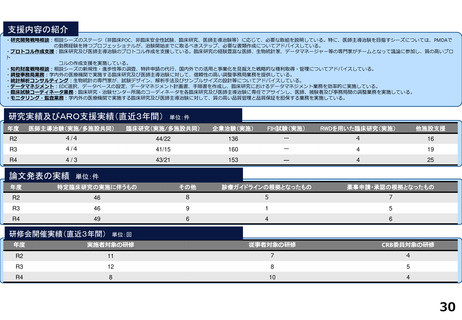
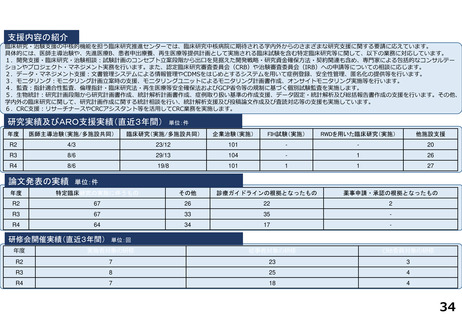
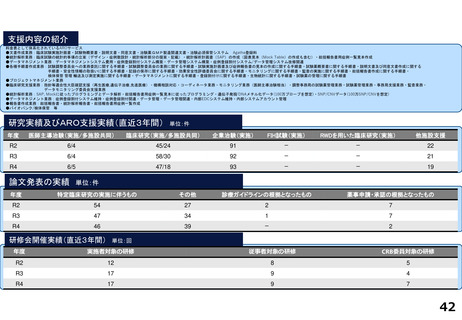
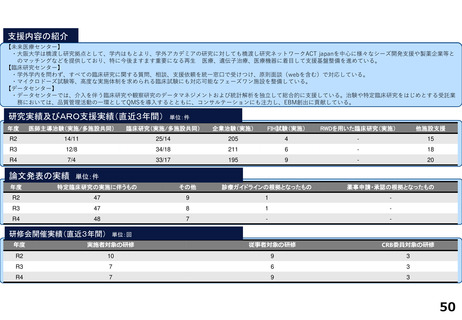
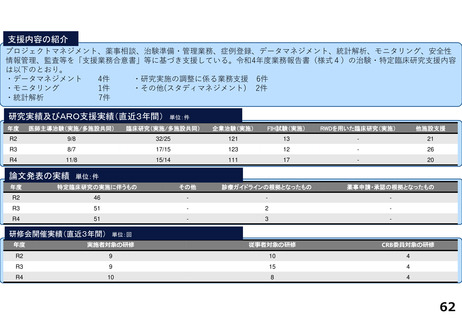
研究実績及びARO支援実績(直近3年間) 単位:件
年度
医師主導治験(実施/多施設共同)
臨床研究(実施/多施設共同)
企業治験(実施)
FIH試験(実施)
RWDを用いた臨床研究(実施)
他施設支援
R2
27/21
6/5
233
29
1
46
R3
21/18
10/10
263
35
2
53
R4
16/14
12/10
286
37
1
47
論文発表の実績 単位:件
年度
特定臨床研究の実施に伴うもの
その他
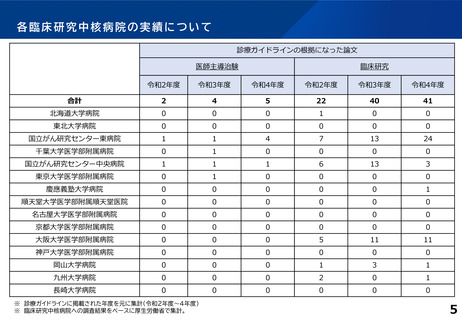
診療ガイドラインの根拠となったもの
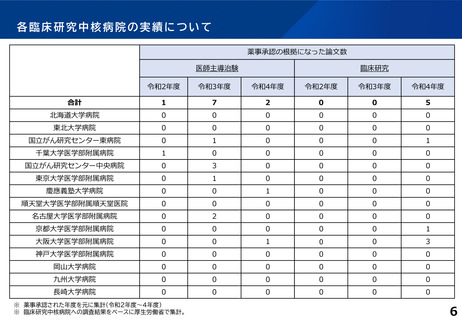
薬事申請・承認の根拠となったもの
R2
75
3
82
5
R3
81
3
99
7
R4
76
7
91
10
研修会開催実績(直近3年間)
単位:回
年度
実施者対象の研修
従事者対象の研修
CRB委員対象の研修
R2
9
12
3
R3
20
13
4
R4
14
12
3
18
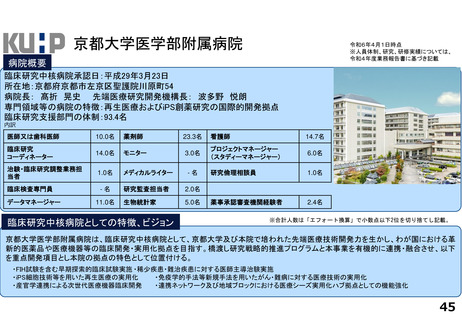
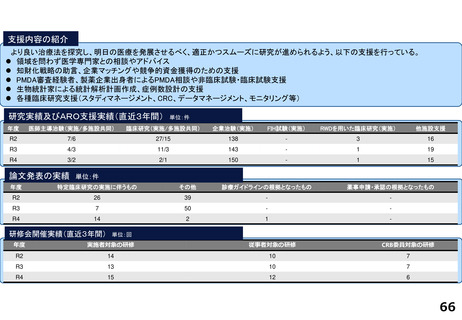
・病院長以下に、医薬品開発推進部門(TR研究・データサイエンス等)、医療機器開発推進部門(各種医療機器・AI等)、臨床研
究支援部門(医師主導治験、企業治験、スタートアップ支援等)が配置され、約400名のスタッフ(併任含む)が支援を実施して
いる。
・治験病棟に加えて、RI治療棟等を新設することで、新規モダリティを含む幅広い治験に対応できる体制を強化している。
・また、隣接する民間ラボ施設や地域連携を通じて、CDMOなどを含む地域クラスターを形成し基礎から実用化を産官学で支援す
る体制整備を行っている。
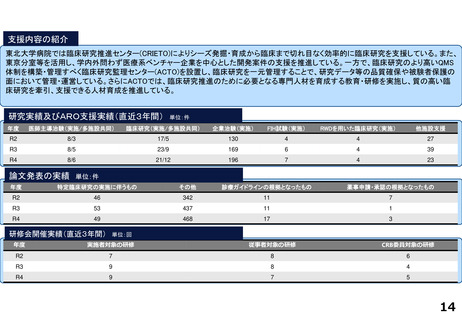
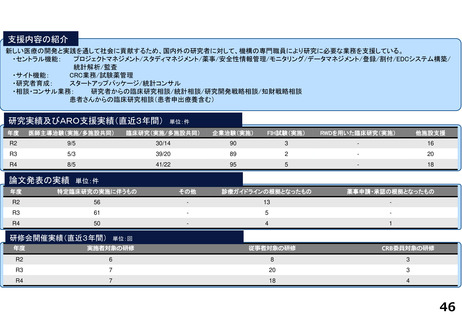
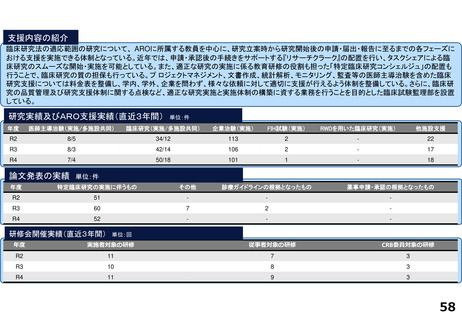
研究実績及びARO支援実績(直近3年間) 単位:件
年度
医師主導治験(実施/多施設共同)
臨床研究(実施/多施設共同)
企業治験(実施)
FIH試験(実施)
RWDを用いた臨床研究(実施)
他施設支援
R2
27/21
6/5
233
29
1
46
R3
21/18
10/10
263
35
2
53
R4
16/14
12/10
286
37
1
47
論文発表の実績 単位:件
年度
特定臨床研究の実施に伴うもの
その他
診療ガイドラインの根拠となったもの
薬事申請・承認の根拠となったもの
R2
75
3
82
5
R3
81
3
99
7
R4
76
7
91
10
研修会開催実績(直近3年間)
単位:回
年度
実施者対象の研修
従事者対象の研修
CRB委員対象の研修
R2
9
12
3
R3
20
13
4
R4
14
12
3
18