よむ、つかう、まなぶ。
資料2-1:前回部会における主な指摘事項への対応(臨床研究中核病院の承認要件見直しについて) (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第38回 11/28)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
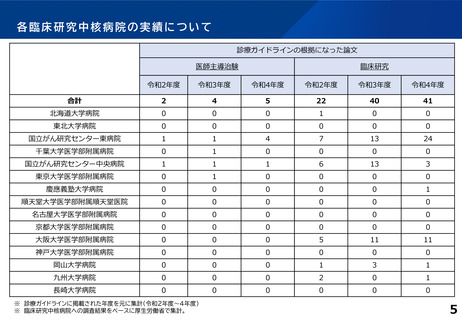
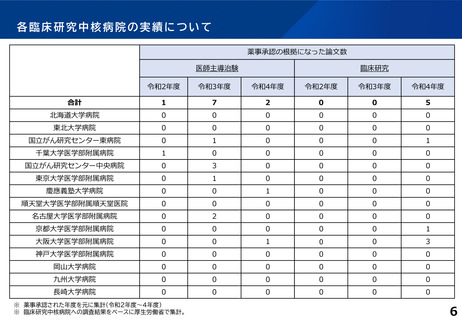
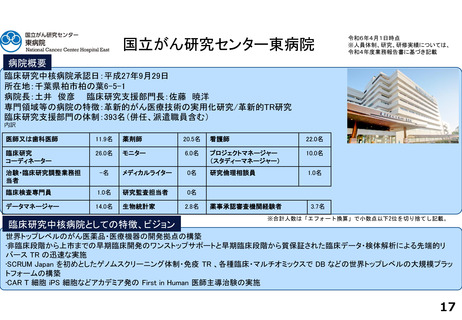
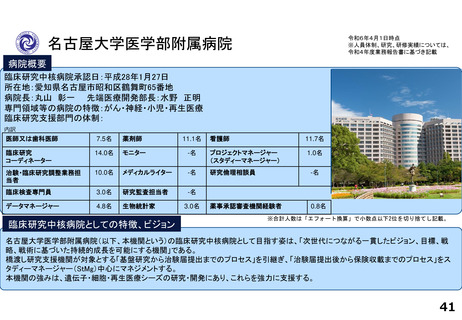
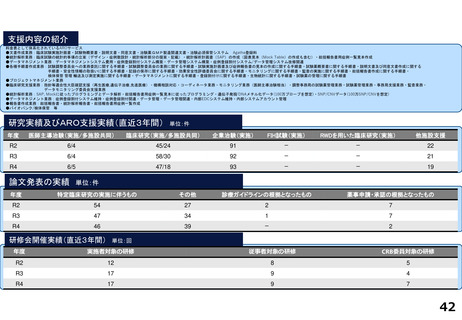
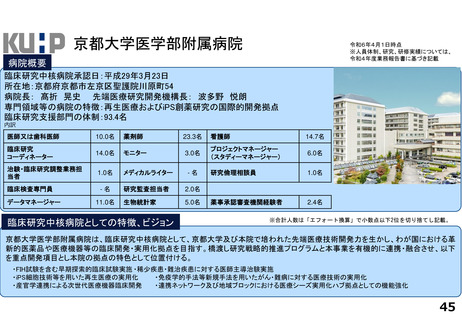
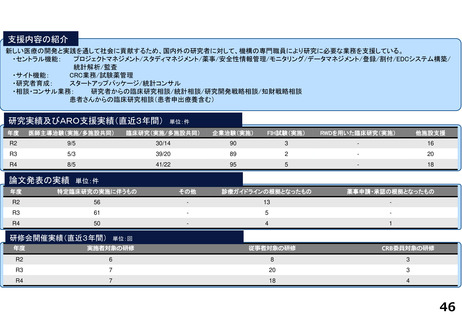
各臨床研究中核病院の実績について
診療ガイドライン、薬事承認の根拠になった論文の実績
診療ガイドラインの根拠になった論文数
薬事承認の根拠になった論文数
195件
26件
がん
消化器腫瘍
呼吸器腫瘍
血液腫瘍
肝胆膵腫瘍
耳鼻科腫瘍
婦人科腫瘍
乳がん
内分泌腫瘍
150
76
26
14
13
9
8
2
2
消化器
呼吸器
神経
循環器
がん治療法等
小児科
感染症
内分泌
皮膚
眼科
移植関連
精神
その他
5
5
5
4
3
3
3
2
2
2
2
2
7
がん
消化器腫瘍
呼吸器腫瘍
血液腫瘍
がん診断・治療
内分泌腫瘍
乳がん
16 神経
4 皮膚
4 血液
代謝拮抗薬
3
解毒剤
2 内分泌代謝
免疫・
2
アレルギー
1 泌尿器
3
2
1
1
1
1
1
※ 公表している令和4年度業務報告書(令和2~4年度の実績)か
ら厚生労働省において集計。
※ 一部の病院の業務報告書では実績の記載がないため、実際よ
り少ない実績数となっている可能性がある。
※ 医師主導治験、臨床研究のほか、企業治験等による実績も含む。
4
診療ガイドライン、薬事承認の根拠になった論文の実績
診療ガイドラインの根拠になった論文数
薬事承認の根拠になった論文数
195件
26件
がん
消化器腫瘍
呼吸器腫瘍
血液腫瘍
肝胆膵腫瘍
耳鼻科腫瘍
婦人科腫瘍
乳がん
内分泌腫瘍
150
76
26
14
13
9
8
2
2
消化器
呼吸器
神経
循環器
がん治療法等
小児科
感染症
内分泌
皮膚
眼科
移植関連
精神
その他
5
5
5
4
3
3
3
2
2
2
2
2
7
がん
消化器腫瘍
呼吸器腫瘍
血液腫瘍
がん診断・治療
内分泌腫瘍
乳がん
16 神経
4 皮膚
4 血液
代謝拮抗薬
3
解毒剤
2 内分泌代謝
免疫・
2
アレルギー
1 泌尿器
3
2
1
1
1
1
1
※ 公表している令和4年度業務報告書(令和2~4年度の実績)か
ら厚生労働省において集計。
※ 一部の病院の業務報告書では実績の記載がないため、実際よ
り少ない実績数となっている可能性がある。
※ 医師主導治験、臨床研究のほか、企業治験等による実績も含む。
4