よむ、つかう、まなぶ。
参考資料4 有効性評価に基づく子宮頸がん検診ガイドライン更新版2020年3月31日 (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_25869.html |
| 出典情報 | がん検診のあり方に関する検討会(第35回 5/25)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
III. 作成方法
1. ガイドライン作成の役割分担
2011 年に米国 IOM (Institute of Medicine:米国医学研究所)では診療ガイドラインの定義を
更新するとともに、ガイドラインの作成要件を提示した。その中で、ガイドライン作成委員会と文献レ
ビュー委員会の分離を勧めている。U.S. Preventive Services Task Force (以下 USPSTF)は
Evidence-based Practice Center (以下 EPC)との連携を図りながら、EPC の提出するエビデン
スレポートをもとに予防対策ガイドラインを作成している。また National Institute for Health and
Care Excellence (英国国立医療技術評価機構、以下 NICE)も同様に英国内の王立大学との連
携を図っている。
2003 年度から作成している「有効性評価に基づくがん検診ガイドライン」は、文献検索からガイ
ドライン作成に至る一連の過程を同一の委員会が担っていた。本ガイドライン作成開始当初は、そ
の必要性も十分に認識されておらず、文献レビューやガイドライン作成を担える人材も不足してい
た。そのため、同一の委員が文献レビューとガイドライン作成を担当したことは、必要な人材を確保
し、基本概念を共有しながらガイドラインを作成するうえでは合理的であった。しかし、当該検診の
専門家の参画は、文献では入手できない専門的知識や国内事情を把握することができるものの、
文献評価に偏りが生じる可能性や、エビデンスレポート作成段階で公正な議論の妨げになることが
あるため、胃がん検診ガイドライン(2014 年度版)の作成段階からガイドライン作成委員会と文献レ
ビュー委員会を分離した。
子宮頸がん検診のエビデンスレポート作成に先立ち、対象となる検診方法の検討と Analytic
Framework(AF)の作成については、エビデンスレポート作成委員会とガイドライン作成委員会で
協議した。またエビデンスレポートの進捗状況をガイドライン作成事務局に逐次報告した。エビデン
スレポートは 2017 年度末には一旦ほぼまとまったものの、ガイドライン作成委員会から、検診の対
象年齢と検診間隔について追加検討の要求があったことから期間を 1 年延長して検討が行われ
た。エビデンスレポートはガイドライン作成委員会に提出され、その内容を再検討した。2018 年度
より市民など広い立場の意見を反映することを目的に組織を改編し、ガイドラインの対象臓器の選
定や課題を検討するアドバイザリー委員会を設け、ガイドライン作成委員会のメンバーを一新した。
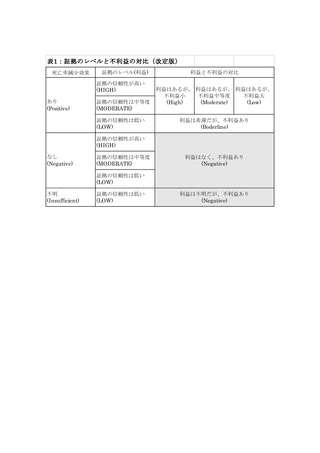
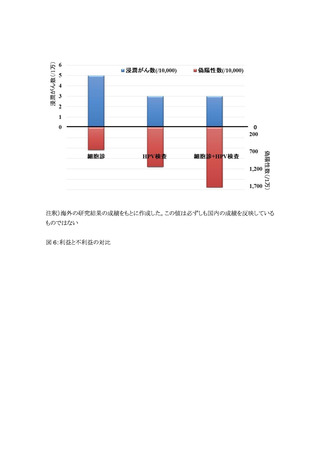
「証拠のレベル」は従来死亡率減少効果の信頼性・妥当性をもとに 4 段階の評価を行っていた
が、新たに利益と不利益に分けて、利益については 3 段階、利益と不利益の対比として 5 段階の
評価を行った(表 1)。
また「推奨グレード」は、推奨 A と推奨 B を決める根拠に、子宮頸がん検診ガイドライン(2009 年
版)までは、利益を示す研究手法(無作為化比較試験;推奨 A, 症例対照研究、コホート研究;推
奨 B)としていたが、乳がん検診ガイドライン(2013 年度版)以降は利益と不利益の差の大きさを根
拠にしていた。しかし推奨 A も B も対策型検診・任意型検診双方に等しく実施を推奨しており、あ
えて区分する必要がなかったことから、今回から B を廃止し、推奨 A に統一した。また推奨 C につ
いては利益と不利益の差が近接しているものと定義し、対策型検診では実施を推奨しない・任意
1. ガイドライン作成の役割分担
2011 年に米国 IOM (Institute of Medicine:米国医学研究所)では診療ガイドラインの定義を
更新するとともに、ガイドラインの作成要件を提示した。その中で、ガイドライン作成委員会と文献レ
ビュー委員会の分離を勧めている。U.S. Preventive Services Task Force (以下 USPSTF)は
Evidence-based Practice Center (以下 EPC)との連携を図りながら、EPC の提出するエビデン
スレポートをもとに予防対策ガイドラインを作成している。また National Institute for Health and
Care Excellence (英国国立医療技術評価機構、以下 NICE)も同様に英国内の王立大学との連
携を図っている。
2003 年度から作成している「有効性評価に基づくがん検診ガイドライン」は、文献検索からガイ
ドライン作成に至る一連の過程を同一の委員会が担っていた。本ガイドライン作成開始当初は、そ
の必要性も十分に認識されておらず、文献レビューやガイドライン作成を担える人材も不足してい
た。そのため、同一の委員が文献レビューとガイドライン作成を担当したことは、必要な人材を確保
し、基本概念を共有しながらガイドラインを作成するうえでは合理的であった。しかし、当該検診の
専門家の参画は、文献では入手できない専門的知識や国内事情を把握することができるものの、
文献評価に偏りが生じる可能性や、エビデンスレポート作成段階で公正な議論の妨げになることが
あるため、胃がん検診ガイドライン(2014 年度版)の作成段階からガイドライン作成委員会と文献レ
ビュー委員会を分離した。
子宮頸がん検診のエビデンスレポート作成に先立ち、対象となる検診方法の検討と Analytic
Framework(AF)の作成については、エビデンスレポート作成委員会とガイドライン作成委員会で
協議した。またエビデンスレポートの進捗状況をガイドライン作成事務局に逐次報告した。エビデン
スレポートは 2017 年度末には一旦ほぼまとまったものの、ガイドライン作成委員会から、検診の対
象年齢と検診間隔について追加検討の要求があったことから期間を 1 年延長して検討が行われ
た。エビデンスレポートはガイドライン作成委員会に提出され、その内容を再検討した。2018 年度
より市民など広い立場の意見を反映することを目的に組織を改編し、ガイドラインの対象臓器の選
定や課題を検討するアドバイザリー委員会を設け、ガイドライン作成委員会のメンバーを一新した。
「証拠のレベル」は従来死亡率減少効果の信頼性・妥当性をもとに 4 段階の評価を行っていた
が、新たに利益と不利益に分けて、利益については 3 段階、利益と不利益の対比として 5 段階の
評価を行った(表 1)。
また「推奨グレード」は、推奨 A と推奨 B を決める根拠に、子宮頸がん検診ガイドライン(2009 年
版)までは、利益を示す研究手法(無作為化比較試験;推奨 A, 症例対照研究、コホート研究;推
奨 B)としていたが、乳がん検診ガイドライン(2013 年度版)以降は利益と不利益の差の大きさを根
拠にしていた。しかし推奨 A も B も対策型検診・任意型検診双方に等しく実施を推奨しており、あ
えて区分する必要がなかったことから、今回から B を廃止し、推奨 A に統一した。また推奨 C につ
いては利益と不利益の差が近接しているものと定義し、対策型検診では実施を推奨しない・任意