よむ、つかう、まなぶ。
【資料No.1】★審査報告書 (22 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26901.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会(令和4年度第3回 7/20)、医薬品第二部会(令和4年度第6回 7/20)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
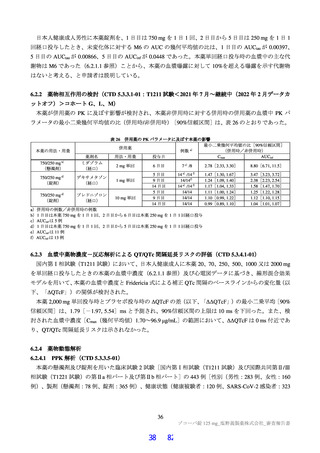
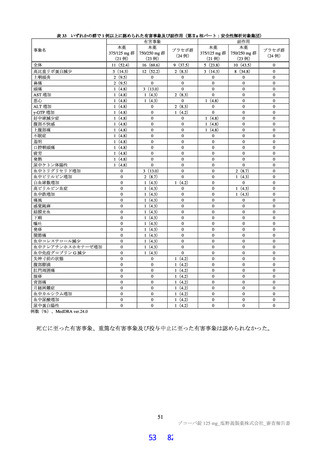
ヒト CYP 分子種(CYP1A2、2B6、2C8、2C9、2C19、2D6、3A4 及び 3A5)発現系に本薬の 14C 標識
体(50 µmol/L)を添加して 90 分間インキュベートしたとき、総放射能に対する未変化体の割合は 94.9
~97.7%24)であった。代謝物の生成はわずかであり、M3(0.11~0.15%)25)、M4(0.10~0.54%)25)及び
M5(0.03~1.08%)25)が認められた。
ヒト肝ミクロソームに本薬の 14C 標識体(50 µmol/L)を添加し、各 CYP 分子種(CYP1A2、2B6、2C8、
2C9、2C19、2D6 又は 3A4/5)に対する阻害剤26)の存在下又は非存在下で、60 分間インキュベートした
ときの M3、M4 及び M5 の生成阻害率が検討された。その結果、M3 の生成は CYP3A4/5 阻害剤で 6.3%、
M4 の生成は CYP3A4/5 阻害剤で 38.1%、M5 の生成は CYP3A4/5 阻害剤で 50.0%、CYP2B6 阻害剤で
10.2%、CYP2C8 阻害剤で 14.1%、CYP2C9 阻害剤で 7.7%、CYP2D6 阻害剤で 2.6%阻害され、その他の
阻害剤による生成阻害は認められなかった。本薬の代謝物(M3、M4 及び M5)の生成について、各 CYP
分子種の阻害剤による生成阻害作用は部分的であり、複数の CYP 分子種が関与することが示唆された。
4.3.3
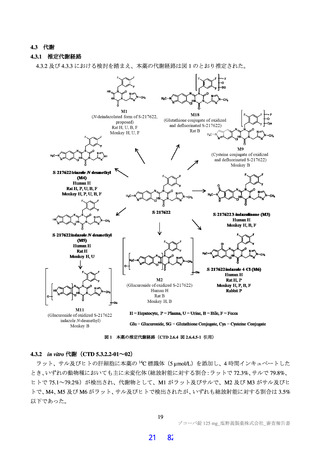
in vivo 代謝(CTD 4.2.2.4-01~03)
胆管カニュレーション施行又は未施行のラット、ウサギ及びサルに本薬の 14C 標識体(2 mg/kg)を単
回経口投与したときの血漿中の総放射能に対する本薬及び代謝物の割合は表 14、尿、糞及び胆汁中にお
ける投与放射能に対する本薬及び代謝物の割合は表 15 のとおりであり、血漿、尿、糞及び胆汁中の代謝
物は表 16 のとおりであった。
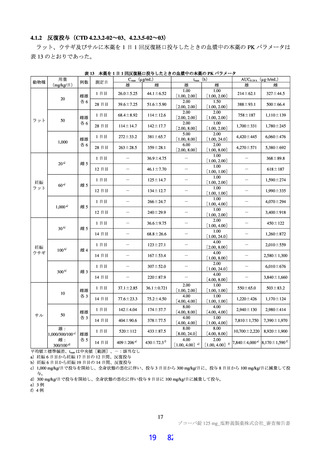
表 14
本薬の 14C 標識体(2 mg/kg)を単回経口投与したときの血漿中の総放射能に対する本薬及び代謝物の割合
血漿中の総放射能に対する割合(%)
動物種 胆管カニュレーション
性別
例数/時点
測定試料
測定時点(h)
本薬
代謝物
2
85.1
1.3
2
8
83.2
3.9
ラット
未施行
雄
血漿
24
43.6
3.7
4
86.0
-
1
ウサギ
未施行
雌
血漿
24
74.2
1.5
4
91.0
1.7
3
24
81.5
5.4
サル
未施行
雄
血漿
48
54.6
9.7
平均値、-:検出されず
表 15
本薬の 14C 標識体(2 mg/kg)を単回経口投与したときの尿、糞及び胆汁中における投与放射能に対する本薬及び代謝物の割合
投与放射能に対する割合(%)
動物種 胆管カニュレーション
性別
例数
測定試料
測定時点(h)
本薬
代謝物
0.3
1.4
尿
0~24
4
未施行
雄
36.7
13.1
ラット
糞
0~48
4
4.5
28.1
施行
雄
胆汁
0~48
0.8
6.7
尿
0~72
3
未施行
雄
24.5
16.2
サル
糞
0~96
2
4.9
26
施行
雄
胆汁
0~72
コントロールの発現系と本薬の 14C 標識体をインキュベートしたときの総放射能に対する本薬及び代謝物の割合は次のとおり。
本薬(未変化体)97.0%、M3:0.10%、M4:0.07%、M5:0.02%
25)
総放射能に対する代謝物の割合
26)
検討に用いられた各 CYP 分子種に対する阻害剤(Thio-TEPA:10 μmol/L、ケトコナゾール:1 μmol/L、それ以外はいずれも 5 μmol/L)
CYP1A2:Furafylline、CYP2B6:Thio-TEPA、CYP2C8:モンテルカスト、CYP2C9:Sulfaphenazole、CYP2C19:S-(+)-N-3-Benzylnirvanol、
CYP2D6:キニジン、CYP3A4/5:ケトコナゾール
24)
20
ゾコーバ錠 125 mg_塩野義製薬株式会社_審査報告書
22 / 82
体(50 µmol/L)を添加して 90 分間インキュベートしたとき、総放射能に対する未変化体の割合は 94.9
~97.7%24)であった。代謝物の生成はわずかであり、M3(0.11~0.15%)25)、M4(0.10~0.54%)25)及び
M5(0.03~1.08%)25)が認められた。
ヒト肝ミクロソームに本薬の 14C 標識体(50 µmol/L)を添加し、各 CYP 分子種(CYP1A2、2B6、2C8、
2C9、2C19、2D6 又は 3A4/5)に対する阻害剤26)の存在下又は非存在下で、60 分間インキュベートした
ときの M3、M4 及び M5 の生成阻害率が検討された。その結果、M3 の生成は CYP3A4/5 阻害剤で 6.3%、
M4 の生成は CYP3A4/5 阻害剤で 38.1%、M5 の生成は CYP3A4/5 阻害剤で 50.0%、CYP2B6 阻害剤で
10.2%、CYP2C8 阻害剤で 14.1%、CYP2C9 阻害剤で 7.7%、CYP2D6 阻害剤で 2.6%阻害され、その他の
阻害剤による生成阻害は認められなかった。本薬の代謝物(M3、M4 及び M5)の生成について、各 CYP
分子種の阻害剤による生成阻害作用は部分的であり、複数の CYP 分子種が関与することが示唆された。
4.3.3
in vivo 代謝(CTD 4.2.2.4-01~03)
胆管カニュレーション施行又は未施行のラット、ウサギ及びサルに本薬の 14C 標識体(2 mg/kg)を単
回経口投与したときの血漿中の総放射能に対する本薬及び代謝物の割合は表 14、尿、糞及び胆汁中にお
ける投与放射能に対する本薬及び代謝物の割合は表 15 のとおりであり、血漿、尿、糞及び胆汁中の代謝
物は表 16 のとおりであった。
表 14
本薬の 14C 標識体(2 mg/kg)を単回経口投与したときの血漿中の総放射能に対する本薬及び代謝物の割合
血漿中の総放射能に対する割合(%)
動物種 胆管カニュレーション
性別
例数/時点
測定試料
測定時点(h)
本薬
代謝物
2
85.1
1.3
2
8
83.2
3.9
ラット
未施行
雄
血漿
24
43.6
3.7
4
86.0
-
1
ウサギ
未施行
雌
血漿
24
74.2
1.5
4
91.0
1.7
3
24
81.5
5.4
サル
未施行
雄
血漿
48
54.6
9.7
平均値、-:検出されず
表 15
本薬の 14C 標識体(2 mg/kg)を単回経口投与したときの尿、糞及び胆汁中における投与放射能に対する本薬及び代謝物の割合
投与放射能に対する割合(%)
動物種 胆管カニュレーション
性別
例数
測定試料
測定時点(h)
本薬
代謝物
0.3
1.4
尿
0~24
4
未施行
雄
36.7
13.1
ラット
糞
0~48
4
4.5
28.1
施行
雄
胆汁
0~48
0.8
6.7
尿
0~72
3
未施行
雄
24.5
16.2
サル
糞
0~96
2
4.9
26
施行
雄
胆汁
0~72
コントロールの発現系と本薬の 14C 標識体をインキュベートしたときの総放射能に対する本薬及び代謝物の割合は次のとおり。
本薬(未変化体)97.0%、M3:0.10%、M4:0.07%、M5:0.02%
25)
総放射能に対する代謝物の割合
26)
検討に用いられた各 CYP 分子種に対する阻害剤(Thio-TEPA:10 μmol/L、ケトコナゾール:1 μmol/L、それ以外はいずれも 5 μmol/L)
CYP1A2:Furafylline、CYP2B6:Thio-TEPA、CYP2C8:モンテルカスト、CYP2C9:Sulfaphenazole、CYP2C19:S-(+)-N-3-Benzylnirvanol、
CYP2D6:キニジン、CYP3A4/5:ケトコナゾール
24)
20
ゾコーバ錠 125 mg_塩野義製薬株式会社_審査報告書
22 / 82