よむ、つかう、まなぶ。
【資料No.1】★審査報告書 (36 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26901.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会(令和4年度第3回 7/20)、医薬品第二部会(令和4年度第6回 7/20)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
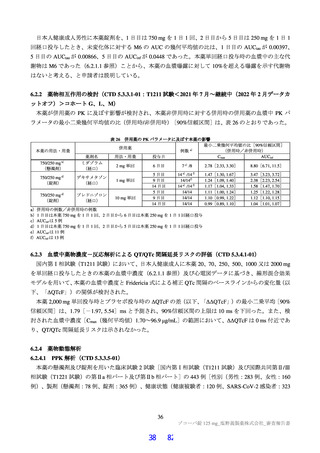
表 23
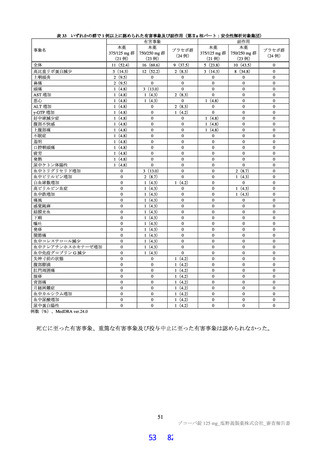
製剤の種類
懸濁剤
125 mg 錠 a)
錠剤
250 mg 錠 b)
臨床試験で使用された製剤の内訳
臨床試験
国内第Ⅰ相試験(T1211 試験 コホート A~H 及び J)
国内第Ⅰ相試験(T1211 試験 コホート N)
国際共同第Ⅱ/Ⅲ相試験(T1221 試験)
国内第Ⅰ相試験(T1211 試験 コホート L、M 及び O)
国際共同第Ⅱ/Ⅲ相試験(T1221 試験)
a)市販予定製剤
b)250 mg 錠は、「含量が異なる経口固形製剤の生物学的同等性試験ガイドライン」(平成 12 年 2 月 14 日付け医薬審第 64 号、令
和 2 年 3 月 19 日付け薬生薬審発 0319 第 1 号により一部改正)に従った溶出試験により、市販予定製剤である 125 mg 錠との同
等性が確認されている。
血漿及び尿中の本薬及び M6(主要代謝物)の血漿中及び尿中濃度測定には、LC-MS/MS 法(定量下限
本薬:血漿及び尿 10.0 ng/mL、M6:血漿 5.00 ng/mL)が用いられた。
なお、本項では、本薬の用量及び濃度はエンシトレルビルとして示す。また、特に記載のない限り、
PK パラメータは幾何平均値(CV%)で示す。
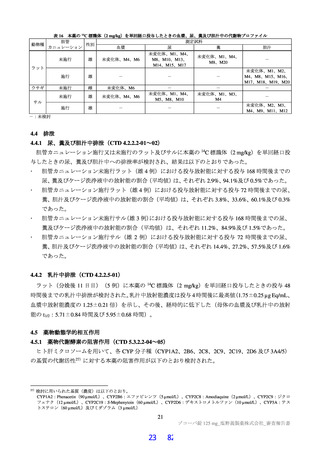
食事の影響に関する検討(CTD 5.3.3.1-01:T1211 試験<2021 年 7 月~継続中(2022 年 2 月デー
6.1.1
タカットオフ)>コホート C)
日本人健康成人(PK 評価例数:8 例)に、本薬 250 mg(懸濁剤)を空腹時又は高脂肪食(863 kcal、
脂肪 58.1%)摂取後に単回経口投与したときの本薬の PK が 2 群 2 期クロスオーバー試験にて検討され
た。
空腹時投与に対する食後投与における血漿中本薬濃度の Cmax 及び AUClast の最小二乗幾何平均値の比
(食後/空腹時)[90%信頼区間]は、0.8508[0.7507, 0.9644]及び 1.0470[1.0061, 1.0895]であった。
6.2
臨床薬理試験
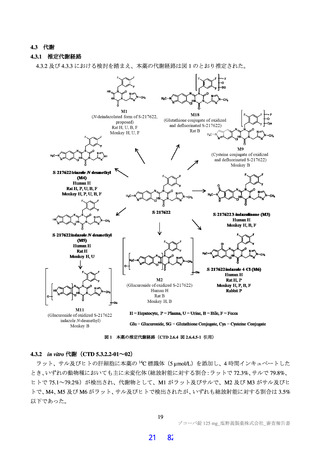
本申請に際し、健康被験者を対象とした PK 試験、PPK 解析及び曝露-応答解析等の結果が提出され
た。なお、ヒト生体試料を用いた in vitro 試験については 4.2.2、4.2.3 及び 4.3.2 項に記載する。
6.2.1
国内第Ⅰ相試験(CTD 5.3.3.1-01:T1211 試験<2021 年 7 月~継続中(2022 年 2 月データカット
オフ)>)
6.2.1.1
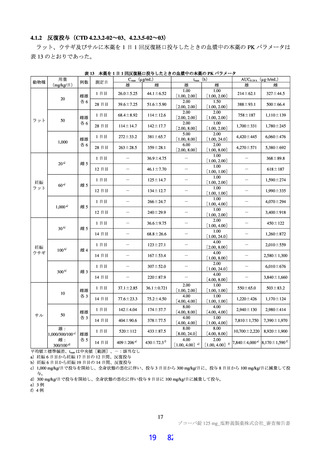
日本人健康成人における単回投与(コホート A、B、C、D、E、J)
日本人健康成人男性に、本薬懸濁剤を空腹時に単回経口投与したときの本薬の PK パラメータが検討
され、結果は表 24 のとおりであった。
34
ゾコーバ錠 125 mg_塩野義製薬株式会社_審査報告書
36 / 82
製剤の種類
懸濁剤
125 mg 錠 a)
錠剤
250 mg 錠 b)
臨床試験で使用された製剤の内訳
臨床試験
国内第Ⅰ相試験(T1211 試験 コホート A~H 及び J)
国内第Ⅰ相試験(T1211 試験 コホート N)
国際共同第Ⅱ/Ⅲ相試験(T1221 試験)
国内第Ⅰ相試験(T1211 試験 コホート L、M 及び O)
国際共同第Ⅱ/Ⅲ相試験(T1221 試験)
a)市販予定製剤
b)250 mg 錠は、「含量が異なる経口固形製剤の生物学的同等性試験ガイドライン」(平成 12 年 2 月 14 日付け医薬審第 64 号、令
和 2 年 3 月 19 日付け薬生薬審発 0319 第 1 号により一部改正)に従った溶出試験により、市販予定製剤である 125 mg 錠との同
等性が確認されている。
血漿及び尿中の本薬及び M6(主要代謝物)の血漿中及び尿中濃度測定には、LC-MS/MS 法(定量下限
本薬:血漿及び尿 10.0 ng/mL、M6:血漿 5.00 ng/mL)が用いられた。
なお、本項では、本薬の用量及び濃度はエンシトレルビルとして示す。また、特に記載のない限り、
PK パラメータは幾何平均値(CV%)で示す。
食事の影響に関する検討(CTD 5.3.3.1-01:T1211 試験<2021 年 7 月~継続中(2022 年 2 月デー
6.1.1
タカットオフ)>コホート C)
日本人健康成人(PK 評価例数:8 例)に、本薬 250 mg(懸濁剤)を空腹時又は高脂肪食(863 kcal、
脂肪 58.1%)摂取後に単回経口投与したときの本薬の PK が 2 群 2 期クロスオーバー試験にて検討され
た。
空腹時投与に対する食後投与における血漿中本薬濃度の Cmax 及び AUClast の最小二乗幾何平均値の比
(食後/空腹時)[90%信頼区間]は、0.8508[0.7507, 0.9644]及び 1.0470[1.0061, 1.0895]であった。
6.2
臨床薬理試験
本申請に際し、健康被験者を対象とした PK 試験、PPK 解析及び曝露-応答解析等の結果が提出され
た。なお、ヒト生体試料を用いた in vitro 試験については 4.2.2、4.2.3 及び 4.3.2 項に記載する。
6.2.1
国内第Ⅰ相試験(CTD 5.3.3.1-01:T1211 試験<2021 年 7 月~継続中(2022 年 2 月データカット
オフ)>)
6.2.1.1
日本人健康成人における単回投与(コホート A、B、C、D、E、J)
日本人健康成人男性に、本薬懸濁剤を空腹時に単回経口投与したときの本薬の PK パラメータが検討
され、結果は表 24 のとおりであった。
34
ゾコーバ錠 125 mg_塩野義製薬株式会社_審査報告書
36 / 82