よむ、つかう、まなぶ。
【資料No.1】★審査報告書 (53 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26901.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会(令和4年度第3回 7/20)、医薬品第二部会(令和4年度第6回 7/20)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
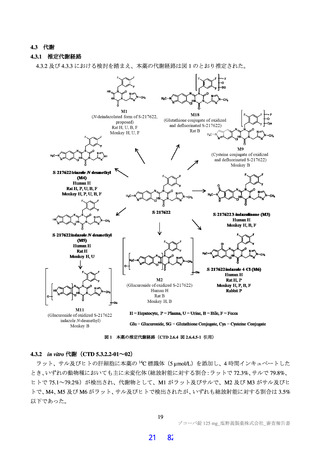
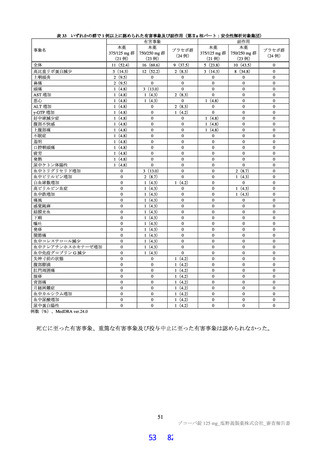
表 33
いずれかの群で 1 例以上に認められた有害事象及び副作用(第Ⅱa 相パート:安全性解析対象集団)
有害事象
副作用
本薬
本薬
本薬
本薬
事象名
プラセボ群
プラセボ群
375/125 mg 群 750/250 mg 群
375/125 mg 群 750/250 mg 群
(24 例)
(24 例)
(21 例)
(23 例)
(21 例)
(23 例)
0
全体
11(52.4)
16(69.6)
9(37.5)
5(23.8)
10(43.5)
0
高比重リポ蛋白減少
3(14.3)
12(52.2)
2(8.3)
3(14.3)
8(34.8)
0
0
0
0
0
上咽頭炎
2(9.5)
0
0
0
0
0
鼻痛
2(9.5)
0
0
0
0
頭痛
1(4.8)
3(13.0)
0
0
0
AST 増加
1(4.8)
1(4.3)
2(8.3)
0
0
0
悪心
1(4.8)
1(4.3)
1(4.8)
0
0
0
0
ALT 増加
1(4.8)
2(8.3)
0
0
0
0
γ-GTP 増加
1(4.8)
1(4.2)
0
0
0
0
好中球減少症
1(4.8)
1(4.8)
0
0
0
0
腹部不快感
1(4.8)
1(4.8)
0
0
0
0
上腹部痛
1(4.8)
1(4.8)
0
0
0
0
0
不眠症
1(4.8)
0
0
0
0
0
羞明
1(4.8)
0
0
0
0
0
口腔咽頭痛
1(4.8)
0
0
0
0
0
疲労
1(4.8)
0
0
0
0
0
発熱
1(4.8)
0
0
0
0
0
尿中ケトン体陽性
1(4.8)
0
0
0
0
血中トリグリセリド増加
3(13.0)
2(8.7)
0
0
0
0
血中ビリルビン増加
2(8.7)
1(4.3)
0
0
0
0
白血球数増加
1(4.3)
1(4.2)
0
0
0
0
高ビリルビン血症
1(4.3)
1(4.3)
0
0
0
0
血中鉄増加
1(4.3)
1(4.3)
0
0
0
0
0
痛風
1(4.3)
0
0
0
0
0
感覚鈍麻
1(4.3)
0
0
0
0
0
結膜充血
1(4.3)
0
0
0
0
0
下痢
1(4.3)
0
0
0
0
0
嘔吐
1(4.3)
0
0
0
0
0
発疹
1(4.3)
0
0
0
0
0
関節痛
1(4.3)
0
0
0
0
0
血中コレステロール減少
1(4.3)
0
0
0
0
0
血中クレアチンホスホキナーゼ増加
1(4.3)
0
0
0
0
0
血中免疫グロブリン G 減少
1(4.3)
0
0
0
0
0
失神寸前の状態
1(4.2)
0
0
0
0
0
腹部膨満
1(4.2)
0
0
0
0
0
肛門周囲痛
1(4.2)
0
0
0
0
0
湿疹
1(4.2)
0
0
0
0
0
背部痛
1(4.2)
0
0
0
0
0
月経困難症
1(4.2)
0
0
0
0
0
血中カルシウム増加
1(4.2)
0
0
0
0
0
血中尿酸増加
1(4.2)
0
0
0
0
0
尿中蛋白陽性
1(4.2)
例数(%)、MedDRA ver.24.0
死亡に至った有害事象、重篤な有害事象及び投与中止に至った有害事象は認められなかった。
51
ゾコーバ錠 125 mg_塩野義製薬株式会社_審査報告書
53 / 82
いずれかの群で 1 例以上に認められた有害事象及び副作用(第Ⅱa 相パート:安全性解析対象集団)
有害事象
副作用
本薬
本薬
本薬
本薬
事象名
プラセボ群
プラセボ群
375/125 mg 群 750/250 mg 群
375/125 mg 群 750/250 mg 群
(24 例)
(24 例)
(21 例)
(23 例)
(21 例)
(23 例)
0
全体
11(52.4)
16(69.6)
9(37.5)
5(23.8)
10(43.5)
0
高比重リポ蛋白減少
3(14.3)
12(52.2)
2(8.3)
3(14.3)
8(34.8)
0
0
0
0
0
上咽頭炎
2(9.5)
0
0
0
0
0
鼻痛
2(9.5)
0
0
0
0
頭痛
1(4.8)
3(13.0)
0
0
0
AST 増加
1(4.8)
1(4.3)
2(8.3)
0
0
0
悪心
1(4.8)
1(4.3)
1(4.8)
0
0
0
0
ALT 増加
1(4.8)
2(8.3)
0
0
0
0
γ-GTP 増加
1(4.8)
1(4.2)
0
0
0
0
好中球減少症
1(4.8)
1(4.8)
0
0
0
0
腹部不快感
1(4.8)
1(4.8)
0
0
0
0
上腹部痛
1(4.8)
1(4.8)
0
0
0
0
0
不眠症
1(4.8)
0
0
0
0
0
羞明
1(4.8)
0
0
0
0
0
口腔咽頭痛
1(4.8)
0
0
0
0
0
疲労
1(4.8)
0
0
0
0
0
発熱
1(4.8)
0
0
0
0
0
尿中ケトン体陽性
1(4.8)
0
0
0
0
血中トリグリセリド増加
3(13.0)
2(8.7)
0
0
0
0
血中ビリルビン増加
2(8.7)
1(4.3)
0
0
0
0
白血球数増加
1(4.3)
1(4.2)
0
0
0
0
高ビリルビン血症
1(4.3)
1(4.3)
0
0
0
0
血中鉄増加
1(4.3)
1(4.3)
0
0
0
0
0
痛風
1(4.3)
0
0
0
0
0
感覚鈍麻
1(4.3)
0
0
0
0
0
結膜充血
1(4.3)
0
0
0
0
0
下痢
1(4.3)
0
0
0
0
0
嘔吐
1(4.3)
0
0
0
0
0
発疹
1(4.3)
0
0
0
0
0
関節痛
1(4.3)
0
0
0
0
0
血中コレステロール減少
1(4.3)
0
0
0
0
0
血中クレアチンホスホキナーゼ増加
1(4.3)
0
0
0
0
0
血中免疫グロブリン G 減少
1(4.3)
0
0
0
0
0
失神寸前の状態
1(4.2)
0
0
0
0
0
腹部膨満
1(4.2)
0
0
0
0
0
肛門周囲痛
1(4.2)
0
0
0
0
0
湿疹
1(4.2)
0
0
0
0
0
背部痛
1(4.2)
0
0
0
0
0
月経困難症
1(4.2)
0
0
0
0
0
血中カルシウム増加
1(4.2)
0
0
0
0
0
血中尿酸増加
1(4.2)
0
0
0
0
0
尿中蛋白陽性
1(4.2)
例数(%)、MedDRA ver.24.0
死亡に至った有害事象、重篤な有害事象及び投与中止に至った有害事象は認められなかった。
51
ゾコーバ錠 125 mg_塩野義製薬株式会社_審査報告書
53 / 82