よむ、つかう、まなぶ。
参考資料8 ヒト受精胚の作成を行う生殖補助医療研究に関する倫理指針ガイダンス(令和3年11月19日) (33 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29769.html |
| 出典情報 | ヒト受精胚等へのゲノム編集技術等を用いる研究に関する合同会議(再設置第4回 12/28)《厚生労働省》《文部科学省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
④ 提供機関の配偶子の採取及び保存に関する規則の写し
《研究機関と提供機関が同一である場合》 この場合であっても、提供機関としての立場において、第
4章第2(提供機関)に規定する基準等を満たす必要がある。このことから、④に掲げる書類を添付するこ
と。
⑤ 提供機関の倫理審査委員会における審査の過程及び結果を示す書類並びに当該機関の倫理審査委員会に
関する事項を記載した書類(様式1-1、添付資料2の様式に従って添付のこと。)
⑤に掲げる書類には、説明資料として、提供機関の倫理審査委員会の具体的な審査等の内容が分かる議
事録(速記録等)及び提供機関の倫理審査委員会の規則の写しを添付すること。
《研究機関と提供機関が同一である場合》 この場合であっても、提供機関としての立場において、第
4章第2(提供機関)に規定する基準等を満たす必要がある。このことから、提供機関としての立場から審
査した過程及び結果等が分かるように⑤に掲げる書類を添付すること。
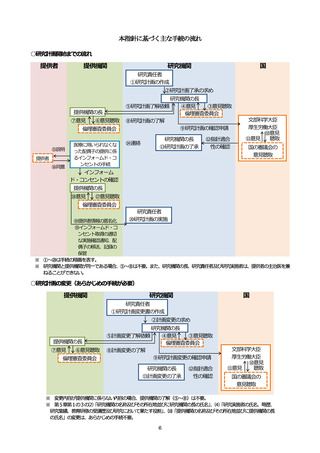
なお、文部科学省及び厚生労働省は、第1の2の⑵に掲げる書類に基づき、研究計画のこの指針に対する適合
性について確認を行う。確認の過程においては、両省が設置する審議会(有識者会議)にて審査を行うことを想
定している。両省にて確認を行った後、研究機関の長へ確認通知を送付するものとする。研究機関の長は、その
通知を受理した後、研究計画の実施を了承し、研究を実施すること。
3 研究計画書
研究計画書には、次に掲げる事項を記載するものとする。
⑴ 研究計画の名称
⑵ 研究機関の名称及びその所在地並びに研究機関の長の氏名
⑶ 研究責任者の氏名、略歴、研究業績、教育研修の受講歴及び研究において果たす役割
⑷ 研究実施者の氏名、略歴、研究業績、教育研修の受講歴及び研究において果たす役割
⑸ 研究に用いられる配偶子及びその入手方法
⑹ 研究の目的及び必要性
⑺ 研究の方法(ヒト受精胚の作成において遺伝情報改変技術等を用いる場合にあっては、研究に用いる遺
伝情報改変技術等の種類を含む。
)及び期間
⑻ 研究機関の基準に関する説明
⑼ インフォームド・コンセントに関する説明
⑽ 提供機関の名称及びその所在地並びに提供機関の長の氏名
⑾ 提供機関の基準に関する説明
⑿ 個人情報の取扱い(匿名化の方法を含む。
)
⒀ 遺伝情報の取扱い
<解説>
研究計画書(様式1-1別紙)は、科学的妥当性及び倫理的妥当性の判断(倫理審査委員会による審査、文部
科学大臣及び厚生労働大臣の確認)の対象であるとともに、研究機関が業務を実施するに当たっての根幹となる
べきものである。このため、研究責任者は、必要な情報を遺漏なく記載するとともに、同時に、誤解が生じない
よう、明確かつ分かりやすく作成すること。
⑴: 「研究計画の名称」は、研究の内容が簡潔に分かるような名称とすること。
⑵: 「研究機関の名称」は、法人又は学部、附置研究所若しくは事業所等の単位(その組織の責任者が、
「研
究機関の長」として研究の監督等を行えるもの)で、機関の正式名称を記載すること。
《研究機関と提供機関が同一である場合》 この場合、例えば、研究所と病院が同一法人内に設置されている
ときは、当該法人名を記載すること。
「所在地」は、研究を実施する場所の住所を記載すること。
「研究機関の長の氏名」は、研究機関の長の氏名及び職名を記載すること。
なお、研究機関の長は、原則として、研究責任者及び研究実施者を兼ねることはできない。ただし、研究機関
の長の業務の代行者が選任されている場合には、兼ねることができるが、その場合には、代行者の氏名及び職名
を記載すること。
33
《研究機関と提供機関が同一である場合》 この場合であっても、提供機関としての立場において、第
4章第2(提供機関)に規定する基準等を満たす必要がある。このことから、④に掲げる書類を添付するこ
と。
⑤ 提供機関の倫理審査委員会における審査の過程及び結果を示す書類並びに当該機関の倫理審査委員会に
関する事項を記載した書類(様式1-1、添付資料2の様式に従って添付のこと。)
⑤に掲げる書類には、説明資料として、提供機関の倫理審査委員会の具体的な審査等の内容が分かる議
事録(速記録等)及び提供機関の倫理審査委員会の規則の写しを添付すること。
《研究機関と提供機関が同一である場合》 この場合であっても、提供機関としての立場において、第
4章第2(提供機関)に規定する基準等を満たす必要がある。このことから、提供機関としての立場から審
査した過程及び結果等が分かるように⑤に掲げる書類を添付すること。
なお、文部科学省及び厚生労働省は、第1の2の⑵に掲げる書類に基づき、研究計画のこの指針に対する適合
性について確認を行う。確認の過程においては、両省が設置する審議会(有識者会議)にて審査を行うことを想
定している。両省にて確認を行った後、研究機関の長へ確認通知を送付するものとする。研究機関の長は、その
通知を受理した後、研究計画の実施を了承し、研究を実施すること。
3 研究計画書
研究計画書には、次に掲げる事項を記載するものとする。
⑴ 研究計画の名称
⑵ 研究機関の名称及びその所在地並びに研究機関の長の氏名
⑶ 研究責任者の氏名、略歴、研究業績、教育研修の受講歴及び研究において果たす役割
⑷ 研究実施者の氏名、略歴、研究業績、教育研修の受講歴及び研究において果たす役割
⑸ 研究に用いられる配偶子及びその入手方法
⑹ 研究の目的及び必要性
⑺ 研究の方法(ヒト受精胚の作成において遺伝情報改変技術等を用いる場合にあっては、研究に用いる遺
伝情報改変技術等の種類を含む。
)及び期間
⑻ 研究機関の基準に関する説明
⑼ インフォームド・コンセントに関する説明
⑽ 提供機関の名称及びその所在地並びに提供機関の長の氏名
⑾ 提供機関の基準に関する説明
⑿ 個人情報の取扱い(匿名化の方法を含む。
)
⒀ 遺伝情報の取扱い
<解説>
研究計画書(様式1-1別紙)は、科学的妥当性及び倫理的妥当性の判断(倫理審査委員会による審査、文部
科学大臣及び厚生労働大臣の確認)の対象であるとともに、研究機関が業務を実施するに当たっての根幹となる
べきものである。このため、研究責任者は、必要な情報を遺漏なく記載するとともに、同時に、誤解が生じない
よう、明確かつ分かりやすく作成すること。
⑴: 「研究計画の名称」は、研究の内容が簡潔に分かるような名称とすること。
⑵: 「研究機関の名称」は、法人又は学部、附置研究所若しくは事業所等の単位(その組織の責任者が、
「研
究機関の長」として研究の監督等を行えるもの)で、機関の正式名称を記載すること。
《研究機関と提供機関が同一である場合》 この場合、例えば、研究所と病院が同一法人内に設置されている
ときは、当該法人名を記載すること。
「所在地」は、研究を実施する場所の住所を記載すること。
「研究機関の長の氏名」は、研究機関の長の氏名及び職名を記載すること。
なお、研究機関の長は、原則として、研究責任者及び研究実施者を兼ねることはできない。ただし、研究機関
の長の業務の代行者が選任されている場合には、兼ねることができるが、その場合には、代行者の氏名及び職名
を記載すること。
33