よむ、つかう、まなぶ。
参考資料8 ヒト受精胚の作成を行う生殖補助医療研究に関する倫理指針ガイダンス(令和3年11月19日) (36 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29769.html |
| 出典情報 | ヒト受精胚等へのゲノム編集技術等を用いる研究に関する合同会議(再設置第4回 12/28)《厚生労働省》《文部科学省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
について記載すること。また、教育研修の内容(指針の内容の理解、生命倫理に関する一般的な知識の向上等を
図るための勉強会・講習会等)について記載すること。
⑿: 「個人情報の取扱い(匿名化の方法を含む。
)
」は、個人情報の保護の方法(匿名化の方法、匿名加工情報
又は非識別加工情報を作成する場合にはその旨、匿名化しない場合の取扱いを含む。
)について記載すること。
個人情報の取扱いについては、第5章第5の解説を参照のこと。
⒀: 「遺伝情報の取扱い」は、遺伝情報の開示に関する考え方について記載すること。
遺伝情報の取扱いについては、第5章第6の解説を参照のこと。
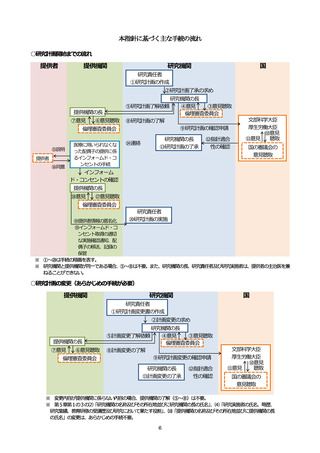
第2 研究計画の変更
⑴ 研究責任者は、研究計画(第1の3の⑵、⑷及び⑽に掲げる事項を除く。)を変更しようとするときは、
あらかじめ、研究計画変更書を作成して、研究機関の長の了承を求めるものとする。提供機関の追加に係
る変更の場合も、同様とする。
⑵ 研究機関の長は、⑴の変更の了承を求められたときは、その妥当性について当該機関の倫理審査委員会
の意見を求めるとともに、当該意見を尊重し、当該変更のこの指針に対する適合性を確認するものとする。
⑶ 研究機関の長は、⑵によりこの指針に対する適合性を確認するに当たって、研究計画の変更の内容が提
供機関に関係する場合には、当該変更について当該提供機関の長の了解を得るものとする。
⑷ 提供機関の長は、⑶の了解をするに当たっては、当該機関の倫理審査委員会の意見を聴くものとする。
⑸ 研究機関の長は、⑴の変更の了承をするに当たっては、当該変更のこの指針に対する適合性について文
部科学大臣及び厚生労働大臣の確認を受けるものとする。
⑹ ⑸の確認を受けようとする研究機関の長は、次に掲げる書類を文部科学大臣及び厚生労働大臣に提出す
るものとする。
① 研究計画変更書
② 当該変更に係る研究機関の倫理審査委員会における審査の過程及び結果を示す書類
③ ⑶に該当する場合には、当該変更に係る提供機関の倫理審査委員会における審査の過程及び結果を示
す書類
⑺ 研究機関の長は、第1の3の⑵又は⑽に掲げる事項を変更したときは、その旨を文部科学大臣及び厚生
労働大臣に届け出るものとする。
<解説>
⑴: 研究責任者は、研究計画(第1の3の⑵、⑷及び⑽に掲げる軽微な変更事項は除く。
)を変更するに当たり、
あらかじめ、様式1-2別紙の研究計画変更書を作成し、研究機関の長の了承を求めること。なお、既存の提供
機関に関する第1の3の⑽に関する変更は含めないが、提供機関の追加に係る変更の場合は、本規定に準じた手
順を行うこと。
⑵: 研究機関の長は、研究機関の倫理審査委員会に研究計画変更の妥当性について意見を聴取すること。
研究機関の倫理審査委員会は、研究計画変更の科学的妥当性及び倫理的妥当性について総合的に審査を行い、
研究機関の長に対し研究計画変更の適否、留意事項及び改善事項等の意見を提出すること。
⑶: 研究機関の長は、研究計画の変更の内容が提供機関に関係する場合(例えば、インフォームド・コンセン
ト、配偶子の移送等)には、提供機関の長の了解を得ること。
⑷: 提供機関の長は、研究計画の変更を了解するに当たっては、提供機関の倫理審査委員会の意見を聴取し、
その審査の過程及び結果を示す書類を添えて、研究機関の長に通知すること。
⑸: 研究機関の長は、倫理審査委員会の意見等を踏まえ、研究計画変更のこの指針に対する適合性について、
文部科学大臣及び厚生労働大臣の確認を受けること。
⑹: 研究機関の長は、文部科学大臣及び厚生労働大臣の確認を受けるための申請に際しては、様式1-2の申
請書を作成の上、以下の書類を文部科学省及び厚生労働省に提出すること。
・ 研究計画変更確認申請書(様式1-2)
・ 研究計画変更書(様式1-2別紙)
36
図るための勉強会・講習会等)について記載すること。
⑿: 「個人情報の取扱い(匿名化の方法を含む。
)
」は、個人情報の保護の方法(匿名化の方法、匿名加工情報
又は非識別加工情報を作成する場合にはその旨、匿名化しない場合の取扱いを含む。
)について記載すること。
個人情報の取扱いについては、第5章第5の解説を参照のこと。
⒀: 「遺伝情報の取扱い」は、遺伝情報の開示に関する考え方について記載すること。
遺伝情報の取扱いについては、第5章第6の解説を参照のこと。
第2 研究計画の変更
⑴ 研究責任者は、研究計画(第1の3の⑵、⑷及び⑽に掲げる事項を除く。)を変更しようとするときは、
あらかじめ、研究計画変更書を作成して、研究機関の長の了承を求めるものとする。提供機関の追加に係
る変更の場合も、同様とする。
⑵ 研究機関の長は、⑴の変更の了承を求められたときは、その妥当性について当該機関の倫理審査委員会
の意見を求めるとともに、当該意見を尊重し、当該変更のこの指針に対する適合性を確認するものとする。
⑶ 研究機関の長は、⑵によりこの指針に対する適合性を確認するに当たって、研究計画の変更の内容が提
供機関に関係する場合には、当該変更について当該提供機関の長の了解を得るものとする。
⑷ 提供機関の長は、⑶の了解をするに当たっては、当該機関の倫理審査委員会の意見を聴くものとする。
⑸ 研究機関の長は、⑴の変更の了承をするに当たっては、当該変更のこの指針に対する適合性について文
部科学大臣及び厚生労働大臣の確認を受けるものとする。
⑹ ⑸の確認を受けようとする研究機関の長は、次に掲げる書類を文部科学大臣及び厚生労働大臣に提出す
るものとする。
① 研究計画変更書
② 当該変更に係る研究機関の倫理審査委員会における審査の過程及び結果を示す書類
③ ⑶に該当する場合には、当該変更に係る提供機関の倫理審査委員会における審査の過程及び結果を示
す書類
⑺ 研究機関の長は、第1の3の⑵又は⑽に掲げる事項を変更したときは、その旨を文部科学大臣及び厚生
労働大臣に届け出るものとする。
<解説>
⑴: 研究責任者は、研究計画(第1の3の⑵、⑷及び⑽に掲げる軽微な変更事項は除く。
)を変更するに当たり、
あらかじめ、様式1-2別紙の研究計画変更書を作成し、研究機関の長の了承を求めること。なお、既存の提供
機関に関する第1の3の⑽に関する変更は含めないが、提供機関の追加に係る変更の場合は、本規定に準じた手
順を行うこと。
⑵: 研究機関の長は、研究機関の倫理審査委員会に研究計画変更の妥当性について意見を聴取すること。
研究機関の倫理審査委員会は、研究計画変更の科学的妥当性及び倫理的妥当性について総合的に審査を行い、
研究機関の長に対し研究計画変更の適否、留意事項及び改善事項等の意見を提出すること。
⑶: 研究機関の長は、研究計画の変更の内容が提供機関に関係する場合(例えば、インフォームド・コンセン
ト、配偶子の移送等)には、提供機関の長の了解を得ること。
⑷: 提供機関の長は、研究計画の変更を了解するに当たっては、提供機関の倫理審査委員会の意見を聴取し、
その審査の過程及び結果を示す書類を添えて、研究機関の長に通知すること。
⑸: 研究機関の長は、倫理審査委員会の意見等を踏まえ、研究計画変更のこの指針に対する適合性について、
文部科学大臣及び厚生労働大臣の確認を受けること。
⑹: 研究機関の長は、文部科学大臣及び厚生労働大臣の確認を受けるための申請に際しては、様式1-2の申
請書を作成の上、以下の書類を文部科学省及び厚生労働省に提出すること。
・ 研究計画変更確認申請書(様式1-2)
・ 研究計画変更書(様式1-2別紙)
36