よむ、つかう、まなぶ。
資料2-7-3 E2B(R3)実装ガイドに対応した市販後副作用等報告及び治験副作用等報告に関するQ&A の改正について[1.2MB] (15 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
その他重篤
15 日
不要
-
既知
死亡・死亡につ
ながるおそれ
15 日
不要
-
不要
不要
-
未知
その他重篤
死亡・死亡につ
ながるおそれ
7日
不要
不要
その他重篤
15 日
不要
不要
死亡・死亡につ
ながるおそれ
15 日
不要
不要
その他重篤
不要
不要
不要
被験薬以外の
治験使用薬
既知
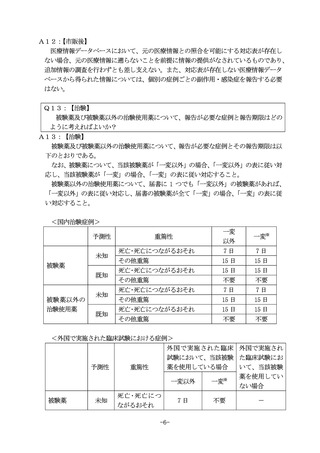
<外国における使用(臨床試験における使用を除く。
)で生じた症例>
一変以外
一変※
死亡・死亡につながるおそれ
7日
不要
その他重篤
15 日
不要
死亡・死亡につながるおそれ
15 日
不要
その他重篤
不要
不要
死亡・死亡につながるおそれ
不要
不要
その他重篤
死亡・死亡につながるおそれ
不要
不要
不要
不要
その他重篤
不要
不要
予測性
未知
被験薬
既知
被験薬以外の
治験使用薬
未知
既知
重篤性
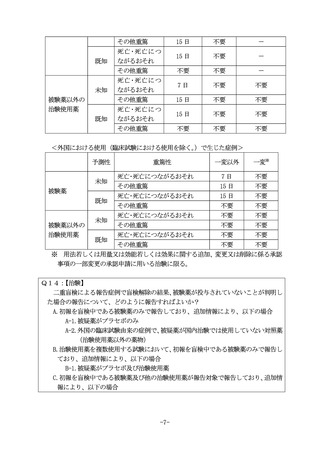
※ 用法若しくは用量又は効能若しくは効果に関する追加、変更又は削除に係る承認
事項の一部変更の承認申請に用いる治験に限る。
Q14:
【治験】
二重盲検による報告症例で盲検解除の結果、被験薬が投与されていないことが判明し
た場合の報告について、どのように報告すればよいか?
A.初報を盲検中である被験薬のみで報告しており、追加情報により、以下の場合
A-1.被疑薬がプラセボのみ
A-2.外国の臨床試験由来の症例で、被疑薬が国内治験では使用していない対照薬
(治験使用薬以外の薬物)
B.治験使用薬を複数使用する試験において、初報を盲検中である被験薬のみで報告し
ており、追加情報により、以下の場合
B-1.被疑薬がプラセボ及び治験使用薬
C.初報を盲検中である被験薬及び他の治験使用薬が報告対象で報告しており、追加情
報により、以下の場合
-7-
15 日
不要
-
既知
死亡・死亡につ
ながるおそれ
15 日
不要
-
不要
不要
-
未知
その他重篤
死亡・死亡につ
ながるおそれ
7日
不要
不要
その他重篤
15 日
不要
不要
死亡・死亡につ
ながるおそれ
15 日
不要
不要
その他重篤
不要
不要
不要
被験薬以外の
治験使用薬
既知
<外国における使用(臨床試験における使用を除く。
)で生じた症例>
一変以外
一変※
死亡・死亡につながるおそれ
7日
不要
その他重篤
15 日
不要
死亡・死亡につながるおそれ
15 日
不要
その他重篤
不要
不要
死亡・死亡につながるおそれ
不要
不要
その他重篤
死亡・死亡につながるおそれ
不要
不要
不要
不要
その他重篤
不要
不要
予測性
未知
被験薬
既知
被験薬以外の
治験使用薬
未知
既知
重篤性
※ 用法若しくは用量又は効能若しくは効果に関する追加、変更又は削除に係る承認
事項の一部変更の承認申請に用いる治験に限る。
Q14:
【治験】
二重盲検による報告症例で盲検解除の結果、被験薬が投与されていないことが判明し
た場合の報告について、どのように報告すればよいか?
A.初報を盲検中である被験薬のみで報告しており、追加情報により、以下の場合
A-1.被疑薬がプラセボのみ
A-2.外国の臨床試験由来の症例で、被疑薬が国内治験では使用していない対照薬
(治験使用薬以外の薬物)
B.治験使用薬を複数使用する試験において、初報を盲検中である被験薬のみで報告し
ており、追加情報により、以下の場合
B-1.被疑薬がプラセボ及び治験使用薬
C.初報を盲検中である被験薬及び他の治験使用薬が報告対象で報告しており、追加情
報により、以下の場合
-7-