よむ、つかう、まなぶ。
資料2-7-3 E2B(R3)実装ガイドに対応した市販後副作用等報告及び治験副作用等報告に関するQ&A の改正について[1.2MB] (52 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
なお、外国規制当局とは、上に示す米国や EU、英国だけに限らない。また、外国での
措置に関する情報を外国の提携企業から入手した場合についても、前述と同様に取り扱
うこと。
Q147:
【治験】
被験薬以外の治験使用薬に関する外国における措置報告については、どのようなもの
が対象となるか?
A147:
【治験】
当該治験での使用において、
保健衛生上の危害の発生又は拡大のおそれのある、
品質、
有効性及び安全性上の問題に基づく措置について対象とする。
4.医薬品未知・非重篤副作用定期報告
(1)報告方法
Q148:【市販後】
安全性定期報告対象医薬品ではない「その他の医薬品」について、投与経路の異な
る同一有効成分をまとめて一つの医薬品未知・非重篤副作用定期報告として報告して
もよいか?
A148:【市販後】
同一有効成分のものであっても、投与経路が異なる場合においては、別の報告書とし
て提出すること。ただし、添付文書(電子化された添付文書を含む。
)が同一である場合
においては、まとめて一つの報告書として提出して差し支えない。
Q149:【市販後】
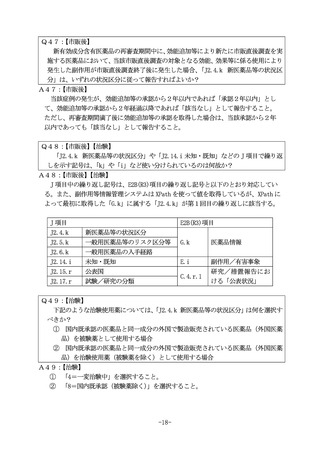
効能追加、含量違い等で複数の承認日等がある製品については、まとめて一つの医
薬品未知・非重篤副作用定期報告として報告してもよいか?
A149:【市販後】
よい。その際は、効能追加、含量違いの承認日等の中で、平成 17 年4月1日以降、最
も提出日が早くなる承認日等を報告起算日とすること。
Q150:【市販後】
一般用医薬品の場合において、配合成分が同一であるものの、分量は異なる等の製
品はまとめて一つの医薬品未知・非重篤副作用定期報告として報告してもよいか?
A150:【市販後】
配合成分が同一である製品は、まとめて一つの報告書として提出して差し支えない。
Q151:【市販後】
一般用医薬品のかぜ薬、解熱鎮痛薬等で、有効成分のうち一部の成分のみ配合成分
が異なるといった場合において、まとめて一つの医薬品未知・非重篤副作用定期報告
として報告してもよいか?
-44-
措置に関する情報を外国の提携企業から入手した場合についても、前述と同様に取り扱
うこと。
Q147:
【治験】
被験薬以外の治験使用薬に関する外国における措置報告については、どのようなもの
が対象となるか?
A147:
【治験】
当該治験での使用において、
保健衛生上の危害の発生又は拡大のおそれのある、
品質、
有効性及び安全性上の問題に基づく措置について対象とする。
4.医薬品未知・非重篤副作用定期報告
(1)報告方法
Q148:【市販後】
安全性定期報告対象医薬品ではない「その他の医薬品」について、投与経路の異な
る同一有効成分をまとめて一つの医薬品未知・非重篤副作用定期報告として報告して
もよいか?
A148:【市販後】
同一有効成分のものであっても、投与経路が異なる場合においては、別の報告書とし
て提出すること。ただし、添付文書(電子化された添付文書を含む。
)が同一である場合
においては、まとめて一つの報告書として提出して差し支えない。
Q149:【市販後】
効能追加、含量違い等で複数の承認日等がある製品については、まとめて一つの医
薬品未知・非重篤副作用定期報告として報告してもよいか?
A149:【市販後】
よい。その際は、効能追加、含量違いの承認日等の中で、平成 17 年4月1日以降、最
も提出日が早くなる承認日等を報告起算日とすること。
Q150:【市販後】
一般用医薬品の場合において、配合成分が同一であるものの、分量は異なる等の製
品はまとめて一つの医薬品未知・非重篤副作用定期報告として報告してもよいか?
A150:【市販後】
配合成分が同一である製品は、まとめて一つの報告書として提出して差し支えない。
Q151:【市販後】
一般用医薬品のかぜ薬、解熱鎮痛薬等で、有効成分のうち一部の成分のみ配合成分
が異なるといった場合において、まとめて一つの医薬品未知・非重篤副作用定期報告
として報告してもよいか?
-44-