よむ、つかう、まなぶ。
資料2-7-3 E2B(R3)実装ガイドに対応した市販後副作用等報告及び治験副作用等報告に関するQ&A の改正について[1.2MB] (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
Q99:【市販後】【治験】
Q99:【市販後】【治験】
承認日前後に発現した国内副作用について、「治験副作
承認日前後に発現した国内副作用について、「治験副作
用等報告」とすべきか「市販後副作用等報告」とすべきか 用等報告」とすべきか「市販後副作用等報告」とすべきか
は、どのように判断すればよいか?
は、どのように判断すればよいか?
A99:【市販後】【治験】
A99:【市販後】【治験】
副作用の発現日時点の当該品目の国内における被験薬の
副作用の発現日時点の当該品目の国内における被験薬の
承認状況により判断すること。
承認状況により判断すること。
(1)承認日より前に発現した副作用に関しては、施行
(1)承認日より前に発現した副作用に関しては、施行
規則第 273 条の規定に基づき「治験副作用等報告」
規則第 273 条の規定に基づき「治験副作用等報告」
として報告すること。
として報告すること。
(2)承認日より前に発現した副作用に関する追加情報
(2)承認日より前に発現した副作用に関する追加情報
は、「治験副作用等報告」として追加報告をするこ
は、「治験副作用等報告」として追加報告をするこ
と。その際、「J2.13.r.3 開発相」には、「8=その
と。その際、「J2.13.r.3 開発相」には、「8=その
他」を記載し、「J2.11 その他参考事項等」には、
他」を記載し、「J2.11 その他参考事項等」には、
「承認後」の文字及び「販売名」をそれぞれ記載す
「承認後」の文字及び「販売名」をそれぞれ記載す
ること。
ること。
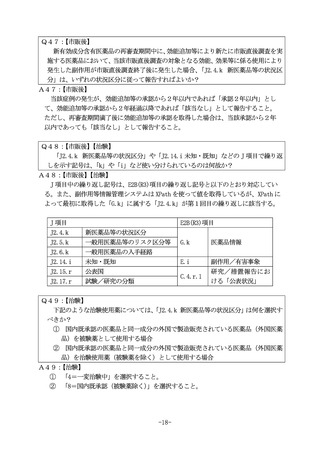
(3)承認日以降に発現した副作用に関しては、施行規
(3)承認日以降に発現した副作用に関しては、施行規
則第 228 条の 20 の規定に基づき「市販後副作用等報
則第 228 条の 20 の規定に基づき「市販後副作用等報
告」として報告すること。また、承認日より前に
告」として報告すること。また、承認日より前に
「治験副作用等報告」として報告した患者に承認日
「治験副作用等報告」として報告した患者に承認日
以降に新たに発現した別の副作用に関する情報も
以降に新たに発現した別の副作用に関する情報も
「市販後副作用等報告」として第一報を報告し、そ
「市販後副作用等報告」として第一報を報告し、そ
の際、Q&A60及び61を参考に必要事項を記載
の際、Q&A62及び63を参考に必要事項を記載
すること。なお、(2)の追加報告と承認日以降に
すること。なお、(2)の追加報告と承認日以降に
新たに発現した別の副作用の報告を同時に報告する
新たに発現した別の副作用の報告を同時に報告する
場合、「市販後副作用等報告」としてまとめて報告
場合、「市販後副作用等報告」としてまとめて報告
Q99:【市販後】【治験】
承認日前後に発現した国内副作用について、「治験副作
承認日前後に発現した国内副作用について、「治験副作
用等報告」とすべきか「市販後副作用等報告」とすべきか 用等報告」とすべきか「市販後副作用等報告」とすべきか
は、どのように判断すればよいか?
は、どのように判断すればよいか?
A99:【市販後】【治験】
A99:【市販後】【治験】
副作用の発現日時点の当該品目の国内における被験薬の
副作用の発現日時点の当該品目の国内における被験薬の
承認状況により判断すること。
承認状況により判断すること。
(1)承認日より前に発現した副作用に関しては、施行
(1)承認日より前に発現した副作用に関しては、施行
規則第 273 条の規定に基づき「治験副作用等報告」
規則第 273 条の規定に基づき「治験副作用等報告」
として報告すること。
として報告すること。
(2)承認日より前に発現した副作用に関する追加情報
(2)承認日より前に発現した副作用に関する追加情報
は、「治験副作用等報告」として追加報告をするこ
は、「治験副作用等報告」として追加報告をするこ
と。その際、「J2.13.r.3 開発相」には、「8=その
と。その際、「J2.13.r.3 開発相」には、「8=その
他」を記載し、「J2.11 その他参考事項等」には、
他」を記載し、「J2.11 その他参考事項等」には、
「承認後」の文字及び「販売名」をそれぞれ記載す
「承認後」の文字及び「販売名」をそれぞれ記載す
ること。
ること。
(3)承認日以降に発現した副作用に関しては、施行規
(3)承認日以降に発現した副作用に関しては、施行規
則第 228 条の 20 の規定に基づき「市販後副作用等報
則第 228 条の 20 の規定に基づき「市販後副作用等報
告」として報告すること。また、承認日より前に
告」として報告すること。また、承認日より前に
「治験副作用等報告」として報告した患者に承認日
「治験副作用等報告」として報告した患者に承認日
以降に新たに発現した別の副作用に関する情報も
以降に新たに発現した別の副作用に関する情報も
「市販後副作用等報告」として第一報を報告し、そ
「市販後副作用等報告」として第一報を報告し、そ
の際、Q&A60及び61を参考に必要事項を記載
の際、Q&A62及び63を参考に必要事項を記載
すること。なお、(2)の追加報告と承認日以降に
すること。なお、(2)の追加報告と承認日以降に
新たに発現した別の副作用の報告を同時に報告する
新たに発現した別の副作用の報告を同時に報告する
場合、「市販後副作用等報告」としてまとめて報告
場合、「市販後副作用等報告」としてまとめて報告