よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1.3MB] (21 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
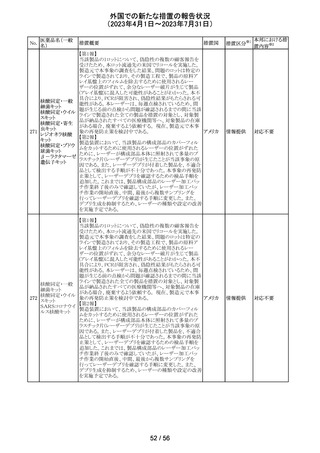
外国での新たな措置の報告状況
(2023年4月1日~2023年7月31日)
措置区分※1
本邦における措
置内容※2
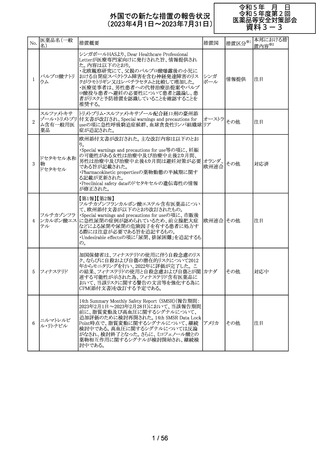
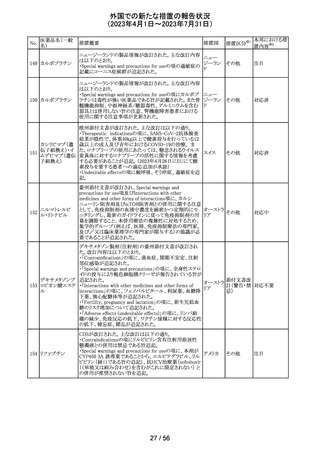
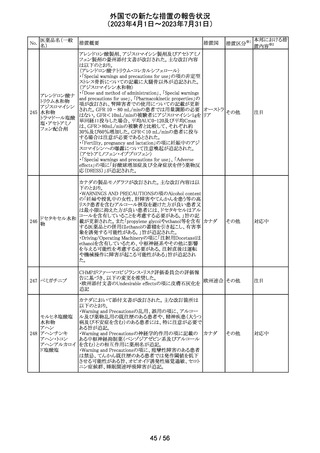
116 ガバペンチン
Company Core Data Sheet(CCDS)が改訂され、以下の内
容が追記された。
・Special warnings and precautions for useの乱用と依存の
項に、 ガバペンチンの乱用リスクが高い薬物乱用中又は
薬物乱用歴のある患者への投与は注意が必要である。投
与中の患者では、耐性発現、用量漸増、薬物探索行等の
乱用・依存の徴候及び症状について監視する必要がある。
旨を追記。
・Pharmacodynamic propertiesの項に、以下の試験結果が
追記された。
薬物依存のない健康なレクリエーショナルオピオイド使用
者(被験者42名、年齢中央値34歳)を対象に、ガバペンチ
アメリカ
ン(600mg又は1200mg)とオキシコドン(20mg速放剤)を併
用した場合の乱用の可能性がオキシコドン単独と同等かど
うかを無作為二重盲検単回クロスオーバー試験で検討し
た。主要評価項目は、視覚的評価尺度(VAS)を用いた薬
物嗜好性であった。一次解析では、オキシコドンと併用した
ガバペンチン600mg、1200mgともに、オキシコドン単剤より
大きな薬物嗜好性を示した。二次解析では、ガバペンチン
単剤600mg、1200mgともに、オキシコドン単剤と比較して有
意に低い薬物嗜好効果が示された。ガバペンチン600mg
単独ではプラセボと同程度の薬物嗜好効果を示し、
1200mg単独ではプラセボと同程度とは確認できないより大
きな薬物嗜好効果を示した。
その他
対応中
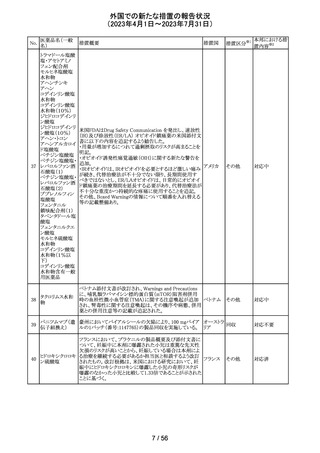
117 ドンペリドン
フィリピン規制当局(FDA Philippines)は、ドンペリドンのス
テークホルダー会議において、ドンペリドンの添付文書 の
Contraindications 及びSpecial warnings and precautions
イギリス
に心血管作用のリスク増大に関する情報を反映するよう指
示した。また、 本リスクに伴い、ドンペリドンの分類がOTC
から処方薬へ変更となった。
添付文書改
訂(警告・禁 注目
忌)
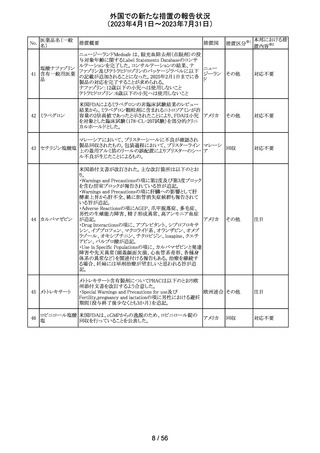
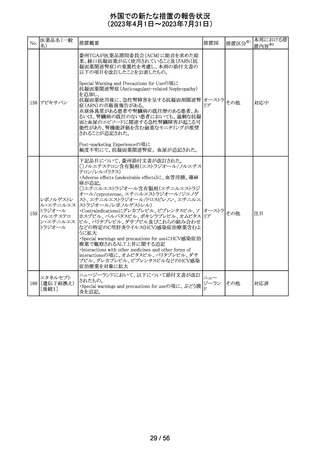
118 イブルチニブ
米国添付文書が改訂された。主な改訂内容は以下のとお
り。
・米国にてAccelerated approvalの状態であったマントル細
胞リンパ腫及び辺縁帯リンパ腫の適応症について、前治療
歴のないマントル細胞リンパ腫患者を対象とした第Ⅲ相
アメリカ
SHINE試験(PCI-32765MCL3002)で臨床的有用性が示さ
れることが承認継続の条件とされたものの、第Ⅲ相試験の
結果は完全承認を支持するには不十分として、自主的な
取り下げに伴い削除された。
・取り下げに伴い560mg剤形が削除された。
その他
対応不要
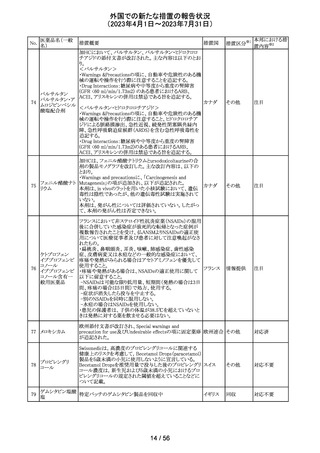
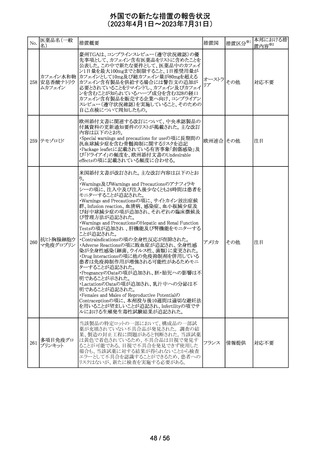
119 ダイズ油
【第1報】
大豆油を有効成分とする静注用脂肪乳剤の米国添付文書
が改訂された。主な改訂は以下のとおり。
・Warnings and Precautionsに以下の追記
-新生児及び乳児における脂質エマルジョンの急速注入に
ついて、市販後に呼吸困難、代謝性アシドーシス、死亡な
どの重篤な副作用が報告されており、一般的に高トリグリセ
リド血症が報告されている旨
-肺水腫又は心不全の患者の体液状態を注意深くモニ
ターする旨
アメリカ
-体液及び電解質の状態、血清浸透圧、血糖、肝臓及び
腎臓の機能、血球数 (血小板を含む)、並びに凝固パラメー
ターをモニターする旨
・Adverse Reactionsに新生児及び乳児における脂質エマ
ルジョン静脈内急速注入による副作用について追記
【第2報】
ダイズ油を有効成分とする静注用脂肪乳剤(第1報と別品
目)の米国添付文書について、第1報と同様の使用上の注
意改訂情報を公表したとの情報を入手した。
その他
注目
No.
医薬品名(一般
名)
措置概要
措置国
21 / 56
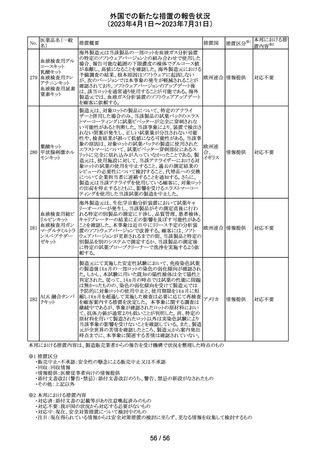
(2023年4月1日~2023年7月31日)
措置区分※1
本邦における措
置内容※2
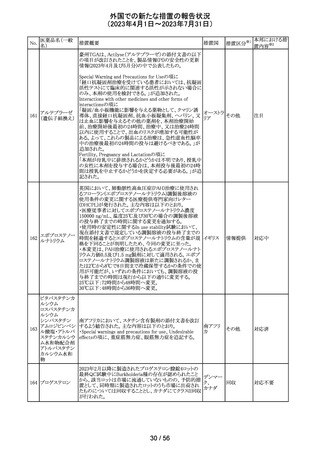
116 ガバペンチン
Company Core Data Sheet(CCDS)が改訂され、以下の内
容が追記された。
・Special warnings and precautions for useの乱用と依存の
項に、 ガバペンチンの乱用リスクが高い薬物乱用中又は
薬物乱用歴のある患者への投与は注意が必要である。投
与中の患者では、耐性発現、用量漸増、薬物探索行等の
乱用・依存の徴候及び症状について監視する必要がある。
旨を追記。
・Pharmacodynamic propertiesの項に、以下の試験結果が
追記された。
薬物依存のない健康なレクリエーショナルオピオイド使用
者(被験者42名、年齢中央値34歳)を対象に、ガバペンチ
アメリカ
ン(600mg又は1200mg)とオキシコドン(20mg速放剤)を併
用した場合の乱用の可能性がオキシコドン単独と同等かど
うかを無作為二重盲検単回クロスオーバー試験で検討し
た。主要評価項目は、視覚的評価尺度(VAS)を用いた薬
物嗜好性であった。一次解析では、オキシコドンと併用した
ガバペンチン600mg、1200mgともに、オキシコドン単剤より
大きな薬物嗜好性を示した。二次解析では、ガバペンチン
単剤600mg、1200mgともに、オキシコドン単剤と比較して有
意に低い薬物嗜好効果が示された。ガバペンチン600mg
単独ではプラセボと同程度の薬物嗜好効果を示し、
1200mg単独ではプラセボと同程度とは確認できないより大
きな薬物嗜好効果を示した。
その他
対応中
117 ドンペリドン
フィリピン規制当局(FDA Philippines)は、ドンペリドンのス
テークホルダー会議において、ドンペリドンの添付文書 の
Contraindications 及びSpecial warnings and precautions
イギリス
に心血管作用のリスク増大に関する情報を反映するよう指
示した。また、 本リスクに伴い、ドンペリドンの分類がOTC
から処方薬へ変更となった。
添付文書改
訂(警告・禁 注目
忌)
118 イブルチニブ
米国添付文書が改訂された。主な改訂内容は以下のとお
り。
・米国にてAccelerated approvalの状態であったマントル細
胞リンパ腫及び辺縁帯リンパ腫の適応症について、前治療
歴のないマントル細胞リンパ腫患者を対象とした第Ⅲ相
アメリカ
SHINE試験(PCI-32765MCL3002)で臨床的有用性が示さ
れることが承認継続の条件とされたものの、第Ⅲ相試験の
結果は完全承認を支持するには不十分として、自主的な
取り下げに伴い削除された。
・取り下げに伴い560mg剤形が削除された。
その他
対応不要
119 ダイズ油
【第1報】
大豆油を有効成分とする静注用脂肪乳剤の米国添付文書
が改訂された。主な改訂は以下のとおり。
・Warnings and Precautionsに以下の追記
-新生児及び乳児における脂質エマルジョンの急速注入に
ついて、市販後に呼吸困難、代謝性アシドーシス、死亡な
どの重篤な副作用が報告されており、一般的に高トリグリセ
リド血症が報告されている旨
-肺水腫又は心不全の患者の体液状態を注意深くモニ
ターする旨
アメリカ
-体液及び電解質の状態、血清浸透圧、血糖、肝臓及び
腎臓の機能、血球数 (血小板を含む)、並びに凝固パラメー
ターをモニターする旨
・Adverse Reactionsに新生児及び乳児における脂質エマ
ルジョン静脈内急速注入による副作用について追記
【第2報】
ダイズ油を有効成分とする静注用脂肪乳剤(第1報と別品
目)の米国添付文書について、第1報と同様の使用上の注
意改訂情報を公表したとの情報を入手した。
その他
注目
No.
医薬品名(一般
名)
措置概要
措置国
21 / 56