よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1.3MB] (53 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
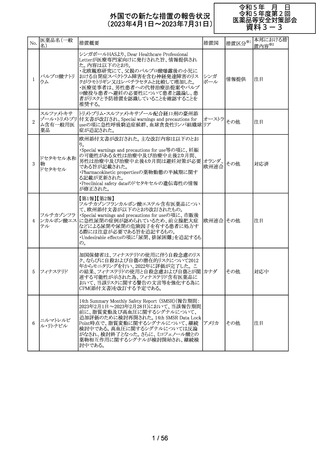
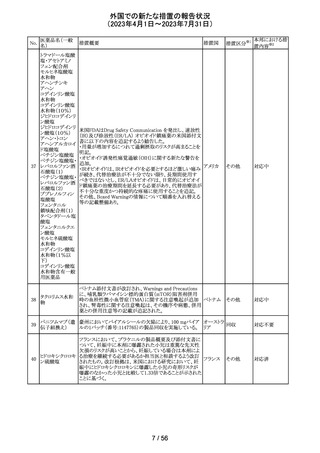
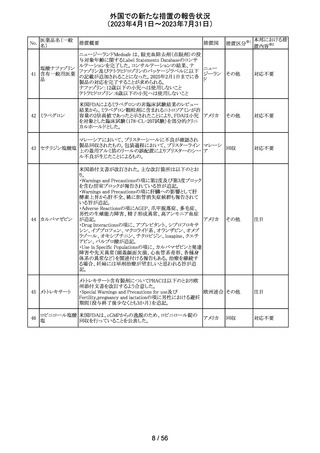
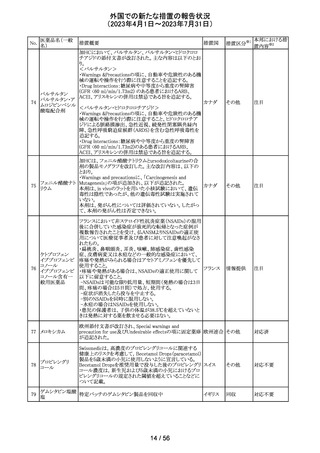
外国での新たな措置の報告状況
(2023年4月1日~2023年7月31日)
No.
医薬品名(一般
名)
措置概要
措置国
措置区分※1
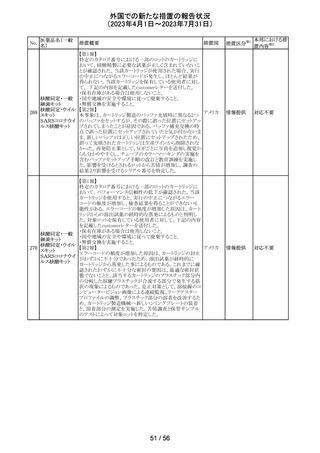
【第1報】
製造元において、当該製品の特定ロットについて、ブロッキ
ング試薬の濃度が不足していることが確認された。 検体中
に含まれる干渉物質が十分に遮断されていないことによっ
て引き起こされる、再現性のある偽高値の結果を示した。
製造元による社内調査の結果、患者検体の約5%以下が当
該不具合の影響を受けることが確認された。 当該試薬で
検査した患者検体の測定結果は、約20~40%高くなる可能
性がある。また、この増加の程度は検体中に存在する干渉
物質の量により異なる可能性がある。 誤った高いp2PSAの
測定結果を用いて計算されたプロステートヘルスインデック
スも同様に偽高値となる。これは、前立腺癌と前立腺の良
性疾患との鑑別において、臨床的特異性が低下する可能
性があり、これにより不必要なフォローアップ検査や前立腺
生検が行われる可能性があるが、精度管理用試料測定の
結果には影響がない。 製造元は、当該ロットの販売を中止
し、以下の内容について、顧客への情報提供を実施する。
・当該製品の使用を中止し、対象ロットの残りの試薬パック
は全て廃棄すること。
・過去の測定結果のレビューが必要かどうか、本通知文を
検査室とメディカルダイレクターに共有することを推奨する
前立腺特異抗原
アメリカ、
273
こと。
情報提供
前駆体キット
欧州連合
・代替品への交換については、担当者へ連絡すること。
【第2報】
当該不具合の根本原因は、充填製造所の製造工程におけ
るオペレーターによる作業の誤りであると特定した。緩衝液
調製におけるブロッキング剤必要量の算出と記録を行う
ワークシートの入力に誤りがあり、ブロッキング剤の添加量
が正しく計算されずに緩衝液が調製され、当該試薬パック
が製造されたことが原因と特定した。当該担当オペレー
ターが手順に従わなかったことが直接原因であり、さらに検
証者による濃度の確認要件について手順の記載が不適切
であったため、オペレーターの入力内容に依存して確認を
実施したことが、当該事象の原因と考えられる。製造元に
おいて、以下の3点を再発予防策として実施する。
1)手順書を更新し、検証者による濃度の確認要件を明確に
手順に含める。
2)原料の使用時点で濃度情報を利用できるようにするた
め、原料試薬の試験成績書を記録に含める事を要求する
よう関連手順を更新するか、あるいは原料濃度情報を基幹
システムを利用して保存する。
3)業務作業手順を改訂し、濃度を含む全ての情報を確認
するためのレビュープロセスが明確になるよう変更する。
53 / 56
本邦における措
置内容※2
対応不要
(2023年4月1日~2023年7月31日)
No.
医薬品名(一般
名)
措置概要
措置国
措置区分※1
【第1報】
製造元において、当該製品の特定ロットについて、ブロッキ
ング試薬の濃度が不足していることが確認された。 検体中
に含まれる干渉物質が十分に遮断されていないことによっ
て引き起こされる、再現性のある偽高値の結果を示した。
製造元による社内調査の結果、患者検体の約5%以下が当
該不具合の影響を受けることが確認された。 当該試薬で
検査した患者検体の測定結果は、約20~40%高くなる可能
性がある。また、この増加の程度は検体中に存在する干渉
物質の量により異なる可能性がある。 誤った高いp2PSAの
測定結果を用いて計算されたプロステートヘルスインデック
スも同様に偽高値となる。これは、前立腺癌と前立腺の良
性疾患との鑑別において、臨床的特異性が低下する可能
性があり、これにより不必要なフォローアップ検査や前立腺
生検が行われる可能性があるが、精度管理用試料測定の
結果には影響がない。 製造元は、当該ロットの販売を中止
し、以下の内容について、顧客への情報提供を実施する。
・当該製品の使用を中止し、対象ロットの残りの試薬パック
は全て廃棄すること。
・過去の測定結果のレビューが必要かどうか、本通知文を
検査室とメディカルダイレクターに共有することを推奨する
前立腺特異抗原
アメリカ、
273
こと。
情報提供
前駆体キット
欧州連合
・代替品への交換については、担当者へ連絡すること。
【第2報】
当該不具合の根本原因は、充填製造所の製造工程におけ
るオペレーターによる作業の誤りであると特定した。緩衝液
調製におけるブロッキング剤必要量の算出と記録を行う
ワークシートの入力に誤りがあり、ブロッキング剤の添加量
が正しく計算されずに緩衝液が調製され、当該試薬パック
が製造されたことが原因と特定した。当該担当オペレー
ターが手順に従わなかったことが直接原因であり、さらに検
証者による濃度の確認要件について手順の記載が不適切
であったため、オペレーターの入力内容に依存して確認を
実施したことが、当該事象の原因と考えられる。製造元に
おいて、以下の3点を再発予防策として実施する。
1)手順書を更新し、検証者による濃度の確認要件を明確に
手順に含める。
2)原料の使用時点で濃度情報を利用できるようにするた
め、原料試薬の試験成績書を記録に含める事を要求する
よう関連手順を更新するか、あるいは原料濃度情報を基幹
システムを利用して保存する。
3)業務作業手順を改訂し、濃度を含む全ての情報を確認
するためのレビュープロセスが明確になるよう変更する。
53 / 56
本邦における措
置内容※2
対応不要