よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1.3MB] (24 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
外国での新たな措置の報告状況
(2023年4月1日~2023年7月31日)
No.
130
131
措置区分※1
本邦における措
置内容※2
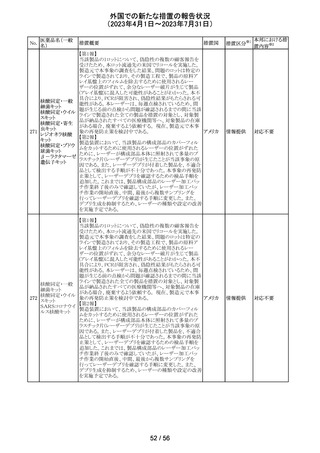
ニルマトレルビ
ル・リトナビル
本剤の16th Summary Monthly Safety Report (SMSR)(報
告期間:2023年4月1日~2023年4月30日)を入手したもの。
当該報告期間中、スティーヴンス・ジョンソン症候群(SJS)
及び中毒性表皮壊死融解症(TEN)のシグナルが検討開 アメリカ
始された。16th SMSR Data Lock Point後、SJS及びTENの
シグナルは検討終了され、特定されたリスクだが、重要では
ないとされた。
その他
対応済
ニルマトレルビ
ル・リトナビル
米国FDA承認による米国添付文書作成に伴い、米国ファク
トシートが改訂された。主な内容は以下の通り。
・Boxed Warningが追加され、強力なCYP3A阻害剤であるリ
トナビルが含まれており、特定の併用薬の曝露量が増加
し、重篤な、生命を脅かす、あるいは致命的な事象を引き
起こす可能性があること、本剤を処方する前に、患者が服
用するすべての薬剤を確認し、併用薬の用量調節、休薬
アメリカ
あるいはモニタリングの必要性を判断すること、本剤による
入院や死亡の減少というベネフィットを考慮し、個々の患者
に対する相互作用のリスクを管理できるかについて検討す
ること、が記載された。
・Drug interactionsの項にベラパミルを追記。
・Advers Reactionsの項に、高血圧、Stevens-Johnson
syndrome(SJS)、Toxic epidermal necrolysis (TEN)が追記。
添付文書改
訂(警告・禁 対応済
忌)
医薬品名(一般
名)
措置概要
措置国
エジプト及びサウジアラビアにおいて、外箱ラベルに表示さ
れた注意喚起内容が変更された。変更内容は以下のとお
り。
・「本製品は、処方された通りにのみ使用する必要がある。
エジプト、
フェンタニルクエ それ以外の人がこの製品を使用した場合、その人の健康
132
サウジア その他
ン酸塩
に重大な危険を及ぼす可能性がある。」から「持続的な癌
ラビア
性疼痛のために、すでに他のオピオイド薬を毎日服用して
いる患者にのみ使用すること。それ以外の人が本製品を使
用した場合、重大な危害が発生し、命に関わる可能性があ
る。」に変更。
対応済
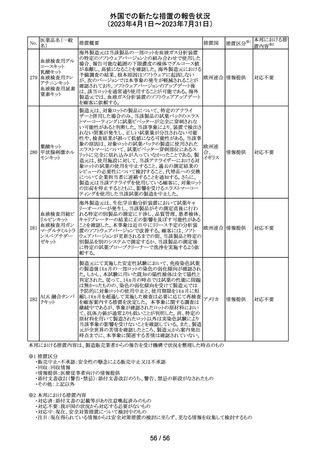
インスリングラルギンの米国添付文書が改訂された。主な
改訂内容は以下のとおり。
・「Adverse reactions」の項に、誤投与による低血糖症が追
記された。
・「Use in specific populations」の「Pregnancy」の項に、妊娠
インスリン グラル
前糖尿病患者では妊娠中に低血糖および高血糖がより頻
133 ギン(遺伝子組換
アメリカ
繁に発生する旨が追記された。
え)[後続2]
・「Use in specific populations」の「Pediatric use」の項に、小
児を対象とした臨床試験結果が追記された。
・「Use in specific populations」の「Geriatric use」の項に、65
歳以上の患者と若年成人患者間で安全性または有効性の
差異はなかった旨が追記された。
その他
注目
米国FDAは、無菌性保証欠如のためフェニレフリン/塩化
トロピカミド・フェ
ナトリウム含有250mLバッグ製剤について、クラスⅡの自主 アメリカ
ニレフリン塩酸塩
回収を実施していると公表した。
回収
対応不要
米国FDAは、製品カートン内に誤った製品が見つかったた
トロピカミド・フェ めフェニレフリン塩酸塩/デキストロメトルファン/グアイフェ
135
アメリカ
ニレフリン塩酸塩 ネシン小児用製剤について、クラスⅠの自主回収を実施し
ていると公表した。
回収
対応不要
134
24 / 56
(2023年4月1日~2023年7月31日)
No.
130
131
措置区分※1
本邦における措
置内容※2
ニルマトレルビ
ル・リトナビル
本剤の16th Summary Monthly Safety Report (SMSR)(報
告期間:2023年4月1日~2023年4月30日)を入手したもの。
当該報告期間中、スティーヴンス・ジョンソン症候群(SJS)
及び中毒性表皮壊死融解症(TEN)のシグナルが検討開 アメリカ
始された。16th SMSR Data Lock Point後、SJS及びTENの
シグナルは検討終了され、特定されたリスクだが、重要では
ないとされた。
その他
対応済
ニルマトレルビ
ル・リトナビル
米国FDA承認による米国添付文書作成に伴い、米国ファク
トシートが改訂された。主な内容は以下の通り。
・Boxed Warningが追加され、強力なCYP3A阻害剤であるリ
トナビルが含まれており、特定の併用薬の曝露量が増加
し、重篤な、生命を脅かす、あるいは致命的な事象を引き
起こす可能性があること、本剤を処方する前に、患者が服
用するすべての薬剤を確認し、併用薬の用量調節、休薬
アメリカ
あるいはモニタリングの必要性を判断すること、本剤による
入院や死亡の減少というベネフィットを考慮し、個々の患者
に対する相互作用のリスクを管理できるかについて検討す
ること、が記載された。
・Drug interactionsの項にベラパミルを追記。
・Advers Reactionsの項に、高血圧、Stevens-Johnson
syndrome(SJS)、Toxic epidermal necrolysis (TEN)が追記。
添付文書改
訂(警告・禁 対応済
忌)
医薬品名(一般
名)
措置概要
措置国
エジプト及びサウジアラビアにおいて、外箱ラベルに表示さ
れた注意喚起内容が変更された。変更内容は以下のとお
り。
・「本製品は、処方された通りにのみ使用する必要がある。
エジプト、
フェンタニルクエ それ以外の人がこの製品を使用した場合、その人の健康
132
サウジア その他
ン酸塩
に重大な危険を及ぼす可能性がある。」から「持続的な癌
ラビア
性疼痛のために、すでに他のオピオイド薬を毎日服用して
いる患者にのみ使用すること。それ以外の人が本製品を使
用した場合、重大な危害が発生し、命に関わる可能性があ
る。」に変更。
対応済
インスリングラルギンの米国添付文書が改訂された。主な
改訂内容は以下のとおり。
・「Adverse reactions」の項に、誤投与による低血糖症が追
記された。
・「Use in specific populations」の「Pregnancy」の項に、妊娠
インスリン グラル
前糖尿病患者では妊娠中に低血糖および高血糖がより頻
133 ギン(遺伝子組換
アメリカ
繁に発生する旨が追記された。
え)[後続2]
・「Use in specific populations」の「Pediatric use」の項に、小
児を対象とした臨床試験結果が追記された。
・「Use in specific populations」の「Geriatric use」の項に、65
歳以上の患者と若年成人患者間で安全性または有効性の
差異はなかった旨が追記された。
その他
注目
米国FDAは、無菌性保証欠如のためフェニレフリン/塩化
トロピカミド・フェ
ナトリウム含有250mLバッグ製剤について、クラスⅡの自主 アメリカ
ニレフリン塩酸塩
回収を実施していると公表した。
回収
対応不要
米国FDAは、製品カートン内に誤った製品が見つかったた
トロピカミド・フェ めフェニレフリン塩酸塩/デキストロメトルファン/グアイフェ
135
アメリカ
ニレフリン塩酸塩 ネシン小児用製剤について、クラスⅠの自主回収を実施し
ていると公表した。
回収
対応不要
134
24 / 56