よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1.3MB] (38 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
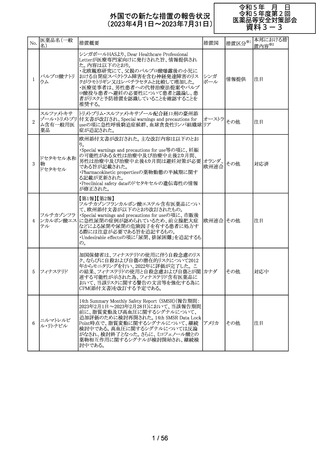
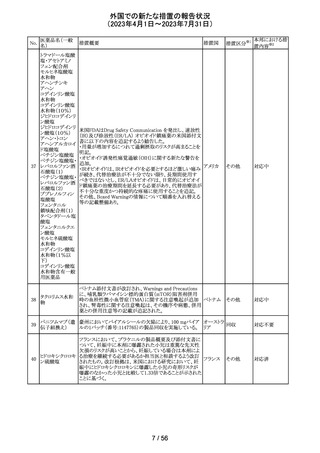
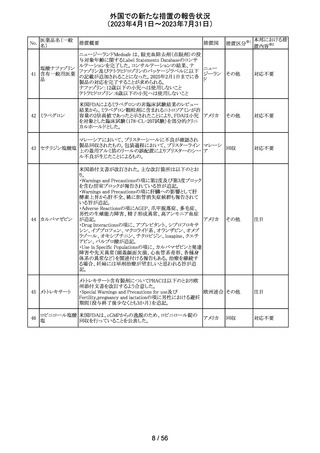
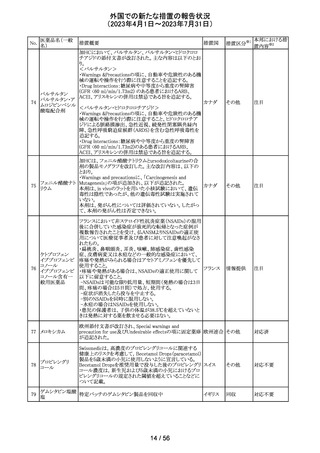
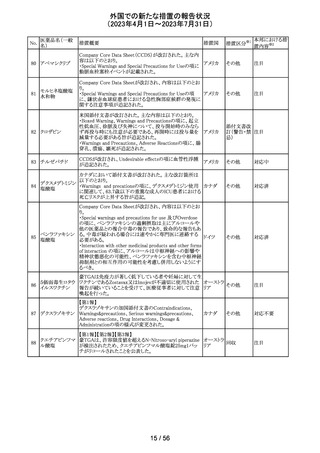
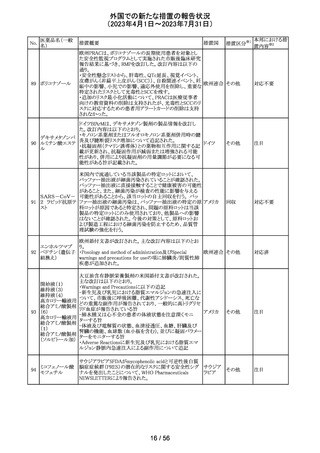
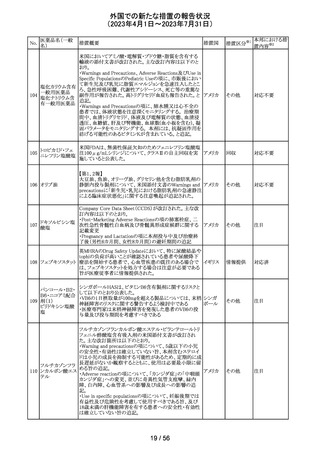
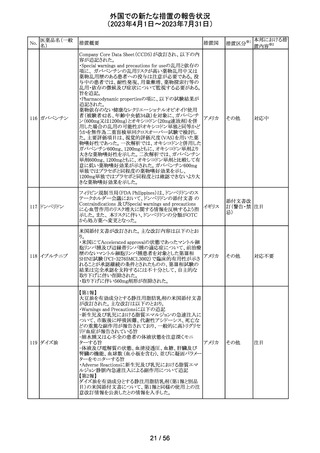
外国での新たな措置の報告状況
(2023年4月1日~2023年7月31日)
No.
医薬品名(一般
名)
措置概要
措置国
措置区分※1
本邦における措
置内容※2
人全血液
人全血液(放射
線照射)
人赤血球液
人赤血球液(放
射線照射)
洗浄人赤血球液
洗浄人赤血球液
(放射線照射)
解凍人赤血球液
解凍人赤血球液
(放射線照射)
207
合成血
合成血(放射線
照射)
新鮮凍結人血漿
人血小板濃厚液
人血小板濃厚液
(放射線照射)
人血小板濃厚液
HLA
人血小板濃厚液
HLA(放射線照
射)
【第1報】
豪州において、新たにタトゥーを入れた者は4カ月の供血
延期が必要とされていたが、安全性が確認されたため、認
可施設でタトゥーを入れた供血者の供血延期期間が7日間 オーストラ
その他
に短縮された。なお、無認可施設及び海外でタトゥーを入 リア
れた場合の供血延期期間は4カ月のままとしている。
【第2報】
措置内容に変更なし。企業の見解が報告された。
注目
208 カルボプラチン
豪州添付文書が改訂された。主な改訂内容は以下のとお
り。
オーストラ
その他
・Special warnings and precautions for useの項にコーニス リア
症候群に関する注意喚起が追記された。
注目
209 パルボシクリブ
欧州添付文書が改訂された。主な改訂内容は以下のとお
り。
・Special warnings and precautions for use及びUndesirable オランダ その他
effectsの項に.静脈血栓塞栓症及び手掌・足底発赤知覚不
全症候群が追記された。
対応中
エジプト規制当局(EDA)は添付文書に尿路感染症及び憩
室炎を追加することを2022年5月19日に承認したが、2023
ウパダシチニブ水
210
年12月以前の添付文書に反映されていないことを考慮し エジプト
和物
て、当該事象の追加するDirect Healthcare Professional
Communication(DHPC)のレターが発出される。
その他
対応済
デソゲストレル/エチニルエストラジオール配合剤及び
etonogestrel/エチニルエストラジオール配合剤の豪州添付
文書が改訂された。主な内容は以下のとおり。
レボノルゲストレ
・Contraindicationsにグレカプレビル、ピブレンタスビル等
ル・エチニルエス
の特定のC型肝炎ウイルス(HCV)感染症治療薬を含むよう
トラジオール
オーストラ
211
に拡大
その他
ノルエチステロ
リア
・Special warnings and precautions for useにHCV医薬品と
ン・エチニルエス
の併用時のALT上昇に関する追記
トラジオール
・Interactions with other medicines and other forms of
interactionsの項に、HCV治療前に、HCV感染症治療薬の
添付文書を確認し代替避妊方法を検討する旨追記
注目
ヒドロコルチゾン・
ヒドロコルチゾンコハク酸ナトリウム静注用製剤の豪州添付
フラジオマイシン
文書が改訂された。主な内容は以下のとおり。
オーストラ
212 配合剤
その他
Special warnings and precautions for useに腫瘍崩壊症候 リア
大腸菌死菌・ヒド
群に関して追記された。
ロコルチゾン
対応不要
38 / 56
(2023年4月1日~2023年7月31日)
No.
医薬品名(一般
名)
措置概要
措置国
措置区分※1
本邦における措
置内容※2
人全血液
人全血液(放射
線照射)
人赤血球液
人赤血球液(放
射線照射)
洗浄人赤血球液
洗浄人赤血球液
(放射線照射)
解凍人赤血球液
解凍人赤血球液
(放射線照射)
207
合成血
合成血(放射線
照射)
新鮮凍結人血漿
人血小板濃厚液
人血小板濃厚液
(放射線照射)
人血小板濃厚液
HLA
人血小板濃厚液
HLA(放射線照
射)
【第1報】
豪州において、新たにタトゥーを入れた者は4カ月の供血
延期が必要とされていたが、安全性が確認されたため、認
可施設でタトゥーを入れた供血者の供血延期期間が7日間 オーストラ
その他
に短縮された。なお、無認可施設及び海外でタトゥーを入 リア
れた場合の供血延期期間は4カ月のままとしている。
【第2報】
措置内容に変更なし。企業の見解が報告された。
注目
208 カルボプラチン
豪州添付文書が改訂された。主な改訂内容は以下のとお
り。
オーストラ
その他
・Special warnings and precautions for useの項にコーニス リア
症候群に関する注意喚起が追記された。
注目
209 パルボシクリブ
欧州添付文書が改訂された。主な改訂内容は以下のとお
り。
・Special warnings and precautions for use及びUndesirable オランダ その他
effectsの項に.静脈血栓塞栓症及び手掌・足底発赤知覚不
全症候群が追記された。
対応中
エジプト規制当局(EDA)は添付文書に尿路感染症及び憩
室炎を追加することを2022年5月19日に承認したが、2023
ウパダシチニブ水
210
年12月以前の添付文書に反映されていないことを考慮し エジプト
和物
て、当該事象の追加するDirect Healthcare Professional
Communication(DHPC)のレターが発出される。
その他
対応済
デソゲストレル/エチニルエストラジオール配合剤及び
etonogestrel/エチニルエストラジオール配合剤の豪州添付
文書が改訂された。主な内容は以下のとおり。
レボノルゲストレ
・Contraindicationsにグレカプレビル、ピブレンタスビル等
ル・エチニルエス
の特定のC型肝炎ウイルス(HCV)感染症治療薬を含むよう
トラジオール
オーストラ
211
に拡大
その他
ノルエチステロ
リア
・Special warnings and precautions for useにHCV医薬品と
ン・エチニルエス
の併用時のALT上昇に関する追記
トラジオール
・Interactions with other medicines and other forms of
interactionsの項に、HCV治療前に、HCV感染症治療薬の
添付文書を確認し代替避妊方法を検討する旨追記
注目
ヒドロコルチゾン・
ヒドロコルチゾンコハク酸ナトリウム静注用製剤の豪州添付
フラジオマイシン
文書が改訂された。主な内容は以下のとおり。
オーストラ
212 配合剤
その他
Special warnings and precautions for useに腫瘍崩壊症候 リア
大腸菌死菌・ヒド
群に関して追記された。
ロコルチゾン
対応不要
38 / 56