参考資料1-7 浜口班の議論における参考資料(令和3年10月25日開催)(令和3年度第6回安全技術調査会参考資料1-2) (104 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27504.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会安全技術調査会(令和4年度第2回 8/23)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
た(接種間隔 5 週以下が本剤群の 93.7%)にも関わらず、他の部分集団と比べて高い中和抗体価が認め
られたことについては、変異株の影響(7.R.2.4 項参照)も含め、製造販売後も引き続き情報収集が必要
と考える。
7.R.2.2.1.3 接種間隔が有効性に及ぼす影響について
接種間隔が有効性に及ぼす影響について、申請者は以下のように説明している。
本臨床開発プログラムでは、当初は接種回数 1 回のみで開発する予定であったが、COV001 試験 3 群
における免疫原性の評価で 2 回目の接種後に免疫原性の増強が認められた(7.R.6.1 項参照)ため、各試
験開始後に、より大規模に 2 回接種の評価を実施することが決定された。また、治験薬の製造スケール
の拡大と並行して本臨床開発プログラムが急速に拡大された結果、4 試験すべてで 2 回目のワクチン接
種のための治験薬の供給が遅延し、主に英国の試験(COV001 試験及び COV002 試験)が影響を受けた。
これらに起因する遅延のため、初回と 2 回目の実際の接種間隔は 4~26 週間の範囲であったが、接種レ
ジメン間に真の差はないと推測し、接種間隔の異なる集団を一つの集団として解析対象とした。
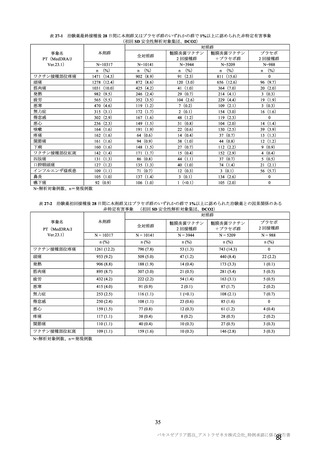
主要解析(DCO2)時点の血清反応陰性有効性解析対象集団における有効性(VE)に関する接種間隔
別の結果は、表 34 のとおりである。4 週以上の接種間隔では、SDSD+LDSD 血清反応陰性有効性解析
対象集団及び SDSD 血清反応解析対象集団のいずれにおいても、接種間隔が長いほど VE が高くなる傾
向が認められた。
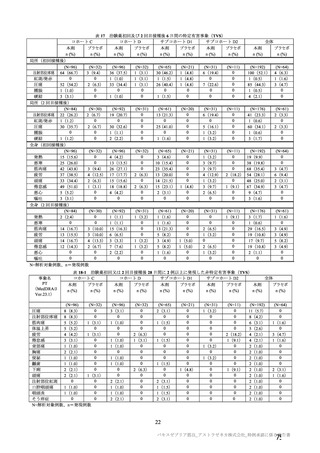
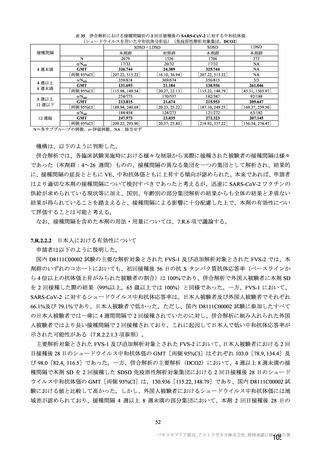
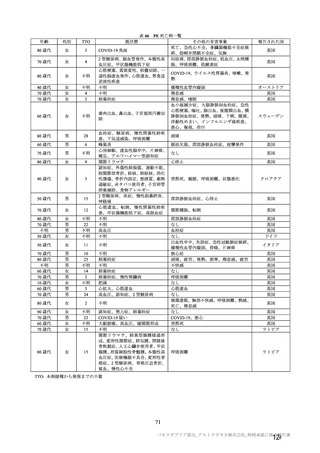
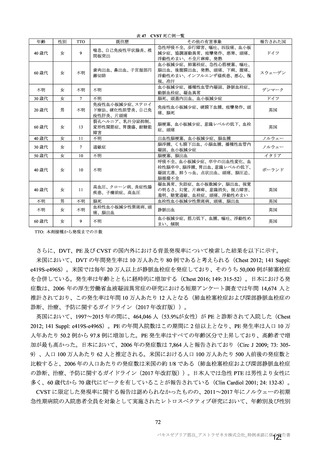
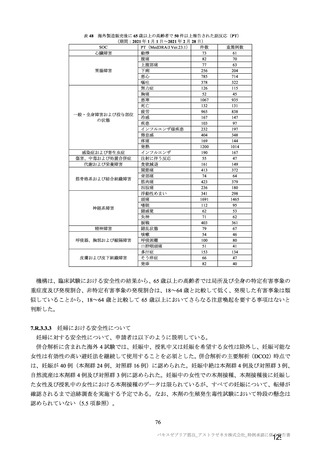
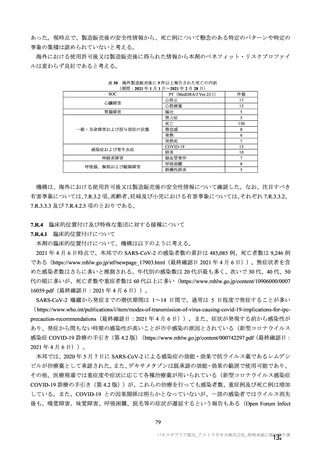
表 34 併合解析における接種間隔別の 2 回目接種後 15 日以降に発現し、
SARS-CoV-2 感染がウイルス学的に確定された初発の COVID-19 の発現に対する VE(DCO2)
COVID-19 発現数
接種間隔
VE(%)
両側 95 % CI(%)a)
本剤群
対照群
n / N(%)
n / N(%)
SDSD+LDSD 血清反応陰性有効性解析対象集団
66.56
4 週未満
1/206(0.49)
3/203(1.48)
[-221.83, 96.53]
50.48
4 週以上 8 週未満
47/4312(1.09)
90/4200(2.14)
[29.56, 65.19]
74.97
8 週以上 12 週以下
23/2308(1.00)
92/2348(3.92)
[60.48, 84.14]
78.91
12 週超
13/1771(0.73)
63/1830(3.44)
[61.68, 88.39]
SDSD 血清反応陰性有効性解析対象集団
66.56
4 週未満
1/206(0.49)
3/203(1.48)
[-221.83, 96.53]
50.48
4 週以上 8 週未満
47/4294(1.09)
90/4183(2.15)
[29.55, 65.19]
72.64
8 週以上 12 週以下
18/1555(1.16)
66/1580(4.18)
[53.95, 83.75]
77.62
12 週超
8/1146(0.7)
38/1213(3.13)
[51.98, 89.57]
LDSD 血清反応陰性有効性解析対象集団
0/0
0/0
NA
NA
4 週未満
0/18
0/17
NC
NC
4 週以上 8 週未満
80.80
8 週以上 12 週以下
5/753(0.66)
26/768(3.39)
[50.05, 92.62]
80.78
12 週超
5/625(0.80)
25/617(4.05)
[49.86, 92.63]
N=解析対象例数、n=発現例数、NA:該当せず、NC:算出せず
a) 接種群を因子とし、追跡期間の対数をオフセット変数としたポアソン回帰モデル
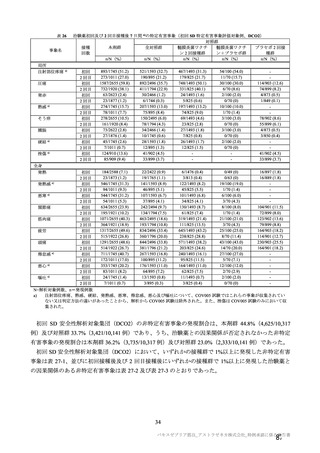
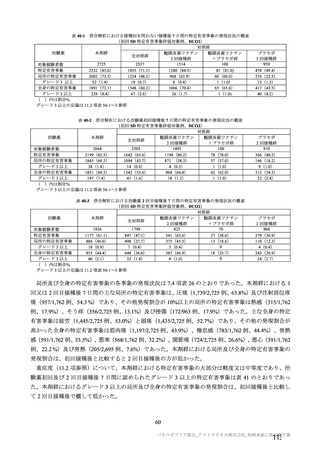
接種間隔別の免疫原性(中和抗体価)の結果は表 35 のとおりであり、VE と同様に、4 週以上の接種
間隔では、接種間隔が長いほど 2 回目接種後の中和抗体価が高くなる傾向が認められた。
51
バキスゼブリア筋注_アストラゼネカ株式会社_特例承認に係る報告書
104