参考資料1-7 浜口班の議論における参考資料(令和3年10月25日開催)(令和3年度第6回安全技術調査会参考資料1-2) (141 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27504.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会安全技術調査会(令和4年度第2回 8/23)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
や COV005 試験等については、接種間隔を「4 週」と設定した。
一方で、より早期に開始となっていた試験群においては、2 回目接種導入決定の遅れ、及び物流面の
制約による製剤供給の遅れにより、4 週間隔で 2 回目接種を行うことが不可能なことも多く、製剤の供
給状況や流通上の問題により実施可能性に基づき設定した。
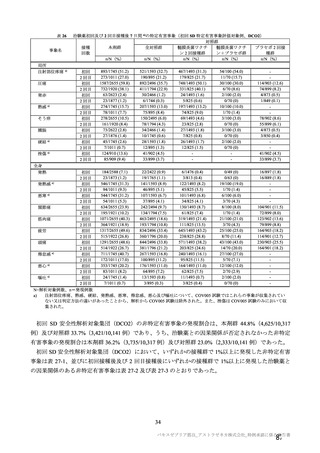
表 53
試験
COV001
COV002
COV003
COV005
国内
D8111C00002
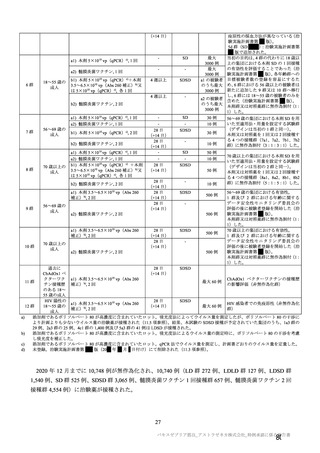
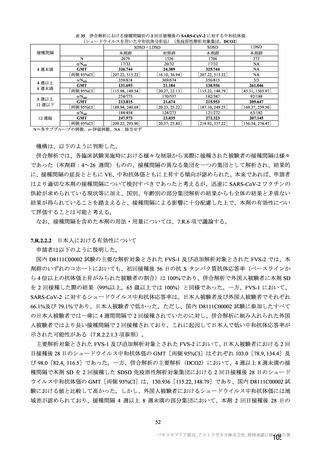
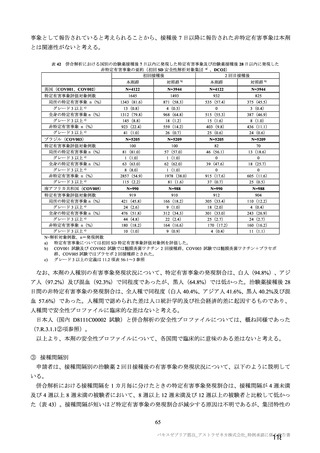
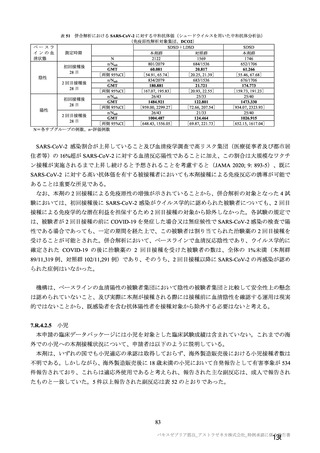
併合解析の対象とされた試験(COV001 試験、COV002 試験、COV003 試験及び COV005 試験)
及び国内 D8111C00002 試験における接種群ごとの初回接種後の接種間隔の規定等
治験実施計画書に規定され
接種群(SDSD+LDSD 有
目標被験者数
併合解析の解析対象者数
た接種間隔(許容範囲)
効性解析対象集団のみ、
(合計)
(SDSD+LDSD 有効性解
対照群含む)
析対象集団)
2c, 2e
8 週(7~10 週)
最大 30 例
17 例
2f, 2g, 4c, 4d
4 週以上
最大 930 例
724 例
4 週(4~6 週)
4 週以上
4~12 週(4~14 週)
4 週(3~5 週)
9-a1, a2, 10-a1, a2
4-c1, c2, 6-b1, b2
1c, 1d
1, 2a, 2b
2000 例
最大 9450 例
最大 10300 例
1970 例
1592 例
6615 例
6753 例
1477 例
4 週(±2 日)
すべて
256 例
-
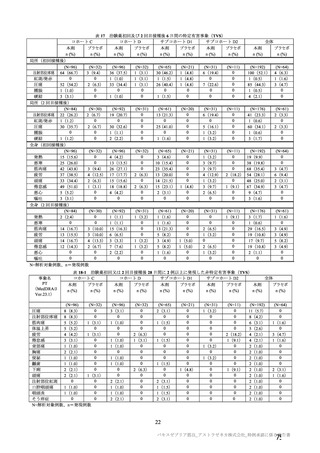
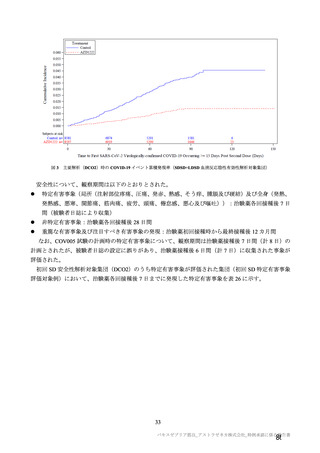
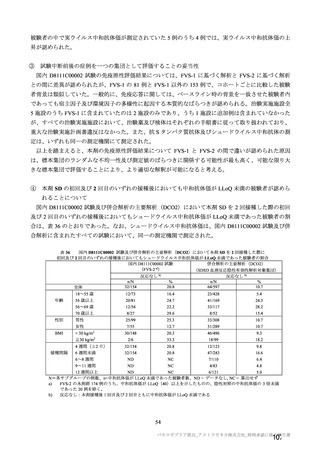
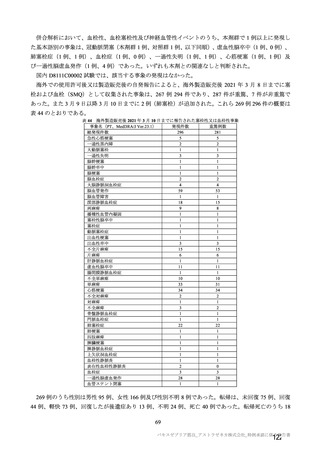
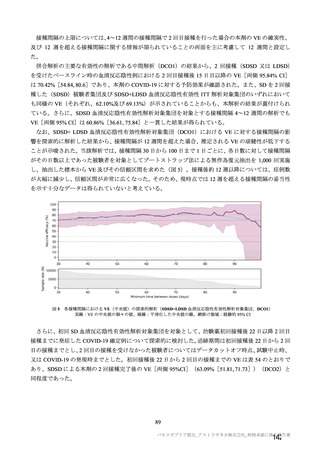
また、併合解析の有効性解析対象とされた SDSD+ LDSD 血清反応陰性有効性解析対象集団において、
実際の試験における接種間隔は図 4 のとおりであった。
図4
主要解析(DCO2)時点での併合解析対象集団(COV001 試験、COV002 試験、COV003 試験及び COV005 試験)における
接種間隔ごとの接種例数(SDSD+ LDSD 血清反応陰性有効性解析対象集団)
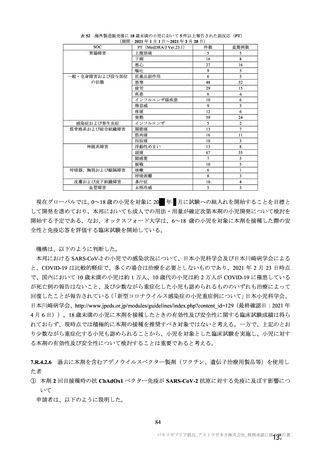
機構は、予定用法・用量において接種間隔の上限を 12 週とした理由を説明するよう求め、申請者は以
下のように説明した。
88
バキスゼブリア筋注_アストラゼネカ株式会社_特例承認に係る報告書
141