参考資料1-7 浜口班の議論における参考資料(令和3年10月25日開催)(令和3年度第6回安全技術調査会参考資料1-2) (108 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27504.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会安全技術調査会(令和4年度第2回 8/23)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
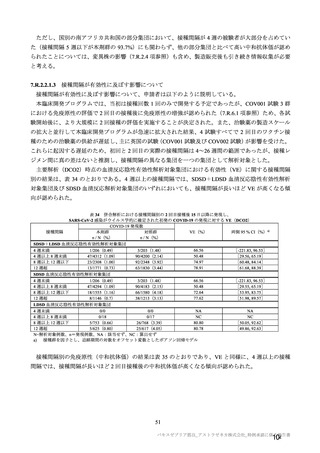
であった被験者の割合は、非高齢者(18~55 歳)と比較して高齢者(56 歳以上)で高かった。併合解析
では、接種間隔の延長に伴ってシュードウイルス中和抗体価が LLoQ 未満であった被験者の割合が低下
する傾向が認められたが、併合解析の高齢者は概して接種間隔が短かったことから、年齢区分と接種間
隔の間に交絡が示唆され(7.R.2.2.1.3 項参照)、国内外で傾向に違いはないと考えられた。
以上の結果から、国内 D8111C00002 試験の各コホートにおいて観測された本剤の免疫原性は、併合解
析で認められた免疫原性と類似しており、日本人においても同様の有効性が期待できると考えられる。
機構は、以下のように判断した。
中和抗体価の測定値にはばらつきが認められることも踏まえると、限られた日本人被験者数のデータ
からは成績の解釈が困難な点もあるが、国内 D8111C00002 試験で本剤 2 回目接種後に認められた中和抗
体価は、併合解析における英国及びブラジルの接種間隔 4~8 週の部分集団で得られた 2 回目接種後の
結果と大きく異ならず、また、日本人高齢者についても高齢者以外の集団と同様の中和抗体価の上昇が
認められた。また、抗 S タンパク質抗体の応答等からも日本人において外国人と同様の免疫原性が示さ
れていることも踏まえると、日本人について本剤接種後の免疫応答が外国人と大きく異なる傾向は示さ
れていないものと考える。
以上のこと、及び併合解析において実施国や人種の違いが VE 及び免疫原性の成績に大きな影響を及
ぼす可能性は一部の SARS-CoV-2 変異株(B.1.351 系統)による影響を除いて(7.R.2.4 項参照)示唆され
ていないことを踏まえると、年齢を問わず 18 歳以上の日本人において本剤の有効性は期待できると考
える。
7.R.2.2.3
高齢者における有効性について
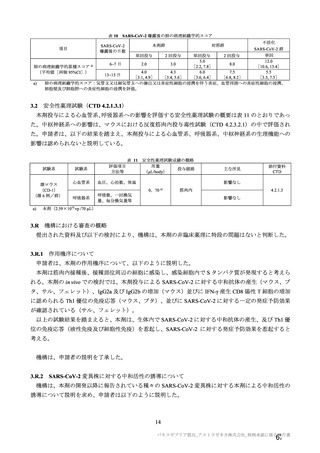
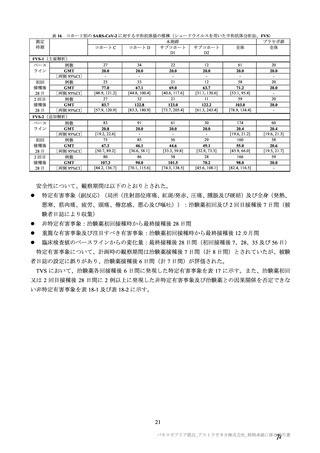
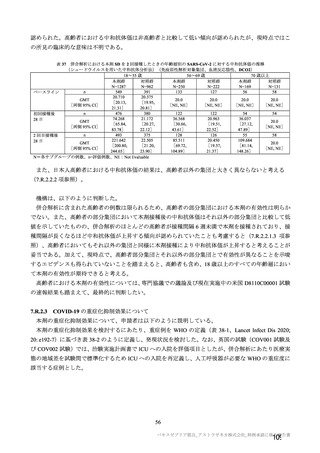
併合解析における年齢による部分集団解析の結果は、7.R.2.2.1.1 項表 30 のとおりである。高齢者にお
ける有効性について、申請者は以下のように説明している。
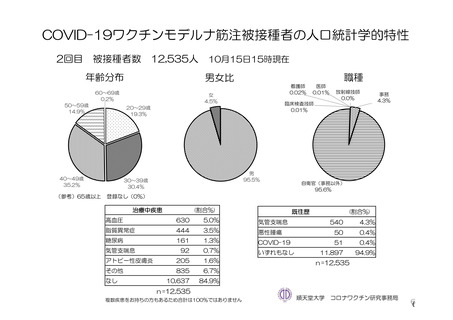
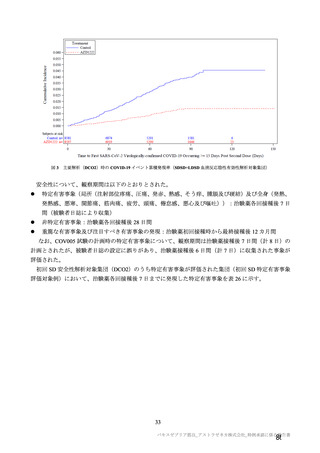
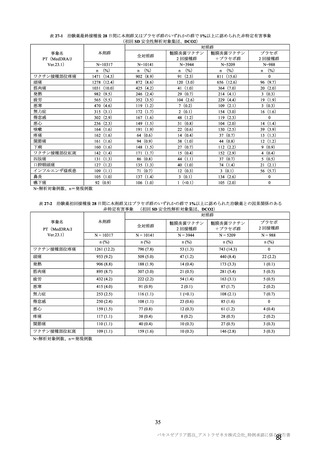
主要解析(DCO2)時点において、併合解析の有効性の主要解析対象集団(SDSD+LDSD 血清反応陰
性有効性解析対象集団)における 65 歳以上の成人は全体の 8.2%と少なかった(本剤群 703 例及び対照
群 680 例)。すべての 65 歳以上の被験者は SDSD の用量を接種され、大部分(本剤群の 89.6%、対照群
の 87.8%)の被験者の接種間隔は 6 週未満であった。また、初回接種後の追跡期間(平均値±標準偏差)
は 82.9±21.5 日、2 回目接種後 15 日以降の追跡期間(平均値±標準偏差)は 34.9±20.9 日であった。
SDSD+LDSD 血清反応陰性有効性解析対象集団の 65 歳以上の成人において、2 回目接種後 15 日以降
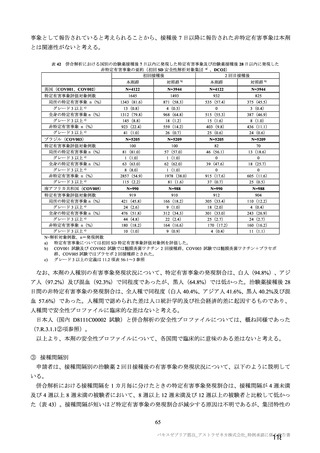
に発現した COVID-19 症例は、本剤群 4/703 例(0.57%)、対照群 8/680 例(1.18%)であった。また、初
回 SD 血清反応陰性有効性解析対象集団の 65 歳以上の成人において、初回 SD 接種後 22 日以降に発現
した COVID-19 症例は本剤群 6/945 例(0.63%)、対照群 13/896 例(1.45%)であり、うち、COVID-19
に関連した入院は本剤群 0 例、対照群 2 例で、重症 COVID-19 は本剤群及び対照群ともに認められな
かった。
以上のように、65 歳以上の高齢者では、VE を評価するためのイベント数が少なかったが、全体集団
の結果と一貫した結果が認められた。
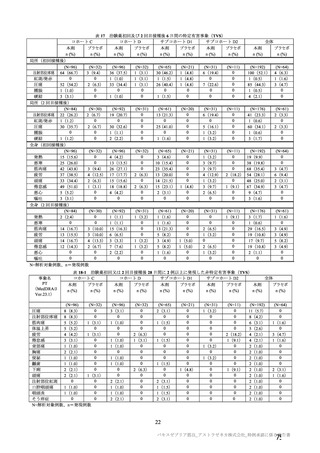
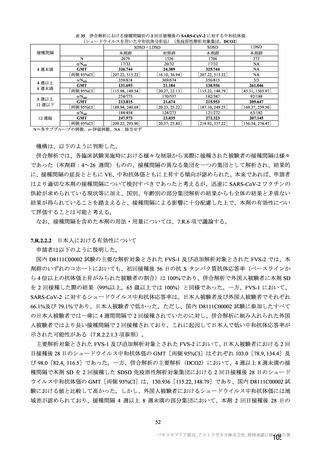
また、併合解析における年齢別の中和抗体価の推移は表 37 のとおりであり、交絡因子として接種間隔
の違いを考慮すれば(7.R.2.2.1.3 項参照)、すべての年齢区分において本剤接種による中和抗体の誘導が
55
バキスゼブリア筋注_アストラゼネカ株式会社_特例承認に係る報告書
108