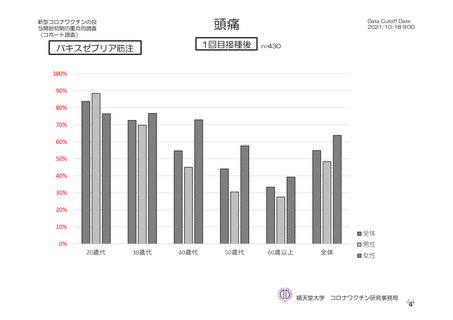
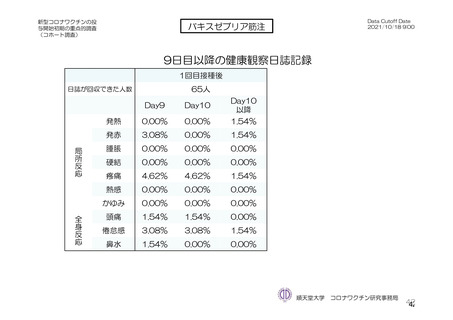
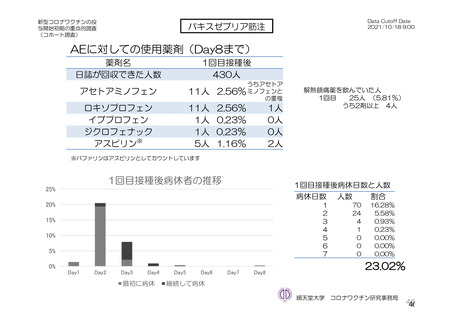
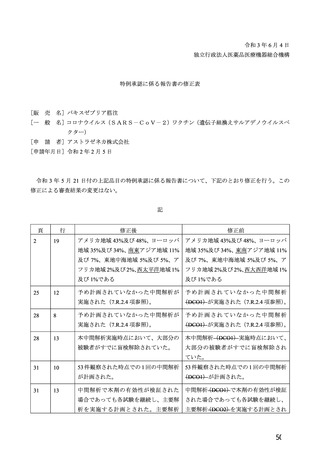
参考資料1-7 浜口班の議論における参考資料(令和3年10月25日開催)(令和3年度第6回安全技術調査会参考資料1-2) (109 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27504.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会安全技術調査会(令和4年度第2回 8/23)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
の所見の臨床的な意味は不明である。
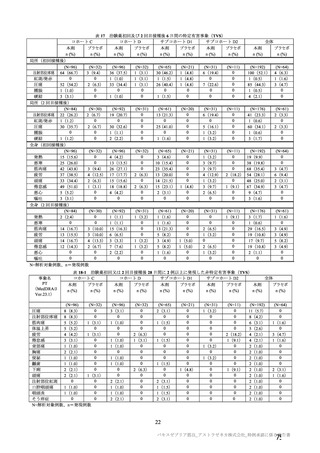
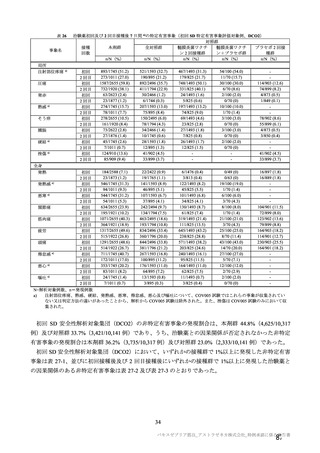
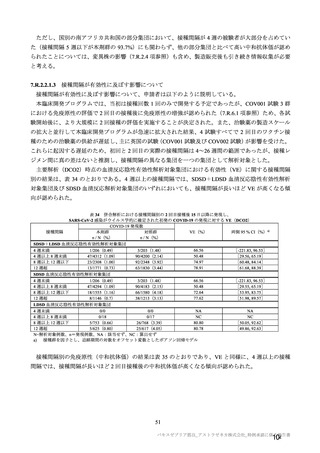
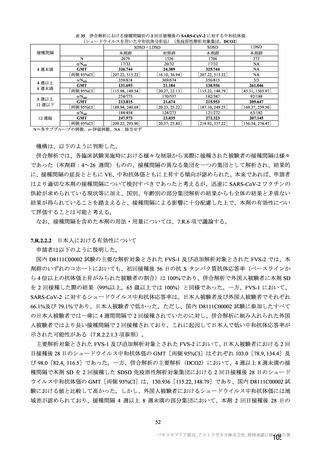
表 37 併合解析における本剤 SD を 2 回接種したときの年齢層別の SARS-CoV-2 に対する中和抗体価の推移
(シュードウイルスを用いた中和抗体分析法)(免疫原性解析対象集団、血清反応陰性、DCO2)
18~55 歳
56~69 歳
70 歳以上
本剤群
対照群
本剤群
対照群
本剤群
対照群
N=1287
N=962
N=250
N=222
N=169
N=131
n
549
391
133
127
56
58
ベースライン
20.710
20.375
GMT
20.0
20.0
20.0
20.0
[20.13,
[19.95,
[両側 95% CI]
[NE, NE]
[NE, NE]
[NE, NE]
[NE, NE]
21.31]
20.81]
n
476
380
122
122
54
54
初回接種後
74.268
21.172
36.568
20.963
36.037
28 日
GMT
20.0
[65.84,
[20.27,
[30.66,
[19.51,
[27.12,
[両側 95% CI]
[NE, NE]
83.78]
22.12]
43.61]
22.52]
47.89]
n
493
375
128
126
55
58
2 回目接種後
221.642
22.505
85.511
20.450
109.684
28 日
GMT
20.0
[200.80,
[21.20,
[69.72,
[19.57,
[81.14,
[両側 95% CI]
[NE, NE]
244.65]
23.90]
104.89]
21.37]
148.26]
N=各サブグループの例数、n=評価例数、NE:Not Evaluable
また、日本人高齢者における中和抗体価の結果は、高齢者以外の集団と大きく異ならないと考える
(7.R.2.2.2 項参照)。
機構は、以下のように判断した。
併合解析に含まれた高齢者の例数は限られるため、高齢者の部分集団における本剤の有効性は明らか
でない。また、高齢者の部分集団において本剤接種後の中和抗体価はそれ以外の部分集団と比較して低
値を示していたものの、併合解析のほとんどの高齢者が接種間隔 6 週未満で本剤を接種されており、接
種間隔が長くなるほど中和抗体価が上昇する傾向が認められていたことも考慮すると(7.R.2.2.1.3 項参
照)、高齢者においてもそれ以外の集団と同様に本剤接種により中和抗体価が上昇すると考えることが
妥当である。加えて、現時点で、高齢者部分集団とそれ以外の部分集団とで有効性が異なることを示唆
するエビデンスも得られていないことを踏まえると、高齢者も含め、18 歳以上のすべての年齢層におい
て本剤の有効性が期待できると考える。
高齢者における本剤の有効性については、専門協議での議論及び現在実施中の米国 D8110C00001 試験
の速報結果も踏まえて、最終的に判断したい。
7.R.2.3
COVID-19 の重症化抑制効果について
本剤の重症化抑制効果について、申請者は以下のように説明している。
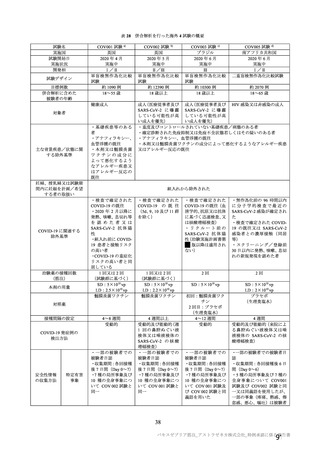
本剤の重症化抑制効果を検討するにあたり、重症例を WHO の定義(表 38-1、Lancet Infect Dis 2020;
20: e192-7)に基づき表 38-2 のように定義し、発現状況を検討した。なお、英国の試験(COV001 試験及
び COV002 試験)では、治験実施計画書で ICU への入院を評価項目としたが、併合解析にあたり医療実
態の地域差を試験間で標準化するため ICU への入院を再定義し、人工呼吸器が必要な WHO の重症度に
該当する症例とした。
56
バキスゼブリア筋注_アストラゼネカ株式会社_特例承認に係る報告書
109