資 料4-2-➀ 令和4年度第2回安全技術調査会の審議結果について➀ (124 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27906.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第2回 9/14)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
令 和 3 年 5 月 20 日
医薬・生活衛生局医薬品審査管理課
[販
[一
売
般
名]
名]
[申 請 者 名]
[申請年月日]
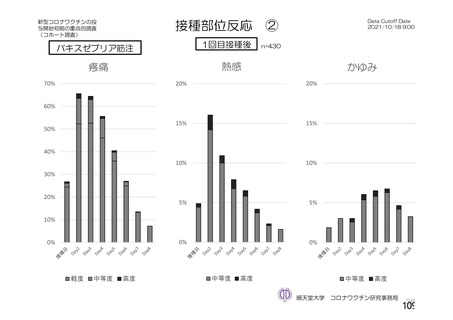
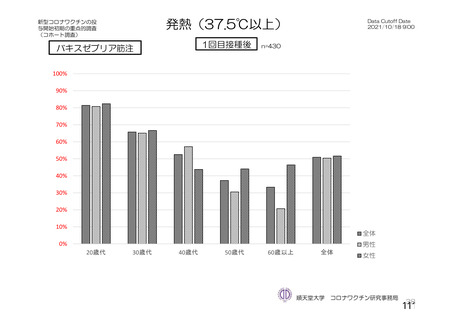
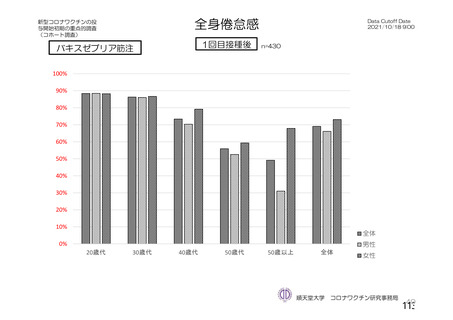
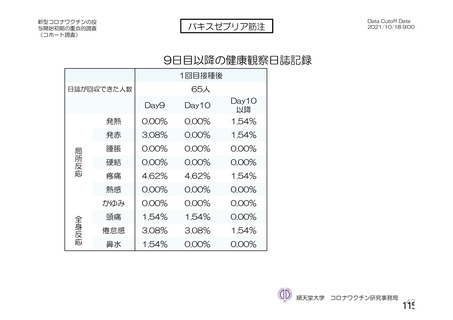
バキスゼブリア筋注
コロナウイルス(SARS-CoV-2)ワクチン(遺伝子組換えサ
ルアデノウイルスベクター)
アストラゼネカ株式会社
令和3年2月5日
[審 議 結 果]
本品目は、新型コロナウイルス(SARS-CoV-2)による感染症が世界的に流行
している昨今の状況において、医薬品、医療機器等の品質、有効性及び安全性
の確保等に関する法律(昭和 35 年法律第 145 号。以下「医薬品医療機器等法」
という。)第 14 条の3第1項に基づく承認に該当することが見込まれるとし
て、承認申請があったものである。
本品目については、令和3年5月 20 日に開催された医薬品第二部会におい
て、医薬品医療機器等法第 14 条の3第1項の規定による特例承認の可否につ
いて審議された。その結果、下記の承認条件が付されることを前提として、承
認して差し支えないものとされ、薬事・食品衛生審議会薬事分科会に報告する
こととされた。
本品目は生物由来製品に該当し、再審査期間は8年、原体及び製剤はいずれ
も劇薬に該当するとされた。
[承 認 条 件]
1. 医薬品リスク管理計画を策定の上、適切に実施すること。
2. 現時点での知見が限られていることから、製造販売後、副反応情報等の本
剤の安全性に関するデータを、あらかじめ定めた計画に基づき早期に収集
するとともに、独立行政法人医薬品医療機器総合機構に提出し、本剤の適
正使用に必要な措置を講じること。その際、国が実施する健康調査等によ
り得られた情報についても適切に反映すること。
3. 現在国内外で実施中又は計画中の臨床試験の成績が得られた際には、速や
かに当該成績を独立行政法人医薬品医療機器総合機構に提出するととも
に、本剤の有効性及び安全性に係る最新の情報を、医療従事者及び被接種
者が容易に入手可能となるよう必要な措置を講じること。また、国が行う
121