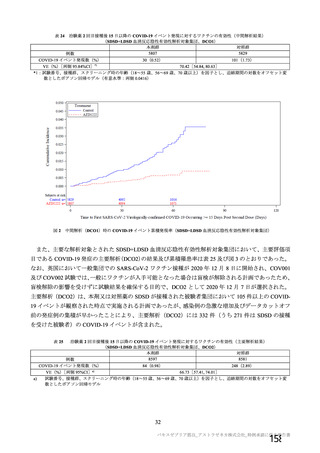
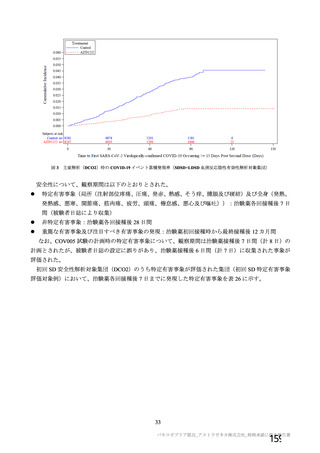
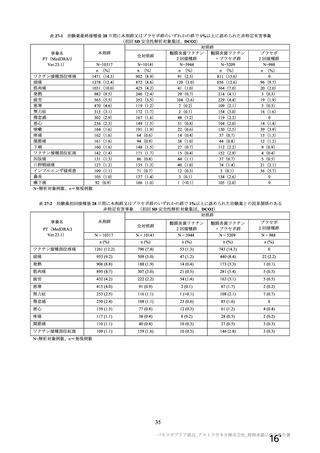
資 料4-2-➀ 令和4年度第2回安全技術調査会の審議結果について➀ (46 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27906.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第2回 9/14)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
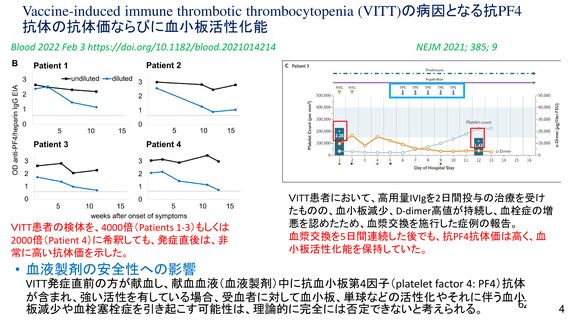
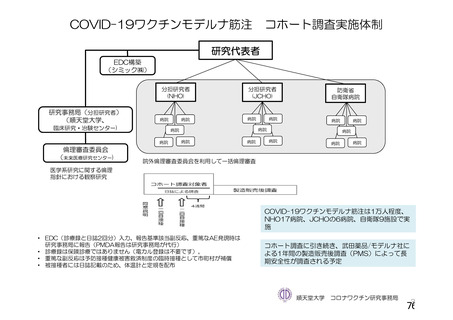
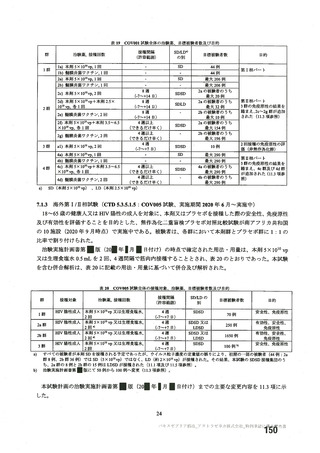
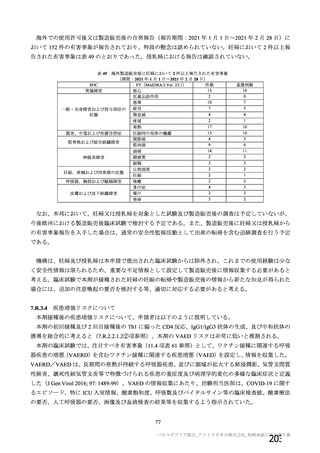
「安全な血液製剤の安定供給の確保等に関する法律第25条に基づく健康診断並びに生物由来原料基準第2の
1(1)及び2(1)に規定する問診等について」(令和4年3月30日現在)
(2)血液製剤の安全性の向上の観点から実施する問診
ワクチン等の接種状況を確認し、以下の全てを満たすことを確認すること。
ワクチン等の種類
例
採血制限の期間
不活化ワクチン
インフルエンザ、日本脳炎、コレラ、肺炎球菌、百日咳、A型肝
接種後24時間を経過していること
炎、狂犬病等
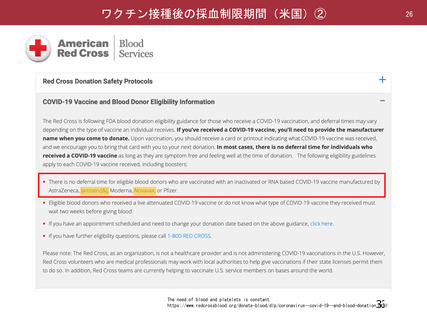
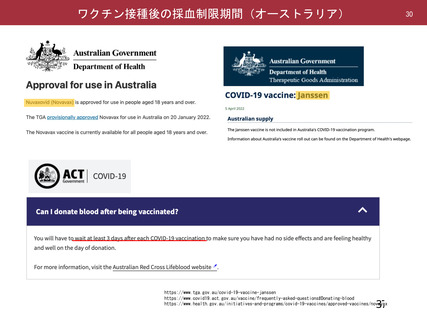
RNAワクチン
新型コロナウイルス等
接種後48時間を経過していること
B型肝炎ワクチン
ー
接種後2週間を経過していること
弱毒生ワクチン
黄熱、麻疹、ポリオ、おたふくかぜ、風疹、水痘、BCG等
接種後4週間を経過していること
ウイルスベクターワクチン
新型コロナウイルス等
接種後6週間を経過していること
抗血清
破傷風、蛇毒、ジフテリア等
接種後3月を経過していること
咬傷後の狂犬病ワクチン ー
接種後1年を経過していること
43
3