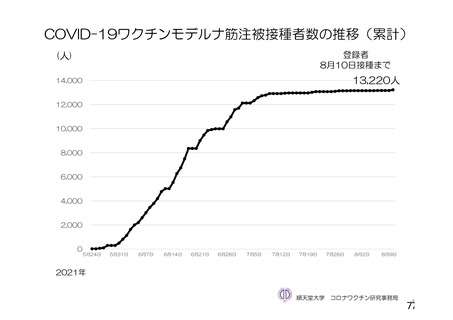
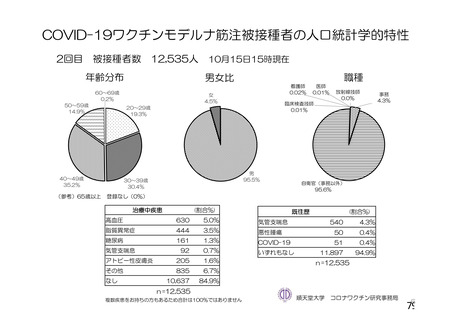
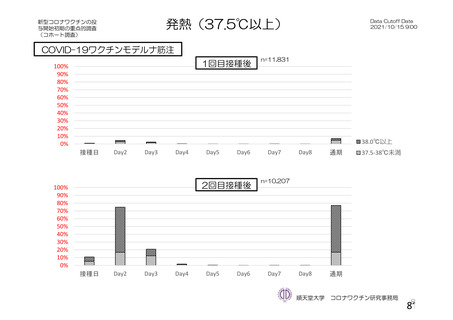
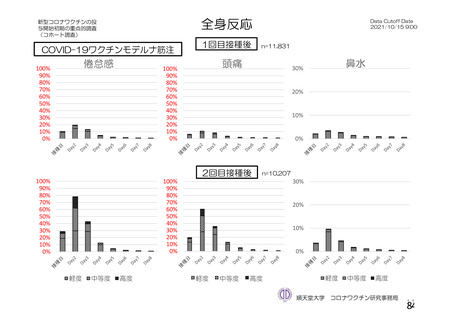
資 料4-2-➀ 令和4年度第2回安全技術調査会の審議結果について➀ (29 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27906.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第2回 9/14)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
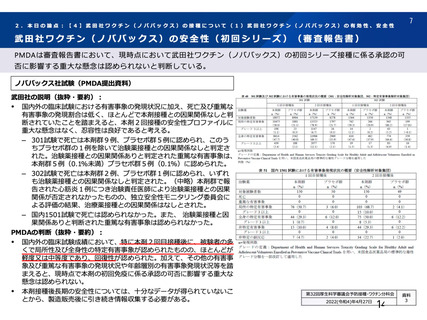
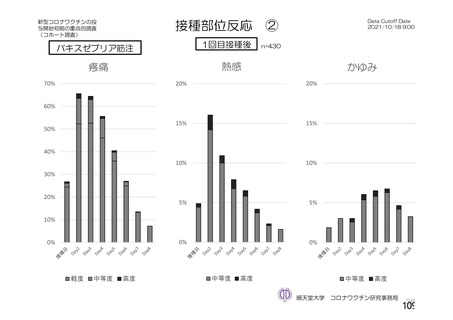
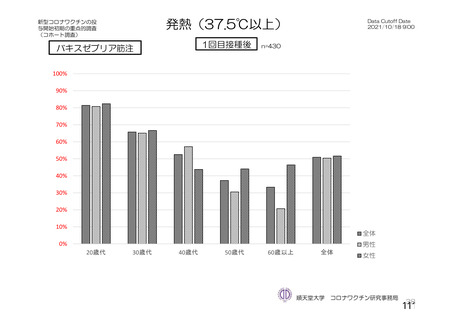
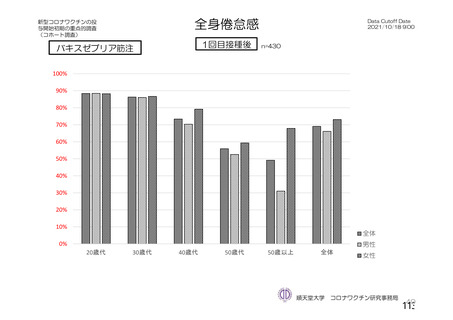
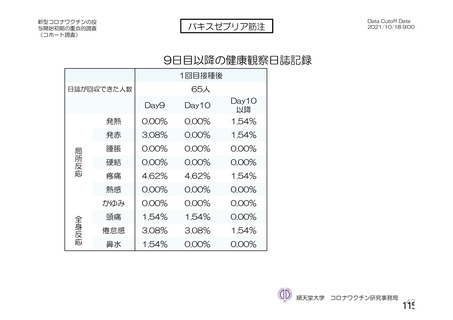
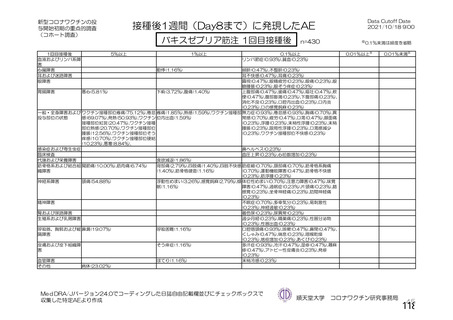
【注目すべき有害事象についてヤンセンファーマ社の説明(要約・抜粋)】
①アナフィラキシーを含む重度のアレルギー反応
本剤接種との因果関係が明確と考えられる症例が認められるため、本剤の成分に対して重度の過敏症の既往歴が
ある者は接種不適者に該当すること等、添付文書等に置いて注意喚起を行う。
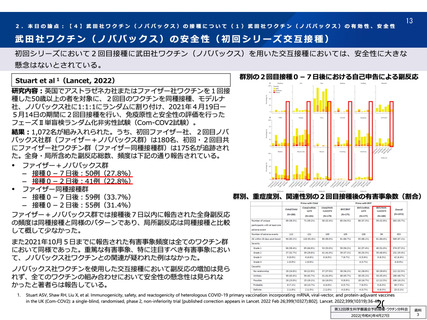
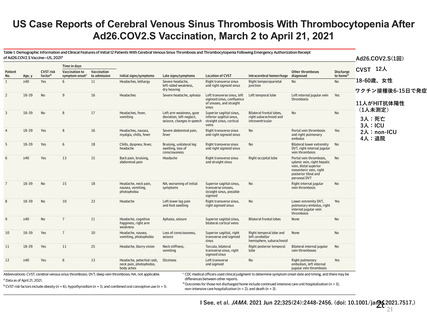
②血栓性及び血栓塞栓性事象
本剤接種と血小板減少症を伴う血栓症の発症との因果関係は否定できないと考え、本剤の重要な特定されたリス
クであると考える。したがって、本剤接種後に、脳静脈洞血栓症、内臓静脈血栓症(門脈血栓症等)、動脈血栓
症との血栓症が稀に認められ、血小板減少症を伴い、致死的転帰に至る可能性があること、これらの症例の多く
は本剤接種の3週間以内に発現していること等について注意喚起する必要がある。
③免疫介在性及び神経炎症性の事象
・ギラン・バレー症候群(GBS)
重大な副反応として添付文書で注意喚起する予定
・脳炎(急性散在性脳脊髄炎(ADEM)及び髄膜脳炎を含む)
多くの事象が報告され、本剤接種後における発現率と背景発現率との比較では不均衡が認められている。しか
しながら、認められた症例の多くは事象と本剤との関連性を確認するための情報が不十分であり、現時点では本
剤との関連性は明確でないと考える。炎症性の中枢神経系の症状は、依然として注目すべき有害事象であり、引
き続き発現状況を注視する。
・横断性脊髄炎
本剤接種後に認められた症例の多くは本剤との関連性は明確ではないと考えれることから、引き続き発現状況
を注視する。
PMDA審議結果報告書
R4.6.1
26
19