資 料4-2-➀ 令和4年度第2回安全技術調査会の審議結果について➀ (52 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27906.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第2回 9/14)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
1 趣旨
献血者等の安全対策及び血液製剤の安全性の向上の観点から、血液法第 25 条及
び規則第 14 条に基づく健康診断並びに基準第2の1(1)及び2(1)に規定す
る問診等の方法について、
「安全な血液製剤の安定供給の確保等に関する法律第 25
条に基づく健康診断並びに生物由来原料基準第2の1(1)及び2(1)に規定す
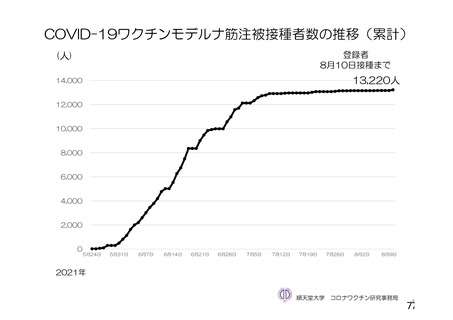
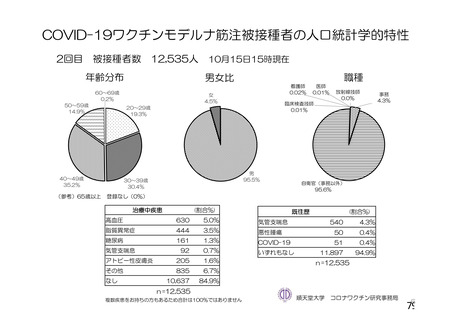
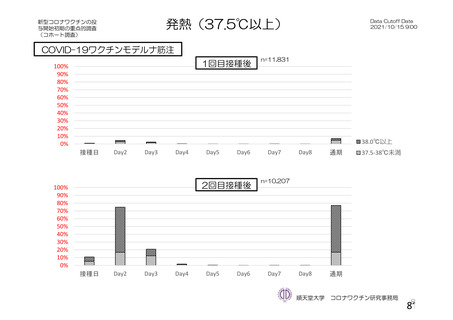
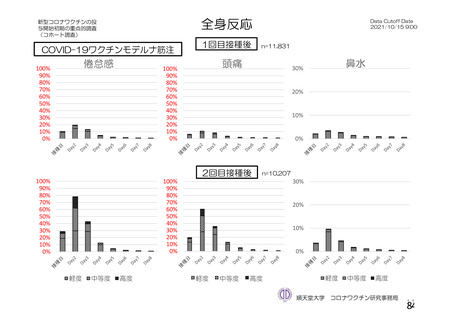
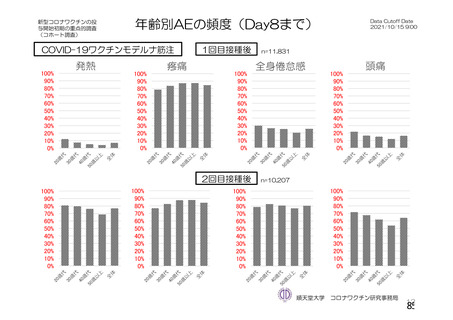
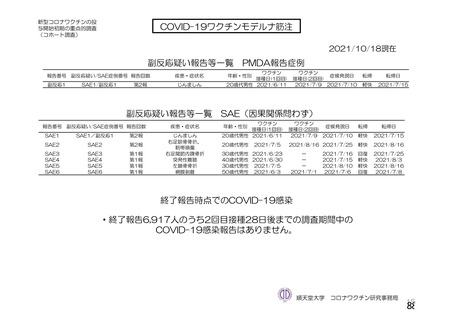
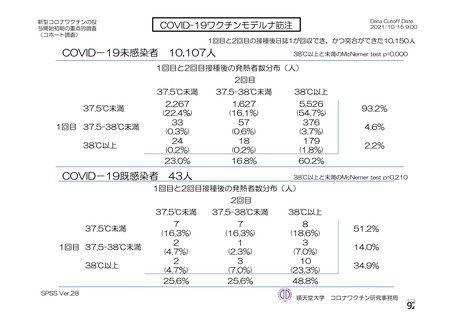
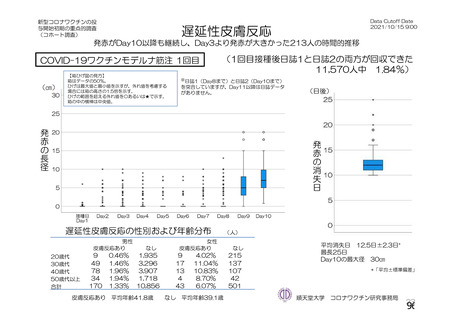
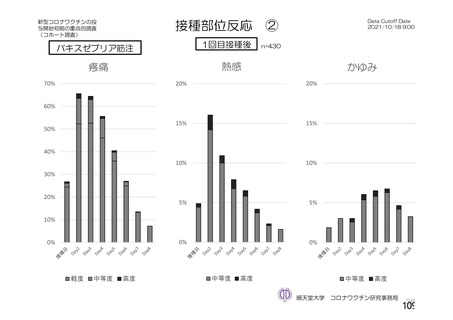
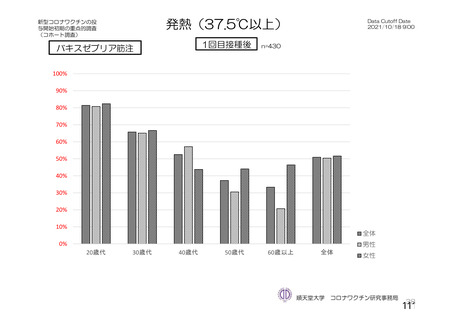
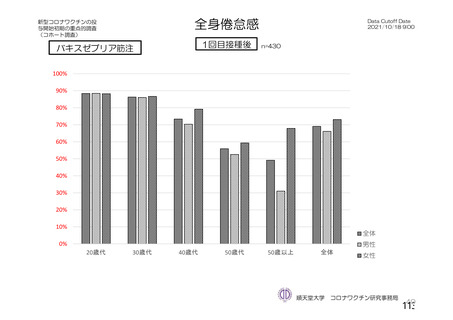
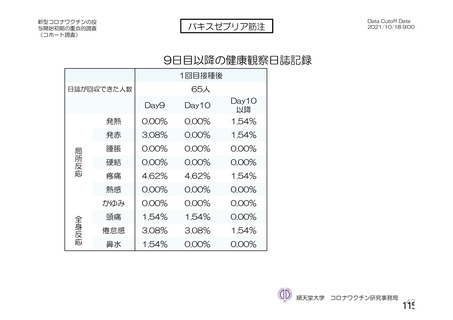
る問診等について」において示してきた。今般、新型コロナウイルス(SARS-CoV-2)
に関し、新たな種類のワクチンが承認されたこと、予防接種が開始されたこと、ワ
クチンの投与開始初期の重点的調査(コホート調査)に関する中間報告がなされた
こと等から、当該問診等について所要の改正を行うものである。
なお、今後、ワクチンの性状やワクチン接種後の長期的な状況等について新たな
知見を踏まえ、変更する可能性があることに留意いただきたい。
2
主な改正内容
「第1 健康診断及び問診等の方法について 1 問診(2)血液製剤の安全性
の向上の観点から実施する問診 エ ワクチン等の接種状況」において、六を七と
し、五を三とし、四を六とし、三を四とし、四の次に「五 ウイルスベクターワク
チン(新型コロナウイルス等)接種後6週間を経過していること」を追記する。
3 適用期日
本通知は、令和4年4月1日から適用する。
49