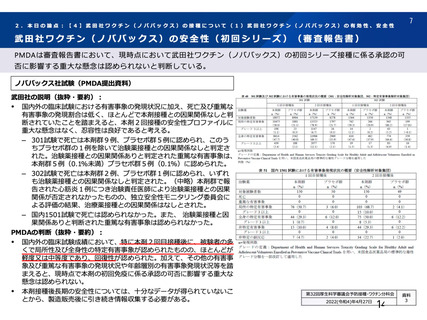
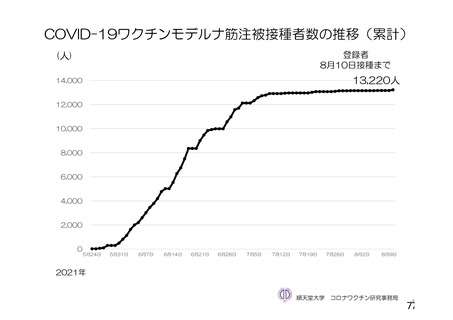
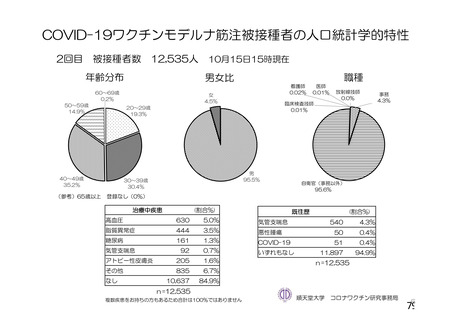
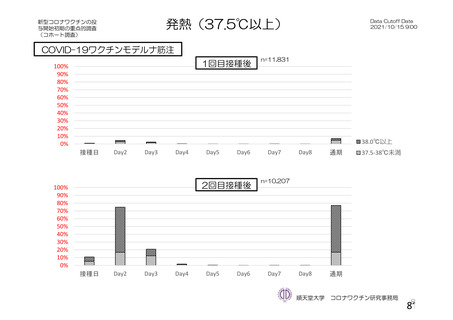
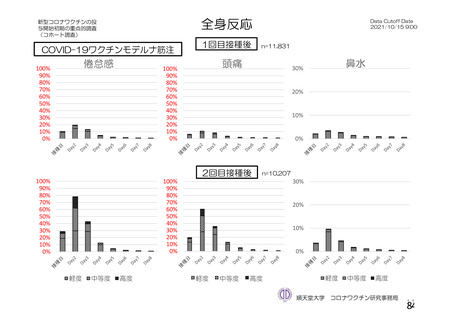
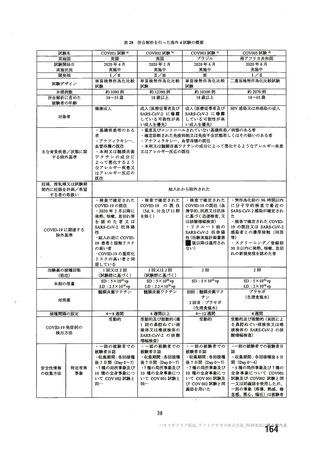
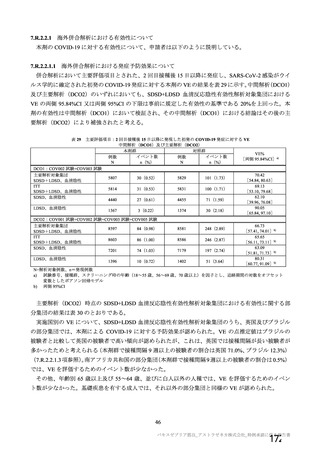
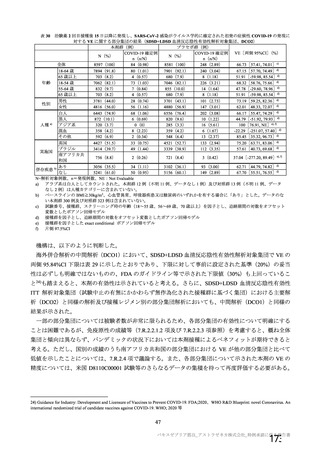
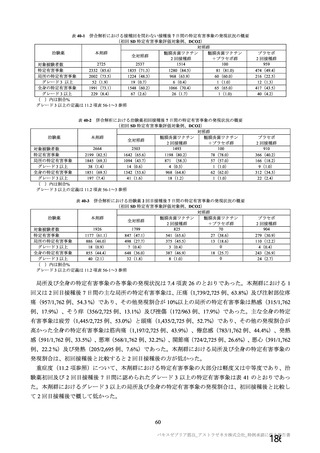
資 料4-2-➀ 令和4年度第2回安全技術調査会の審議結果について➀ (20 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27906.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第2回 9/14)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
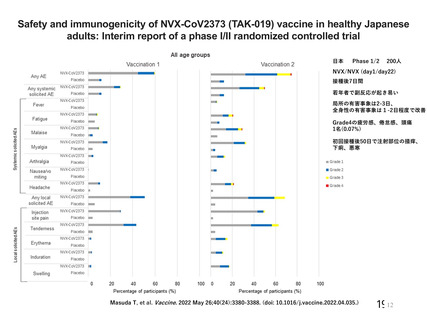
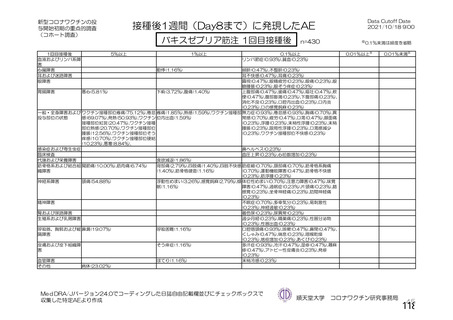
United States and Mexico Phase 3
約30,000⼈
NVX/NVX (day0/day21)
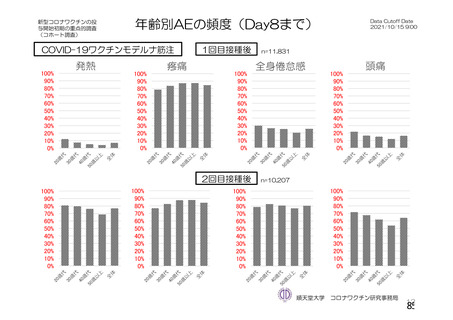
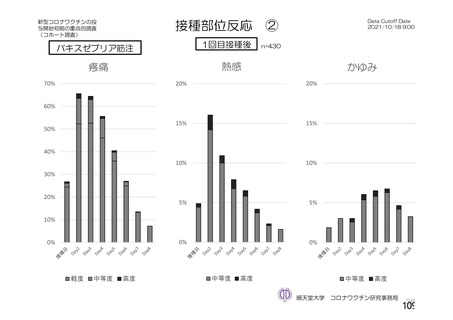
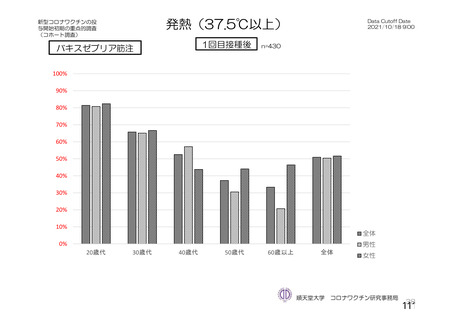
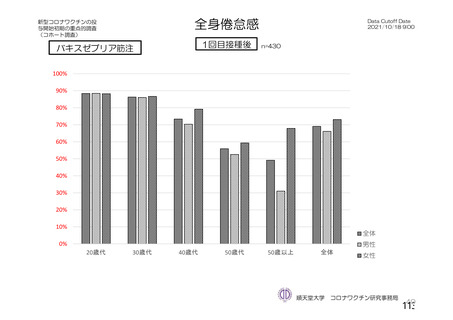
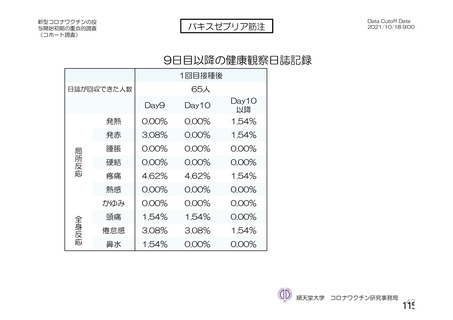
接種後7⽇間
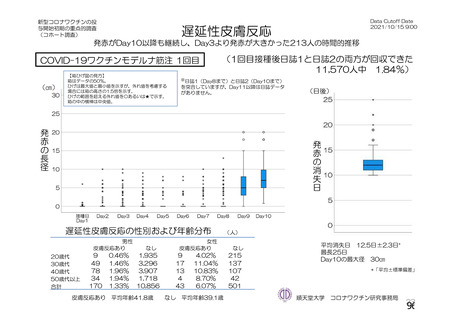
局所の有害事象は2⽇、全⾝性の有害事象は1⽇程度で改善
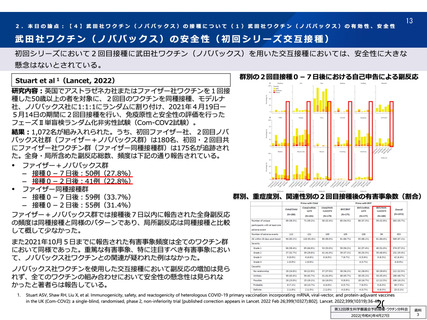
アナフィラキシー
ギランバレー症候群
なし
⼼筋炎や⼼膜炎
⾎⼩板減少を伴うワクチン誘導免疫性⾎栓症
群間で不均衡なし
Dunkle LM, et al. N Engl J Med. 2022 Feb 10;386(6):531-543.
(DOI: 10.1056/NEJMoa2116185)
17 10