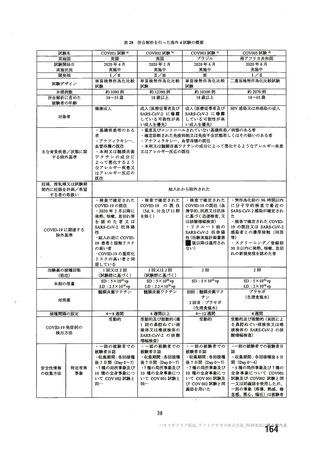
資 料4-2-➀ 令和4年度第2回安全技術調査会の審議結果について➀ (45 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27906.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第2回 9/14)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
時 期
内 容
2021/2/14
mRNAタイプの新型コロナワクチン(ファイザー社製)承認
2021/2/16
新型コロナワクチン接種(16歳以上の国民を対象)指示にかかる国の通知
2021/2月
医療関係者を対象に新型コロナワクチン接種開始
2021/4月
全国で高齢者を対象に新型コロナワクチン接種開始
2021/4/28
mRNAタイプの新型コロナワクチン接種後の献血延期期間通知(薬生発第0428号厚生労働省医薬・生活衛生局長通知)
←48時間延期
2021/5/14
mRNAワクチン接種者の献血受け入れ開始
2021/5/21
mRNAタイプの新型コロナワクチン(モデルナ社製)、ウイルスベクタータイプの新型コロナワクチン(アストラゼネカ社製)承認
2021/5月
自衛隊大規模接種会場でのワクチン接種開始
2021/6月
職域接種開始
2021/11月
3回目接種開始
2022/3/30
ウイルスベクタータイプの新型コロナワクチン接種後の献血延期期間通知(薬生発第0330号厚生労働省医薬・生活衛生局長通知)←6週間延期
2022/4/1
ウイルスベクターワクチン接種者の献血受け入れ開始
2022/4/19
組み換えタンパクタイプの新型コロナワクチン(武田社製)承認
2022/5/30
ウイルスベクタータイプの新型コロナワクチン(ヤンセンファーマ製)承認
42
2