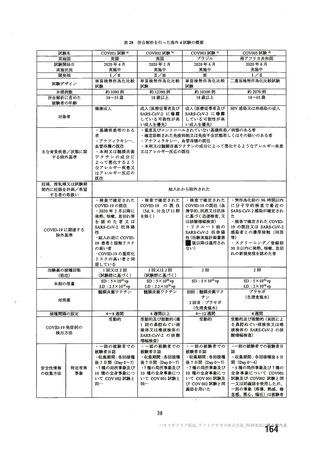
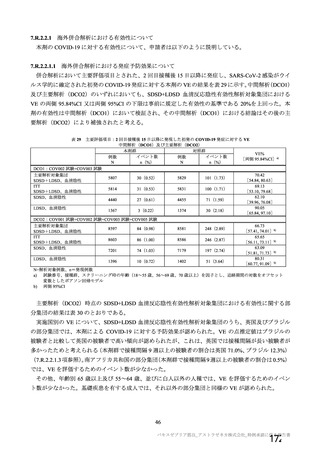
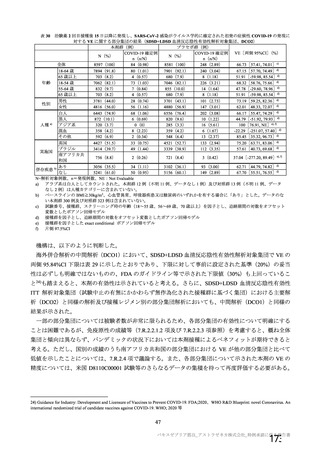
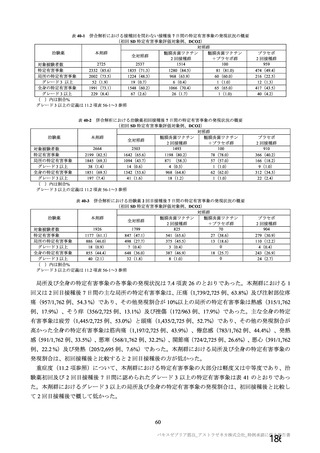
資 料4-2-➀ 令和4年度第2回安全技術調査会の審議結果について➀ (176 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27906.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第2回 9/14)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
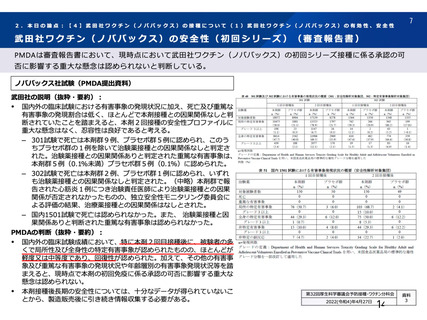
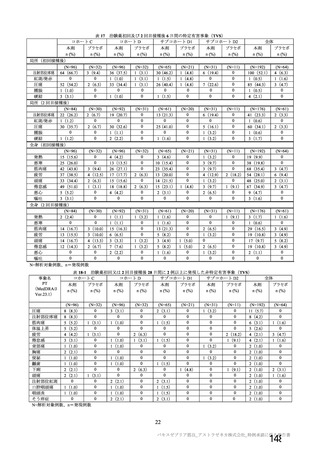
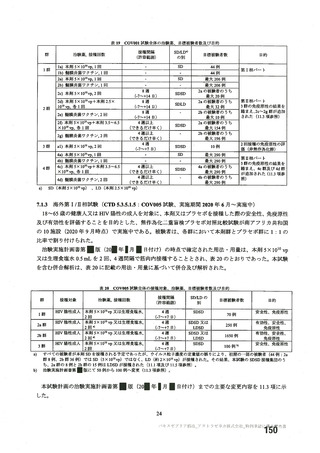
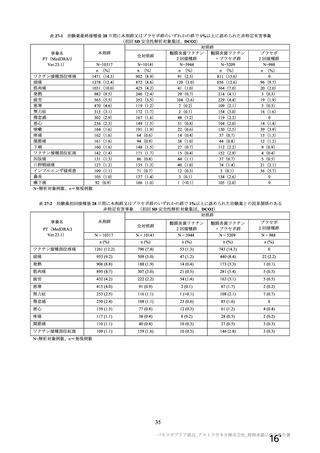
治験薬 2 回目接種後 15 日以降に発現し、SARS-CoV-2 感染がウイルス学的に確定された初発の症候性 COVID-19 の発現に
対する VE に関する部分集団の結果(SDSD+LDSD 血清反応陰性有効性解析対象集団、DCO2)
本剤群(例)
プラセボ群(例)
COVID-19 確定例
COVID-19 確定例 VE[両側 95%CI](%)
N(%)
N(%)
n(n/N)
n(n/N)
全体
8597(100)
84(0.98)
8581(100)
248(2.89)
66.73[57.41, 74.01]c)
18-64 歳
7894(91.8)
80(1.01)
7901(92.1)
240(3.04)
67.15[57.70, 74.49]d)
65 歳以上
703(8.2)
4(0.57)
680(7.9)
8(1.18)
51.91[-59.98, 85.54]d)
年齢
18-54 歳
7062(82.1)
73(1.03)
7046(82.1)
226(3.21)
68.32[58.76, 75.66]d)
55-64 歳
832(9.7)
7(0.84)
855(10.0)
14(1.64)
47.78[-29.60, 78.96]d)
65 歳以上
703(8.2)
4(0.57)
680(7.9)
8(1.18)
51.91[-59.98, 85.54]d)
男性
3781(44.0)
28(0.74)
3701(43.1)
101(2.73)
73.19[59.25, 82.36]d)
性別
女性
4816(56.0)
56(1.16)
4880(56.9)
147(3.01)
62.01[48.33, 72.07]d)
白人
6443(74.9)
68(1.06)
6556(76.4)
202(3.08)
66.17[55.47, 74.29]d)
黒人
872(10.1)
6(0.69)
820(9.6)
10(1.22)
44.79[-51.92, 79.93]d)
人種 a) アジア系
320(3.7)
0(0)
285(3.3)
16(5.61)
100[76.91, NE]e), f)
混血
358(4.2)
8(2.23)
359(4.2)
6(1.67)
-22.29[-251.07, 57.40]d)
その他
592(6.9)
2(0.34)
548(6.4)
13(2.37)
85.45[35.32, 96.73]d)
英国
4427(51.5)
33(0.75)
4521(52.7)
133(2.94)
75.20[63.71, 83.06]d)
ブラジル
3414(39.7)
49(1.44)
3339(38.9)
112(3.35)
57.61[40.73, 69.68]d)
実施国
南アフリカ共
756(8.8)
2(0.26)
721(8.4)
3(0.42)
37.04[-277.20, 89.49]e), f)
和国
あり
3056(35.5)
34(1.11)
3102(36.1)
93(3.00)
62.71[44.79, 74.82]d)
併存疾患 b)
なし
5241(61.0)
50(0.95)
5156(60.1)
149(2.89)
67.70[55.51, 76.55]d)
N=解析対象例数、n=発現例数、NE:Not Evaluable
a) アラブ系は白人としてカウントされた。本剤群 12 例(不明 11 例、データなし 1 例)及び対照群 13 例(不明 11 例、データ
なし 2 例)は人種カテゴリーに含まれていない。
b) ベースラインの BMI≧30kg/m2、心血管異常、呼吸器疾患又は糖尿病のいずれかを有する場合に「あり」とした。データのな
い本剤群 300 例及び対照群 323 例は含まれていない。
c) 試験番号、接種群、スクリーニング時の年齢(18~55 歳、56~69 歳、70 歳以上)を因子とし、追跡期間の対数をオフセット
変数としたポアソン回帰モデル
d) 接種群を因子とし、追跡期間の対数をオフセット変数としたポアソン回帰モデル
e) 接種群を因子とした exact conditional ポアソン回帰モデル
f)
片側 97.5%CI
機構は、以下のように判断した。
海外併合解析の中間解析(DCO1)において、SDSD+LDSD 血清反応陰性有効性解析対象集団で VE の
両側 95.84%CI 下限は表 29 に示したとおりであり、下限に対して事前に設定された基準(20%)の妥当
性は必ずしも明確ではないものの、FDA のガイドライン等で示された下限値(30%)も上回っているこ
と24)も踏まえると、本剤の有効性は示されていると考える。さらに、SDSD+LDSD 血清反応陰性有効性
ITT 解析対象集団(試験中止の有無にかかわらず無作為化された接種群に基づく集団)における主要解
析(DCO2)と同様の解析及び接種レジメン別の部分集団解析においても、中間解析(DCO1)と同様の
結果が示された。
一部の部分集団については被験者数が非常に限られるため、各部分集団の有効性について明確にする
ことは困難であるが、免疫原性の成績等(7.R.2.2.1.2 項及び 7.R.2.2.3 項参照)を考慮すると、概ね全体
集団と傾向は異ならず、パンデミックの状況下においては本剤接種によるベネフィットが期待できると
考える。ただし、国別の成績のうち南アフリカ共和国の部分集団における VE が他の部分集団と比べて
低値を示したことについては、7.R.2.4 項で議論する。また、各部分集団について示された本剤の VE の
精度については、米国 D8110C00001 試験等のさらなるデータの集積を待って再度評価する必要がある。
24) Guidance for Industry: Development and Licensure of Vaccines to Prevent COVID-19. FDA;2020、WHO R&D Blueprint: novel Coronavirus. An
international randomized trial of candidate vaccines against COVID-19. WHO; 2020 等
47
バキスゼブリア筋注_アストラゼネカ株式会社_特例承認に係る報告書
173