よむ、つかう、まなぶ。
資料5-3 外国での新たな措置の報告状況 (17 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29460.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第3回 12/1)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
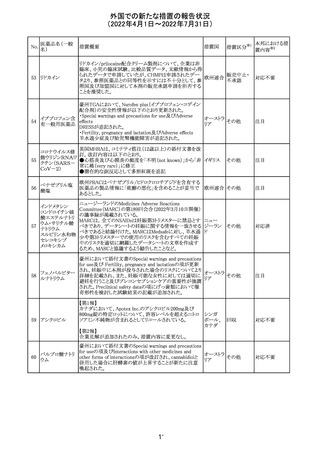
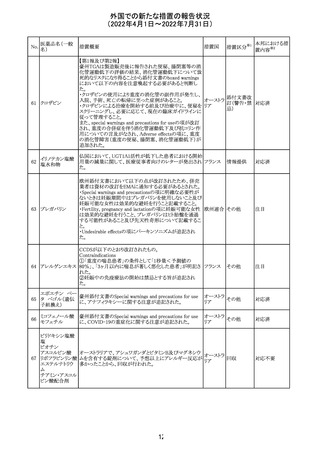
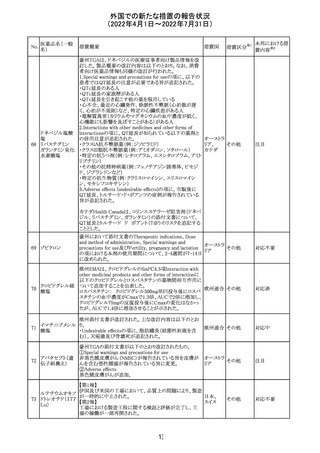
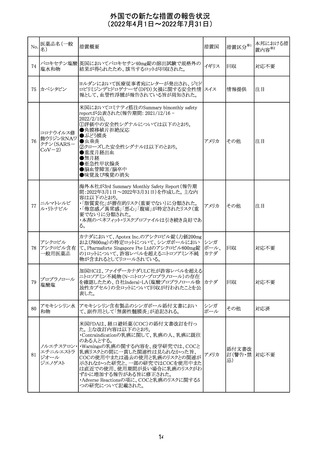
外国での新たな措置の報告状況
(2022年4月1日~2022年7月31日)
No.
医薬品名(一般
名)
措置概要
措置国
米国FDAは、ヒドロクロロチアジド/メトプロロール製剤の米
国添付文書を改訂した。改訂内容は以下のとおり。
・Contraindicationsの項に、メトプロロールの添付文書との
整合を図るため、次の患者を追加・変更した。「心原性
ショックまたは悪化した心不全」、「洞性徐脈、シックサイナ
ス症候群、および永久ペースメーカーを装着していない1度
以上のブロック」、「無尿症」、「メトプロロール酒石酸塩、ヒド
ロクロロチアジド、または他のスルホンアミド系薬剤に対する
ロサルタンカリウ
過敏症。」
ム・ヒドロクロロチ
・Warnings and Precautionsの項について、メトプロロールの
93 アジド
アメリカ
添付文書との整合を図るため、サブセクションを作成した。
メトプロロール酒
・Adverse Reactionsについて、「狭心症又は心筋梗塞の悪
石酸塩
化」、「心不全の悪化」、「房室ブロックの悪化」に関しては、
他の項で詳細に記載されている旨が追加された。
・Drug Interactionsの項について、メトプロロールとの相互
作用、ヒドロクロロチアジドとの相互作用のサブセクションが
作成された。
・Pregnancy及びLactationの項について、PLLR(妊婦及び
授乳婦に関するラベリングルール)に基づく変更がなされ
た。
措置区分※1
添付文書改
訂(警告・禁 対応不要
忌)
【第1報】
欧州EMAのPRACは、造血幹細胞移植(HSCT)後の静脈閉
塞性疾患(VOD)の予防に対し、本剤とBSC
(BestSupportiveCare)の併用群、BSC単独群で比較した第
3相海外臨床試験(15-007)(成人および小児患者372 例を
対象)において、本剤を使用することにベネフィットがない
結果が確認され中間解析の段階で試験が中止されたこと
を受けて、『本剤をVODの予防的治療として使用するべき
ではないと医療専門家に通知すること』を提案し、
ドイツ、
デフィブロチドナ
94
RMPVer9.0への更新が予定されているもの。
フランス、 その他
トリウム
【第2報】
欧州連合
本試験(15-007)中止後にJazz Pharmaceuticals社が試験内
容を再評価し、新たなベネフィットリスクプロファイルに変更
はないことを公表した。
【第3報】
独国BfArM医薬品医療機器研究所と仏国ANSM医薬品安
全庁は、欧州EMA勧告を受け、本剤を造血幹細胞移植
(HSCT)後の静脈閉塞性疾患(VOD)の予防に使用するべ
きではないこと通知したことを公表した。
95
イキサゾミブクエ
ン酸エステル
米国添付文書が改訂された。主な改訂内容は以下のとお
り。
・Indication and Usage, Warnings and Precautions及び
Clinical Studiesの項に、多発性骨髄腫における維持療法 アメリカ
に係る二つの臨床試験において死亡率が増加したことか
ら、管理下にある試験以外では、維持療法としての本剤の
使用は推奨されない旨が追記された。
トラスツズマブ(遺
96 伝子組換え)[後 オーストラリアにおいて、特定のロットが回収された。
続1]
97 アシクロビル
17
その他
オーストラ
回収
リア
英国において、アシクロビル静注製剤の一部ロットに同封さ
れている添付文書及び患者用リーフレットに誤記があるとし イギリス
て、医療従事者向けレターが配布されている。
本邦における措
置内容※2
情報提供
注目
対応中
対応不要
対応不要
(2022年4月1日~2022年7月31日)
No.
医薬品名(一般
名)
措置概要
措置国
米国FDAは、ヒドロクロロチアジド/メトプロロール製剤の米
国添付文書を改訂した。改訂内容は以下のとおり。
・Contraindicationsの項に、メトプロロールの添付文書との
整合を図るため、次の患者を追加・変更した。「心原性
ショックまたは悪化した心不全」、「洞性徐脈、シックサイナ
ス症候群、および永久ペースメーカーを装着していない1度
以上のブロック」、「無尿症」、「メトプロロール酒石酸塩、ヒド
ロクロロチアジド、または他のスルホンアミド系薬剤に対する
ロサルタンカリウ
過敏症。」
ム・ヒドロクロロチ
・Warnings and Precautionsの項について、メトプロロールの
93 アジド
アメリカ
添付文書との整合を図るため、サブセクションを作成した。
メトプロロール酒
・Adverse Reactionsについて、「狭心症又は心筋梗塞の悪
石酸塩
化」、「心不全の悪化」、「房室ブロックの悪化」に関しては、
他の項で詳細に記載されている旨が追加された。
・Drug Interactionsの項について、メトプロロールとの相互
作用、ヒドロクロロチアジドとの相互作用のサブセクションが
作成された。
・Pregnancy及びLactationの項について、PLLR(妊婦及び
授乳婦に関するラベリングルール)に基づく変更がなされ
た。
措置区分※1
添付文書改
訂(警告・禁 対応不要
忌)
【第1報】
欧州EMAのPRACは、造血幹細胞移植(HSCT)後の静脈閉
塞性疾患(VOD)の予防に対し、本剤とBSC
(BestSupportiveCare)の併用群、BSC単独群で比較した第
3相海外臨床試験(15-007)(成人および小児患者372 例を
対象)において、本剤を使用することにベネフィットがない
結果が確認され中間解析の段階で試験が中止されたこと
を受けて、『本剤をVODの予防的治療として使用するべき
ではないと医療専門家に通知すること』を提案し、
ドイツ、
デフィブロチドナ
94
RMPVer9.0への更新が予定されているもの。
フランス、 その他
トリウム
【第2報】
欧州連合
本試験(15-007)中止後にJazz Pharmaceuticals社が試験内
容を再評価し、新たなベネフィットリスクプロファイルに変更
はないことを公表した。
【第3報】
独国BfArM医薬品医療機器研究所と仏国ANSM医薬品安
全庁は、欧州EMA勧告を受け、本剤を造血幹細胞移植
(HSCT)後の静脈閉塞性疾患(VOD)の予防に使用するべ
きではないこと通知したことを公表した。
95
イキサゾミブクエ
ン酸エステル
米国添付文書が改訂された。主な改訂内容は以下のとお
り。
・Indication and Usage, Warnings and Precautions及び
Clinical Studiesの項に、多発性骨髄腫における維持療法 アメリカ
に係る二つの臨床試験において死亡率が増加したことか
ら、管理下にある試験以外では、維持療法としての本剤の
使用は推奨されない旨が追記された。
トラスツズマブ(遺
96 伝子組換え)[後 オーストラリアにおいて、特定のロットが回収された。
続1]
97 アシクロビル
17
その他
オーストラ
回収
リア
英国において、アシクロビル静注製剤の一部ロットに同封さ
れている添付文書及び患者用リーフレットに誤記があるとし イギリス
て、医療従事者向けレターが配布されている。
本邦における措
置内容※2
情報提供
注目
対応中
対応不要
対応不要