よむ、つかう、まなぶ。
資料5-3 外国での新たな措置の報告状況 (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29460.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第3回 12/1)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
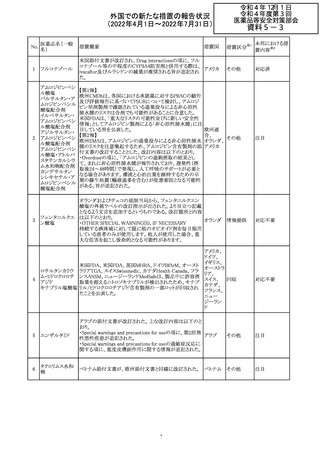
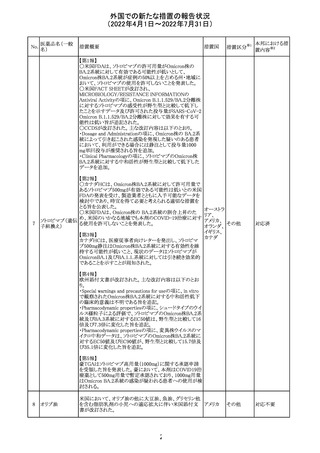
外国での新たな措置の報告状況
(2022年4月1日~2022年7月31日)
措置区分※1
本邦における措
置内容※2
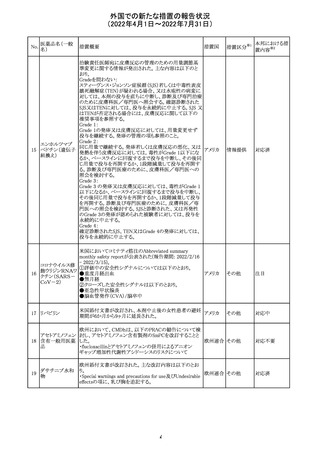
治験責任医師宛に皮膚反応の管理のための用量調節基
準変更に関する情報が発出された。主な内容は以下のと
おり。
Gradeを問わない:
スティーヴンス・ジョンソン症候群(SJS)若しくは中毒性表皮
壊死融解症(TEN)が疑われる場合、又は水疱性の病変に
対しては、本剤の投与を直ちに中断し、診断及び専門治療
のために皮膚科医/専門医へ照会する。確認診断された
SJS又はTENに対しては、投与を永続的に中止する。SJS 又
はTENが否定される場合には、皮膚反応に関して以下の
推奨事項を参照する。
Grade 1:
Grade 1の発疹又は皮膚反応に対しては、用量変更せず
投与を継続する。発疹の管理の項も参照のこと。
Grade 2:
エンホルツマブ
同じ用量で継続する。発疹若しくは皮膚反応の悪化、又は
15 ベドチン(遺伝子
アメリカ
発熱を伴う皮膚反応に対しては,毒性がGrade 1以下にな
組換え)
るか、ベースラインに回復するまで投与を中断し、その後同
じ用量で投与を再開するか、1段階減量して投与を再開す
る。診断及び専門医療のために、皮膚科医/専門医への
照会を検討する。
Grade 3:
Grade 3 の発疹又は皮膚反応に対しては、毒性がGrade 1
以下になるか、ベースラインに回復するまで投与を中断し、
その後同じ用量で投与を再開するか、1段階減量して投与
を再開する。診断及び専門医療のために,皮膚科医/専
門医への照会を検討する。SJSと診断された、又は再発性
のGrade 3の発疹が認められた被験者に対しては、投与を
永続的に中止する。
Grade 4:
確定診断されたSJS、TEN又はGrade 4の発疹に対しては、
投与を永続的に中止する。
情報提供
対応済
米国においてコミナティ筋注のAbbreviated summary
monthly safety reportが公表された(報告期間: 2022/2/16
- 2022/3/15)。
コロナウイルス修
①評価中の安全性シグナルについては以下のとおり。
飾ウリジンRNAワ
16
●重度月経出血
アメリカ
クチン(SARS-
●無月経
CoV-2)
②クローズした安全性シグナルは以下のとおり。
●亜急性甲状腺炎
●脳血管発作(CVA)/脳卒中
その他
注目
米国添付文書が改訂され、本剤中止後の女性患者の避妊
アメリカ
期間が6か月から9ヶ月に延長された。
その他
対応中
No.
医薬品名(一般
名)
17 リバビリン
措置概要
措置国
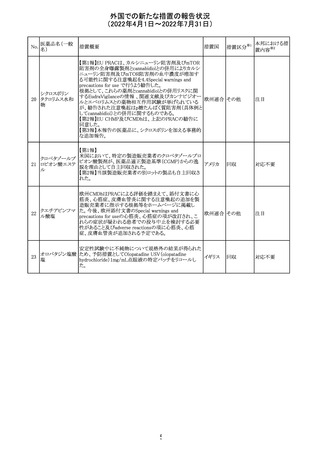
欧州において、CMDhは、以下のPRACの勧告について検
アセトアミノフェン 討し、アセトアミノフェン含有製剤のSmPCを改訂することと
18 含有一般用医薬 した。
欧州連合 その他
品
・flucloxacillinとアセトアミノフェンの併用によるアニオン
ギャップ増加性代謝性アシドーシスのリスクについて
ダサチニブ水和
19
物
欧州添付文書が改訂された。主な改訂内容は以下のとお
り。
欧州連合 その他
・Special warnings and precautions for use及びUndesirable
effectsの項に、乳び胸を追記する。
4
対応不要
対応済
(2022年4月1日~2022年7月31日)
措置区分※1
本邦における措
置内容※2
治験責任医師宛に皮膚反応の管理のための用量調節基
準変更に関する情報が発出された。主な内容は以下のと
おり。
Gradeを問わない:
スティーヴンス・ジョンソン症候群(SJS)若しくは中毒性表皮
壊死融解症(TEN)が疑われる場合、又は水疱性の病変に
対しては、本剤の投与を直ちに中断し、診断及び専門治療
のために皮膚科医/専門医へ照会する。確認診断された
SJS又はTENに対しては、投与を永続的に中止する。SJS 又
はTENが否定される場合には、皮膚反応に関して以下の
推奨事項を参照する。
Grade 1:
Grade 1の発疹又は皮膚反応に対しては、用量変更せず
投与を継続する。発疹の管理の項も参照のこと。
Grade 2:
エンホルツマブ
同じ用量で継続する。発疹若しくは皮膚反応の悪化、又は
15 ベドチン(遺伝子
アメリカ
発熱を伴う皮膚反応に対しては,毒性がGrade 1以下にな
組換え)
るか、ベースラインに回復するまで投与を中断し、その後同
じ用量で投与を再開するか、1段階減量して投与を再開す
る。診断及び専門医療のために、皮膚科医/専門医への
照会を検討する。
Grade 3:
Grade 3 の発疹又は皮膚反応に対しては、毒性がGrade 1
以下になるか、ベースラインに回復するまで投与を中断し、
その後同じ用量で投与を再開するか、1段階減量して投与
を再開する。診断及び専門医療のために,皮膚科医/専
門医への照会を検討する。SJSと診断された、又は再発性
のGrade 3の発疹が認められた被験者に対しては、投与を
永続的に中止する。
Grade 4:
確定診断されたSJS、TEN又はGrade 4の発疹に対しては、
投与を永続的に中止する。
情報提供
対応済
米国においてコミナティ筋注のAbbreviated summary
monthly safety reportが公表された(報告期間: 2022/2/16
- 2022/3/15)。
コロナウイルス修
①評価中の安全性シグナルについては以下のとおり。
飾ウリジンRNAワ
16
●重度月経出血
アメリカ
クチン(SARS-
●無月経
CoV-2)
②クローズした安全性シグナルは以下のとおり。
●亜急性甲状腺炎
●脳血管発作(CVA)/脳卒中
その他
注目
米国添付文書が改訂され、本剤中止後の女性患者の避妊
アメリカ
期間が6か月から9ヶ月に延長された。
その他
対応中
No.
医薬品名(一般
名)
17 リバビリン
措置概要
措置国
欧州において、CMDhは、以下のPRACの勧告について検
アセトアミノフェン 討し、アセトアミノフェン含有製剤のSmPCを改訂することと
18 含有一般用医薬 した。
欧州連合 その他
品
・flucloxacillinとアセトアミノフェンの併用によるアニオン
ギャップ増加性代謝性アシドーシスのリスクについて
ダサチニブ水和
19
物
欧州添付文書が改訂された。主な改訂内容は以下のとお
り。
欧州連合 その他
・Special warnings and precautions for use及びUndesirable
effectsの項に、乳び胸を追記する。
4
対応不要
対応済