よむ、つかう、まなぶ。
資料5-3 外国での新たな措置の報告状況 (45 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29460.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第3回 12/1)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
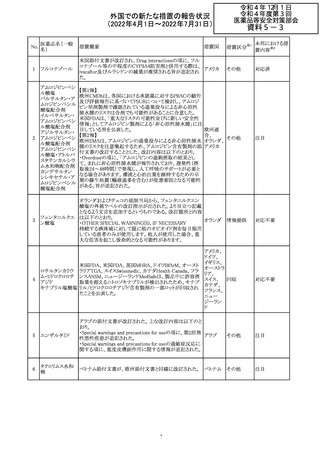
外国での新たな措置の報告状況
(2022年4月1日~2022年7月31日)
措置国
措置区分※1
本邦における措
置内容※2
アメリカ
その他
注目
豪州において添付文書が改訂された。改訂箇所は以下の
とおり。
・Special warnings and precautions for useの項に心筋症又
クエチアピンフマ
オーストラ
253
は心筋炎患者では投与の中止を考慮する旨が追記され
その他
ル酸塩
リア
た。
・Adverse effectsの項に製造販売後に報告された事象とし
て心筋症又は心筋炎が追加された。
注目
豪州添付文書が改訂され、シアノコバラミン(ビタミンB12)と
オーストラ
の併用時に、本剤はビタミンB12の吸収を阻害し、ビタミン
その他
リア
B12欠乏症を起こす恐れる恐れがある旨追記された。
注目
豪州において添付文書が改訂され、Interactions with
オーストラ
other medicines and other forms of interactionsの項にスル
その他
リア
ピリンが追記された。
対応済
No.
医薬品名(一般
名)
措置概要
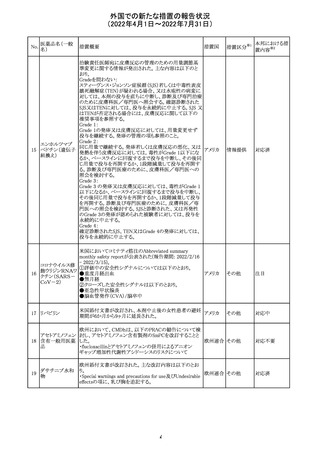
米国本社よりAbbreviated summary monthly safety report
(期間:2022/5/16 - 2022/6/15)を入手した。
3. SUMMARY OF SAFETY CONCERNS
重要な特定されたリスク:アナフィラキシー、心筋炎及び心
膜炎
重要な潜在的リスク:ワクチン接種に伴う疾患増強及びワク
チン関連の呼吸器疾患増強
重要な不足情報:妊婦・授乳婦、免疫不全患者、基礎疾患
のある患者、自己免疫疾患患者又は炎症性疾患患者、他
のワクチンとの相互作用、長期安全性、5歳未満の小児、ワ
クチンの有効性
報告期間中に新たな安全性の懸念は表れていない。
252
コロナウイルス修
飾ウリジンRNAワ 4. OVERVIEW OF SAFETY SIGNALS DURING THE
クチン(SARS- REPORTING INTERVAL
CoV-2)
報告対象期間中に新たに設定したシグナル:聴力低下
評価中のシグナル:角膜移植拒絶反応
クローズされたシグナル:慢性蕁麻疹、心膜炎・心筋炎
(CDSに追記)
6. CONCLUSION AND ACTIONS
報告期間における利用可能な安全性及び有効性データに
基づくと、本剤のベネフィット・リスクプロファイルは引き続き
良好である。集積安全性データ及びベネフィット・リスク解
析の評価に基づき、RSI(安全性参照情報)の変更や追加の
リスク最小化活動は必要とされない。
MAHは、すべての有害事象の報告を含む本剤の安全性を
引き続き検討し、安全性データの評価で重要な新たな情報
が得られた場合には、製品文書を改訂する。
254 ニザチジン
255
セルトラリン塩酸
塩
フルチカゾンプロ
ピオン酸エステル
米国において、HI-TECH PHARMACAL社製造のフルチ
サルメテロールキ
256
カゾンプロピオン酸塩点鼻製剤について容器の欠損、欠陥 アメリカ
シナホ酸塩・フル
を理由に回収が進行中であるとのこと。
チカゾンプロピオ
ン酸エステル
回収
対応不要
プレドニゾロン酢 台湾において、副腎皮質ホルモン外用剤の「使用上の注
257 酸エステル含有 意」「警告」の項に「ステロイド外用剤の離脱反応」について 台湾
一般用医薬品
追記するよう勧告が行われた。
その他
注目
45
(2022年4月1日~2022年7月31日)
措置国
措置区分※1
本邦における措
置内容※2
アメリカ
その他
注目
豪州において添付文書が改訂された。改訂箇所は以下の
とおり。
・Special warnings and precautions for useの項に心筋症又
クエチアピンフマ
オーストラ
253
は心筋炎患者では投与の中止を考慮する旨が追記され
その他
ル酸塩
リア
た。
・Adverse effectsの項に製造販売後に報告された事象とし
て心筋症又は心筋炎が追加された。
注目
豪州添付文書が改訂され、シアノコバラミン(ビタミンB12)と
オーストラ
の併用時に、本剤はビタミンB12の吸収を阻害し、ビタミン
その他
リア
B12欠乏症を起こす恐れる恐れがある旨追記された。
注目
豪州において添付文書が改訂され、Interactions with
オーストラ
other medicines and other forms of interactionsの項にスル
その他
リア
ピリンが追記された。
対応済
No.
医薬品名(一般
名)
措置概要
米国本社よりAbbreviated summary monthly safety report
(期間:2022/5/16 - 2022/6/15)を入手した。
3. SUMMARY OF SAFETY CONCERNS
重要な特定されたリスク:アナフィラキシー、心筋炎及び心
膜炎
重要な潜在的リスク:ワクチン接種に伴う疾患増強及びワク
チン関連の呼吸器疾患増強
重要な不足情報:妊婦・授乳婦、免疫不全患者、基礎疾患
のある患者、自己免疫疾患患者又は炎症性疾患患者、他
のワクチンとの相互作用、長期安全性、5歳未満の小児、ワ
クチンの有効性
報告期間中に新たな安全性の懸念は表れていない。
252
コロナウイルス修
飾ウリジンRNAワ 4. OVERVIEW OF SAFETY SIGNALS DURING THE
クチン(SARS- REPORTING INTERVAL
CoV-2)
報告対象期間中に新たに設定したシグナル:聴力低下
評価中のシグナル:角膜移植拒絶反応
クローズされたシグナル:慢性蕁麻疹、心膜炎・心筋炎
(CDSに追記)
6. CONCLUSION AND ACTIONS
報告期間における利用可能な安全性及び有効性データに
基づくと、本剤のベネフィット・リスクプロファイルは引き続き
良好である。集積安全性データ及びベネフィット・リスク解
析の評価に基づき、RSI(安全性参照情報)の変更や追加の
リスク最小化活動は必要とされない。
MAHは、すべての有害事象の報告を含む本剤の安全性を
引き続き検討し、安全性データの評価で重要な新たな情報
が得られた場合には、製品文書を改訂する。
254 ニザチジン
255
セルトラリン塩酸
塩
フルチカゾンプロ
ピオン酸エステル
米国において、HI-TECH PHARMACAL社製造のフルチ
サルメテロールキ
256
カゾンプロピオン酸塩点鼻製剤について容器の欠損、欠陥 アメリカ
シナホ酸塩・フル
を理由に回収が進行中であるとのこと。
チカゾンプロピオ
ン酸エステル
回収
対応不要
プレドニゾロン酢 台湾において、副腎皮質ホルモン外用剤の「使用上の注
257 酸エステル含有 意」「警告」の項に「ステロイド外用剤の離脱反応」について 台湾
一般用医薬品
追記するよう勧告が行われた。
その他
注目
45